Clear Sky Science · it
Interruzione dell'assemblaggio dell'inflammasoma NLRP3 mediante rimodellamento indotto dal ligando delle interfacce del dominio pirina
Perché è importante calmare l'infiammazione fuori controllo
Molte malattie croniche — dall'artrite e la gotta alle cardiopatie e alle neurodegenerazioni — sono alimentate da un sistema di allarme immunitario intracellulare iperattivo. Una componente chiave di questo allarme, chiamata inflammasoma NLRP3, ci aiuta a combattere le infezioni ma può anche guidare infiammazione dannosa quando funziona male. Questo studio descrive una nuova piccola molecola, denominata E9, che prende di mira un primo passo nell'attivazione di NLRP3, offrendo un'angolazione nuova per progettare farmaci che temperino l'infiammazione nociva senza spegnere completamente il sistema immunitario.
Un allarme cellulare con un lato oscuro
Quando il corpo percepisce pericolo, le cellule immunitarie assemblano l'inflammasoma NLRP3, un grande complesso proteico che funziona come un allarme molecolare. Una volta formato, questa struttura attiva un enzima chiamato caspasi-1, che a sua volta attiva potenti mediatori infiammatori, tra cui le citochine IL-1β e IL-18. Questi segnali sono fondamentali per combattere infezioni e rimuovere tessuto danneggiato. Ma se l'inflammasoma resta attivo troppo a lungo o si attiva al momento sbagliato, contribuisce a condizioni infiammatorie croniche che colpiscono articolazioni, vasi sanguigni, cervello e altri organi. Per questo i ricercatori di tutto il mondo sono alla ricerca di modi precisi per controllare NLRP3 senza sopprimere in modo generalizzato l'immunità.
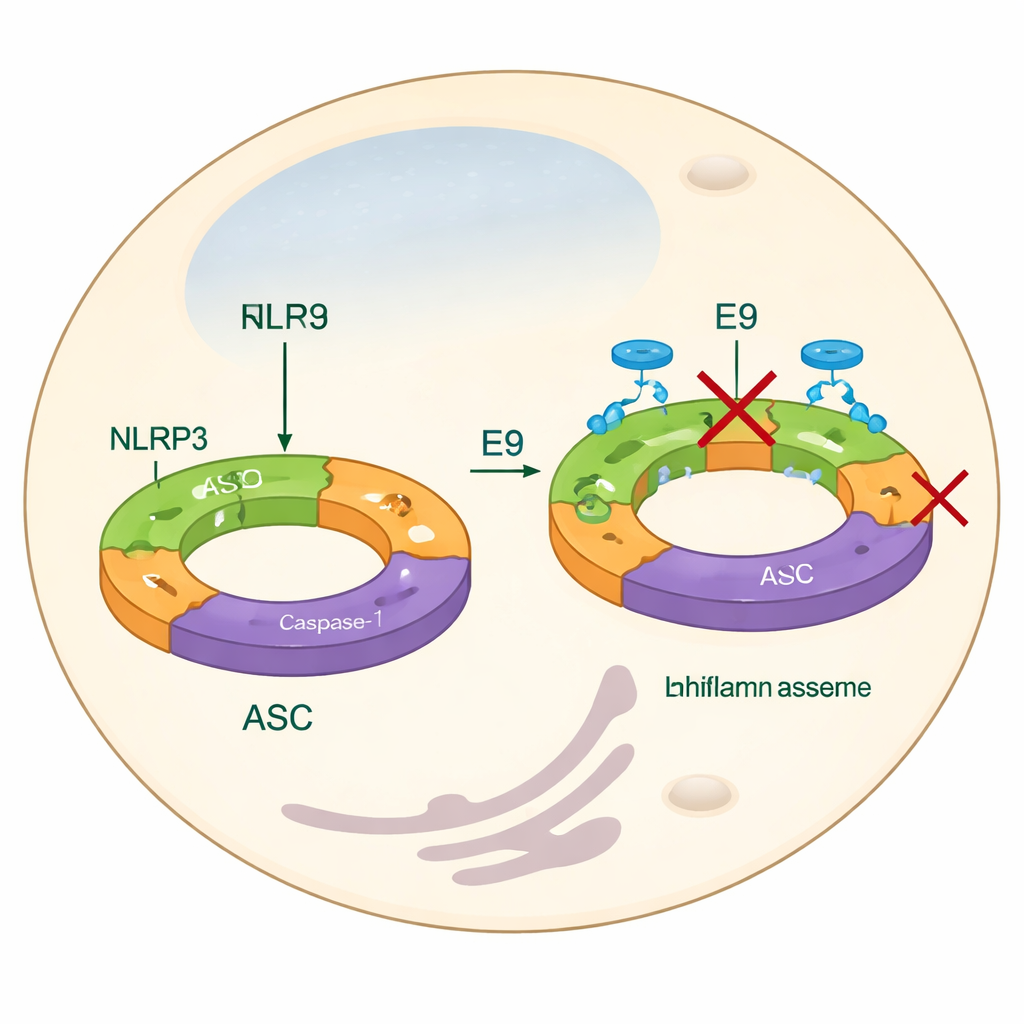
Oltre i bersagli farmacologici consueti
La maggior parte delle strategie attuali per domare NLRP3 si concentra sul blocco dei suoi prodotti finali — come l'IL-1β — o sull'interferenza con un dominio centrale simile a un motore che usa molecole energetiche come l'ATP. Pur essendo efficaci, questi approcci possono trascurare i primi passaggi di assemblaggio e non affrontano pienamente come le proteine NLRP3 si uniscono per formare una macchina funzionale. In questo lavoro, gli autori si concentrano invece sul dominio pirina, una parte di NLRP3 che aiuta le unità individuali a incastrarsi tra loro formando lunghi filamenti. Questi filamenti reclutano poi un'altra proteina adattatrice, ASC, che si agglomera in brillanti «speck» all'interno delle cellule — un marcatore visivo dell'attivazione dell'inflammasoma. Cercando sostanze chimiche che impediscano ai domini pirina di incastrarsi correttamente, il gruppo mira a impedire la formazione dell'inflammasoma sin dall'inizio.
Trovare una molecola che spezzi la catena
I ricercatori hanno screeningato una libreria di 1500 piccole molecole di nuova sintesi usando un intelligente test basato sulla luce. Hanno fuso pezzi spezzati di un'enzima luciferasi al dominio pirina di NLRP3; quando due domini pirina si avvicinavano, i frammenti enzimatici si riassemblavano e producevano luce. I composti che bloccavano il contatto pirina–pirina facevano diminuire il segnale luminoso. Da questo schermo sono emersi quattro candidati promettenti, con uno — E9 — che si è distinto per la sua forte e costante capacità inibitoria. Misurazioni successive con una tecnica chiamata termoforesi microscalare hanno mostrato che E9 si lega saldamente al dominio pirina a concentrazioni molto basse (submicromolari), confermando che il suo effetto non è un artefatto casuale ma il risultato di un'interazione specifica.
Osservare l'effetto nelle cellule vive
Per verificare se E9 potesse funzionare anche in un sistema vivo, il gruppo ha usato cellule di tipo immunitario umano ingegnerizzate per esprimere una versione fluorescente di ASC. Quando queste cellule sono stimolate con componenti batterici e un secondo segnale, NLRP3 si attiva e le proteine ASC si aggregano in brillanti speck che possono essere contati al microscopio. In presenza di E9, il numero di questi speck è diminuito in modo marcato, paragonabile o superiore ad alcuni noti inibitori di NLRP3. Ciò dimostra che interferire con i contatti del dominio pirina è sufficiente a ridurre l'assemblaggio dell'inflammasoma e i passaggi iniziali della morte cellulare infiammatoria, almeno in condizioni di laboratorio.
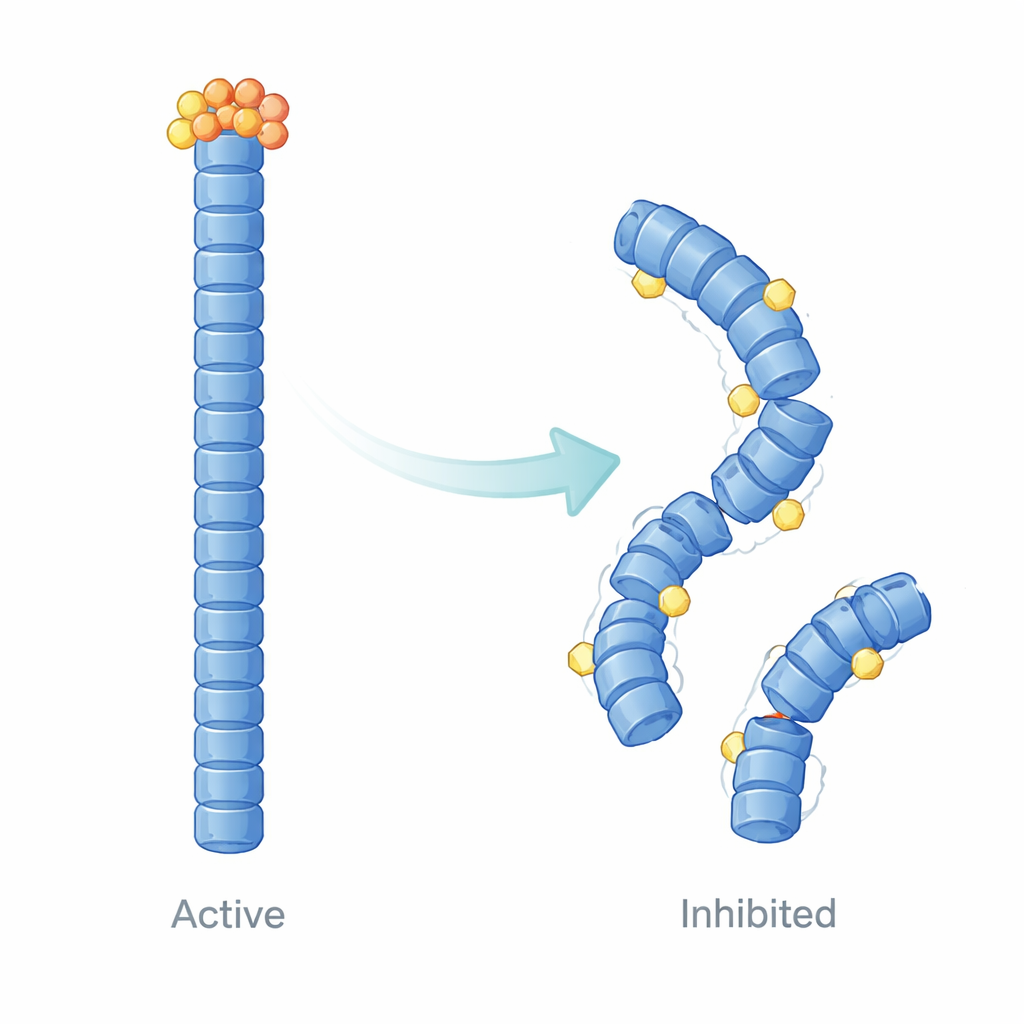
Come E9 rimodella l'impalcatura dell'inflammasoma
Oltre a misurare il legame, gli autori hanno usato modellizzazione strutturale al computer e simulazioni di dinamica molecolare per visualizzare come E9 modifica il comportamento dei filamenti di NLRP3 nel tempo. I loro calcoli suggeriscono che E9 si alloggi in superfici di contatto specifiche dove i domini pirina si toccano, allentando e rimodellando sottilmente il filamento. Invece di una struttura uniformemente stabile e cooperativa, il filamento diventa irregolare: le regioni vicine a E9 legato diventano più flessibili e perdono l'allineamento preciso, mentre altre parti risultano dinamicamente isolate. Questi cambiamenti smorzano i moti su larga scala e la comunicazione stretta necessaria per un efficiente reclutamento di ASC, fornendo una spiegazione fisica alla ridotta formazione di speck osservata nelle cellule.
Cosa potrebbe significare per le terapie future
Complessivamente, i risultati collocano E9 come prototipo per una nuova classe di farmaci mirati all'inflammasoma che agiscono interrompendo le interfacce tra i mattoni di NLRP3 anziché bloccando il suo utilizzo energetico o i prodotti finali. Sebbene il lavoro attuale sia limitato ad esperimenti in provetta, simulazioni al computer e cellule coltivate — e siano necessari ulteriori studi in animali e in esseri umani — dimostra che molecole a piccola scala progettate con cura possono rimodellare l'impalcatura stessa dell'inflammasoma. Per i pazienti con malattie guidate da infiammazione fuori controllo, farmaci focalizzati sulle interfacce potrebbero un giorno offrire un controllo più preciso, riducendo l'attivazione immunitaria dannosa lasciando intatte per lo più le difese essenziali.
Citazione: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Parole chiave: inflammasoma NLRP3, dominio pirina, inibitore a piccola molecola, immunità innata, piropotosi