Clear Sky Science · it
Profilazione molecolare del carcinoma renale a cellule chiare primario versus metastatico asincrono abbinato rivela eterogeneità nel microambiente immunitario tumorale
Perché questo studio sul cancro del rene è importante
Il cancro del rene si diffonde spesso in altre parti del corpo e le immunoterapie moderne non funzionano allo stesso modo per tutti i pazienti o per tutti i tumori. Questo studio indaga il carcinoma renale a cellule chiare — il tipo più comune di cancro renale — per capire come il sistema immunitario si comporta in modo diverso nel tumore primario del rene rispetto alle successive metastasi. Comprendere queste differenze potrebbe aiutare a spiegare perché alcuni tumori rispondono meglio ai trattamenti rispetto ad altri e potrebbe guidare cure più precise e personalizzate.
Uno sguardo ai tumori primari e metastatici
I ricercatori si sono concentrati su 19 pazienti a cui era stato asportato il tumore renale primario e che in seguito hanno sviluppato metastasi in sedi come polmone, osso, fegato, ghiandola surrenale, linfonodi o tessuto molle. Da questi pazienti hanno prelevato 42 campioni tumorali: 19 tumori primitivi e 23 metastasi non trattate. Hanno estratto RNA — una molecola che riflette quali geni sono attivi — da fette sottili di tessuto conservato e hanno usato il sequenziamento ad alto rendimento per catturare l’attività genica di migliaia di geni in ciascun campione. 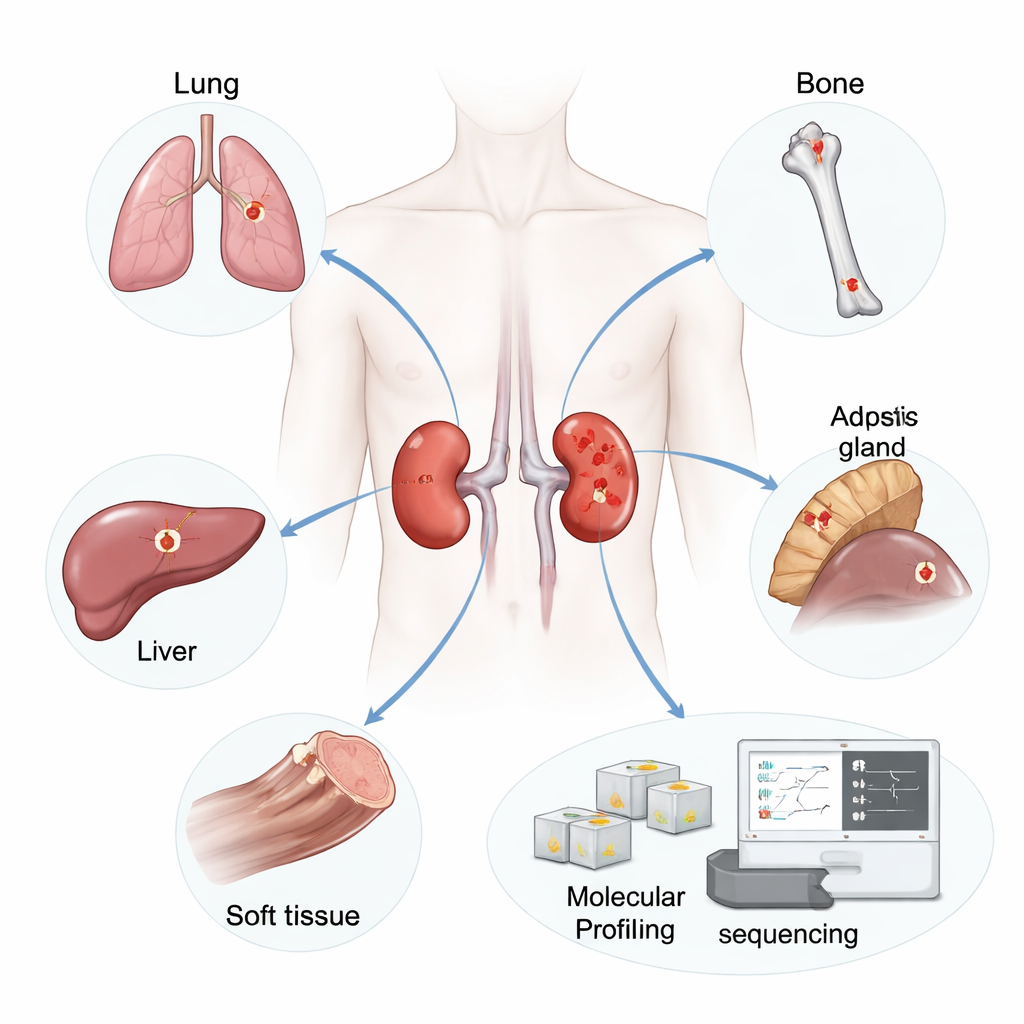
I tumori primari e metastatici sono distinti a livello molecolare
Quando il team ha analizzato i pattern di espressione genica, ha scoperto che i tumori renali primari tendevano a raggrupparsi tra loro e risultavano più simili tra loro che non alle loro metastasi. In altre parole, la metastasi di un paziente poteva essere più diversa dal suo tumore originale che non dalla metastasi di un’altra persona. Migliaia di geni risultavano più o meno attivi nelle metastasi rispetto ai primari. I tumori metastatici mostravano segnali più forti da programmi genici legati alla rapida divisione cellulare e a un comportamento aggressivo, inclusi percorsi coinvolti nei checkpoint del ciclo cellulare e nella produzione proteica. Al contrario, i tumori primari erano più arricchiti per percorsi di stress e segnali come l’ipossia (basso ossigeno) e la segnalazione infiammatoria, suggerendo pressioni biologiche diverse nel rene rispetto agli organi distanti.
Il paesaggio immunitario cambia con la diffusione del cancro
Oltre alla semplice attività genica, gli scienziati hanno stimato quali tipi di cellule immunitarie fossero presenti in ciascun tumore usando un metodo computazionale che deconvolge i dati di RNA bulk. Hanno scoperto una differenza notevole: i tumori renali primari contenevano una frazione significativamente maggiore di cellule T regolatorie (Treg), un tipo di cellula immunitaria che attenua le risposte immunitarie e può proteggere i tumori dall’attacco. I primari presentavano inoltre più cellule dendritiche in stato di riposo, monociti, cellule natural killer e linfociti CD8+. Al contrario, le metastasi erano più ricche di cosiddetti macrofagi M2 — cellule immunitarie spesso associate alla riparazione dei tessuti e a un ambiente che sostiene il tumore piuttosto che a uno che lo distrugge — insieme a più plasmacellule e cellule dendritiche attivate. 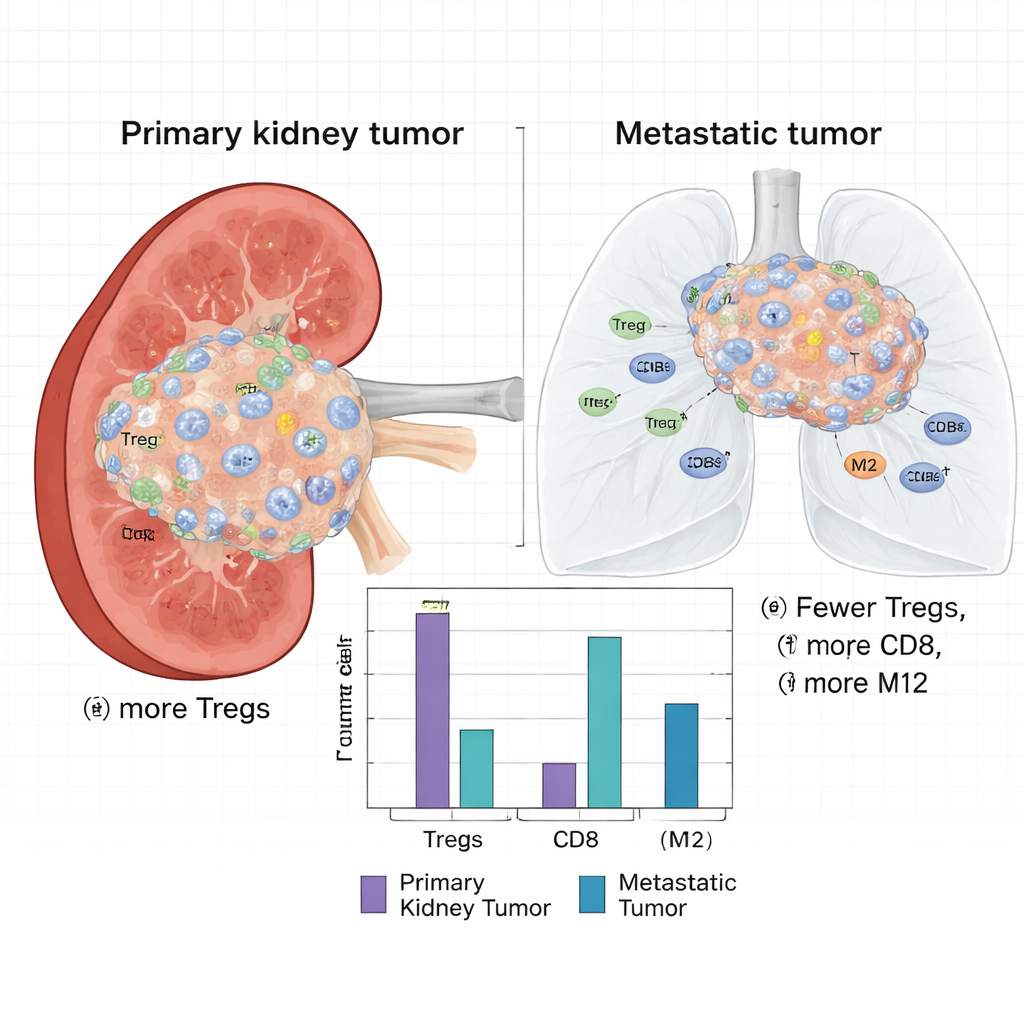
Metastasi polmonari e ossee raccontano storie immunitarie diverse
Quando i ricercatori si sono concentrati su specifiche sedi metastatiche, sono emerse sfumature importanti. Le metastasi polmonari mostravano aumentata attività di insiemi genici legati al controllo della divisione cellulare (il checkpoint G2M) e ai fattori di trascrizione E2F, oltre a elevata espressione di hornerin, una proteina collegata alla crescita dei vasi sanguigni nei tumori. I loro tumori renali primari abbinati erano invece più arricchiti per programmi genici correlati all’ipossia e presentavano nuovamente più Treg. Le metastasi ossee, al contrario, si distinguevano per una più forte attivazione della transizione epitelio-mesenchimale, un processo che aiuta le cellule tumorali a diventare più mobili e invasive. Queste lesioni ossee contenevano anche livelli più alti di macrofagi M2, mentre i primari che le hanno generate mostravano una maggiore espressione di HHLA2, una molecola checkpoint immunitario riconosciuta di recente. Complessivamente, questi risultati sottolineano che gli ambienti immunitari e molecolari delle metastasi non solo differiscono dai primari, ma variano anche tra le diverse sedi metastatiche.
Bilancio delle cellule immunitarie e risultati per i pazienti
Per capire cosa significano questi pattern immunitari per i pazienti, il gruppo ha esaminato tre grandi set di dati pubblici sul carcinoma renale a cellule chiare. Hanno usato lo stesso approccio computazionale per stimare i livelli di Treg e di linfociti T CD8+ e poi hanno collegato queste stime agli esiti di sopravvivenza. Nelle coorti analizzate, le persone i cui tumori presentavano la combinazione di bassi livelli di CD8+ (i principali linfociti T che uccidono il cancro) e alti livelli di Treg tendevano ad avere esiti peggiori in termini di sopravvivenza libera da progressione o sopravvivenza specifica per la malattia, anche dopo aver tenuto conto di età, grado e stadio del tumore. Pur restando lo stadio complessivo un fattore fortemente influente sulla sopravvivenza, l’equilibrio tra Treg soppressive e cellule CD8+ attaccanti è emerso come un marcatore aggiuntivo di rischio.
Cosa significa per la cura futura del cancro del rene
In termini accessibili, questo studio mostra che il tumore primario nel rene e le sue metastasi vivono in “quartieri” immunitari diversi. Il tumore primario sembra particolarmente abile a reclutare cellule pacificatrici che silenziano il sistema immunitario, il che può spiegare in parte perché i tumori renali in sede spesso rispondono meno bene all’immunoterapia rispetto alle depositi metastatici. Le metastasi, nel frattempo, sviluppano i propri sistemi di supporto locali che variano a seconda dell’organo. Queste intuizioni suggeriscono che i medici potrebbero a volte aver bisogno di analizzare sia il tumore renale che le metastasi per comprendere appieno la malattia di un paziente, e che trattamenti che combinano inibitori dei checkpoint immunitari con strategie mirate a Treg o macrofagi M2 potrebbero migliorare gli esiti per le persone con carcinoma renale a cellule chiare metastatico.
Citazione: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
Parole chiave: cancro del rene, microambiente tumorale, immunoterapia, metastasi, cellule T regolatorie