Clear Sky Science · it
Caratterizzazione trascrittomica dell'alterato splicing alternativo nei muscoli scheletrici di pazienti con sarcopenia
Perché i muscoli invecchiati perdono forza
La sarcopenia—la perdita graduale di massa e forza muscolare con l'età—è una delle principali cause per cui gli anziani incontrano difficoltà nelle attività quotidiane, dal salire le scale al portare la spesa. Questo studio esplora il muscolo invecchiato a livello dell'RNA, i messaggi che dicono alle cellule quali proteine produrre. Gli autori mostrano che nella sarcopenia molti di questi messaggi di RNA vengono tagliati e ricuciti in modi anomali, potenzialmente disturbando la produzione di energia nel muscolo e indicando nuovi possibili bersagli terapeutici.
Perdita muscolare e il sistema di “editing” genetico del corpo
I nostri geni sono scritti nel DNA, ma le cellule lavorano a partire dalle copie in RNA di quei geni. Prima che un messaggio di RNA venga utilizzato, le cellule lo rifiniscono e lo splicano—simile al montaggio di un film—così che un singolo gene possa produrre diverse versioni di una proteina. Questo processo, chiamato splicing alternativo, è particolarmente attivo nel muscolo, che richiede proteine finemente regolate per contrarsi, ripararsi e adattarsi all'esercizio. Quando lo splicing non funziona correttamente, si possono produrre versioni proteiche errate o perdere versioni importanti, contribuendo a malattie come la distrofia muscolare e alcuni disturbi cerebrali. Gli autori hanno ipotizzato che un analogo livello nascosto di errore nell'editing dell'RNA potesse guidare la sarcopenia.
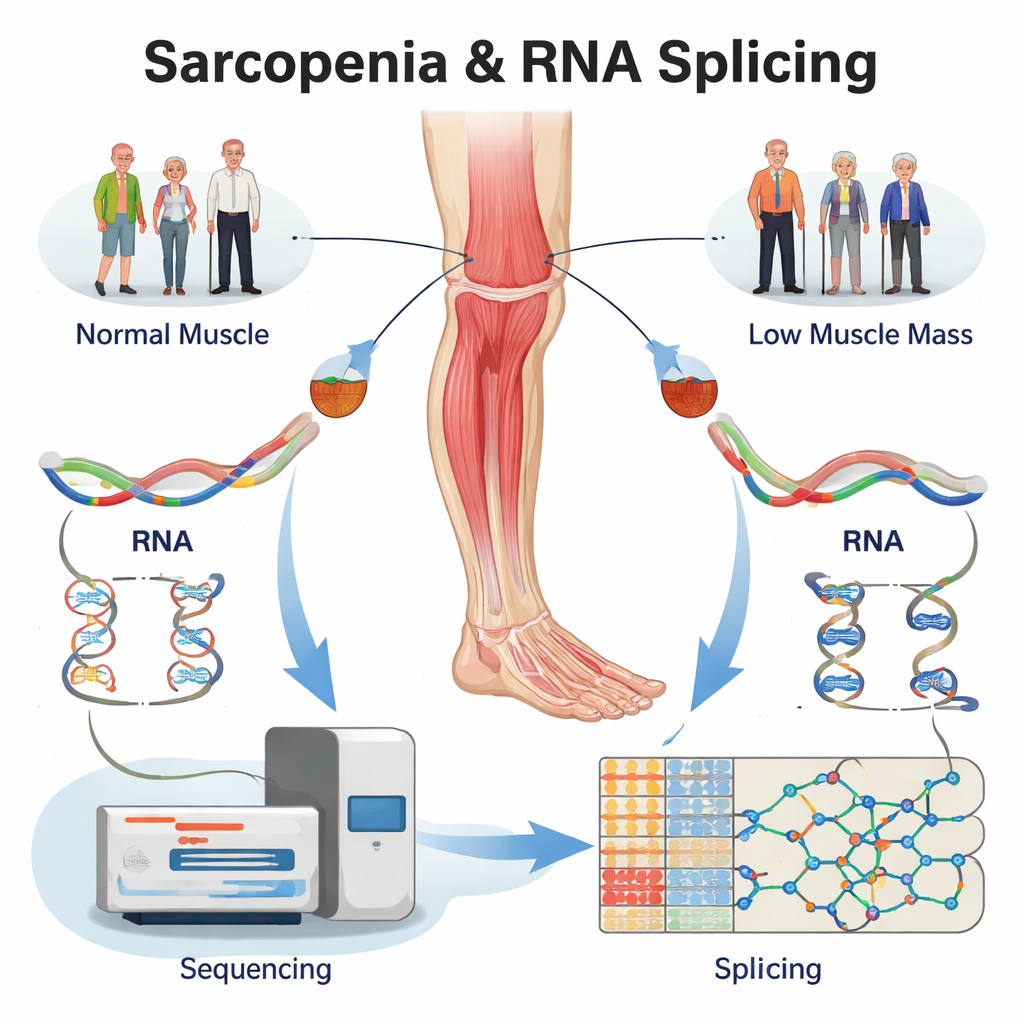
Rileggere dati esistenti per trovare errori nascosti nell'RNA
Invece di reclutare nuovi volontari, il team ha rianalizzato un ampio dataset di sequenziamento dell'RNA già disponibile proveniente da biopsie del muscolo della coscia umana. I campioni provenivano da quattro gruppi: anziani con sarcopenia conclamata, persone con solo bassa massa muscolare, persone con solo bassa forza muscolare e controlli sani di pari età. Con software specializzati hanno prima confermato che centinaia di geni risultavano sovra- o sottoespressi nei muscoli malati. Ancora più importante, hanno poi esaminato come l'RNA di ciascun gene fosse splicato, catalogando più di 5.000 cambiamenti nello splicing nei tre gruppi problematici rispetto al muscolo sano. Questi cambiamenti si concentravano in pochi tipi fondamentali—come il salto di un esone o la scelta di un sito di taglio alternativo—pattern noti per alterare profondamente la struttura delle proteine.
Le fabbriche di energia e le vie del “contagiri” cellulare sono disturbate
I cambiamenti nello splicing sono emersi in geni centrali per la biologia muscolare. Molti geni interessati costruiscono parti dei mitocondri, le piccole fabbriche energetiche che alimentano la contrazione muscolare. Nel muscolo sarcopenico, 16 geni coinvolti nella fosforilazione ossidativa—il processo che trasforma i nutrienti in energia utilizzabile—mostravano splicing alterato, in particolare componenti dei complessi mitocondriali che gestiscono il trasporto di elettroni e la pompa di protoni. Altri cambiamenti sono apparsi in geni che sintetizzano o utilizzano NAD⁺, una molecola chiave per l'energia e la riparazione cellulare. Piuttosto che variare semplicemente in quantità, enzimi importanti come CD38, PARP2 e diverse sirtuine producevano varianti di RNA differenti, suggerendo che l'equilibrio tra produzione e consumo di NAD⁺ sia distorto a livello di splicing. I geni interessati si raggruppavano anche in note vie di segnalazione muscolare, incluse le vie AMPK e FoxO, che funzionano come indicatori di carburante e risponditori allo stress cellulare.
Modelli condivisi attraverso le fasi diverse—e tra le specie
In modo sorprendente, molti degli stessi geni mostravano cambiamenti nello splicing non solo nelle persone con sarcopenia piena, ma anche in quelle con sola bassa massa muscolare o sola bassa forza. Questo suggerisce che lo splicing anomalo inizi precocemente e attraversi le diverse manifestazioni cliniche della malattia. Per verificare se questi cambiamenti potessero essere riprodotti in un modello animale, i ricercatori indussero atrofia muscolare nei topi con il cortisone desametasone, un metodo standard per imitare alcune caratteristiche della sarcopenia. I topi svilupparono presa manuale più debole e prestazioni peggiori nei test di corsa e equilibrio. Quando il team sequenziò l'RNA muscolare dei topi, trovò nuovamente centinaia di geni con splicing alterato. Circa un quinto di questi sovrapponeva ai geni umani associati alla sarcopenia, e molti erano coinvolti nel controllo della trascrizione, della struttura della cromatina e dello stesso splicing—interruttori di livello superiore che possono rimodellare l'intera produzione proteica di una cellula.
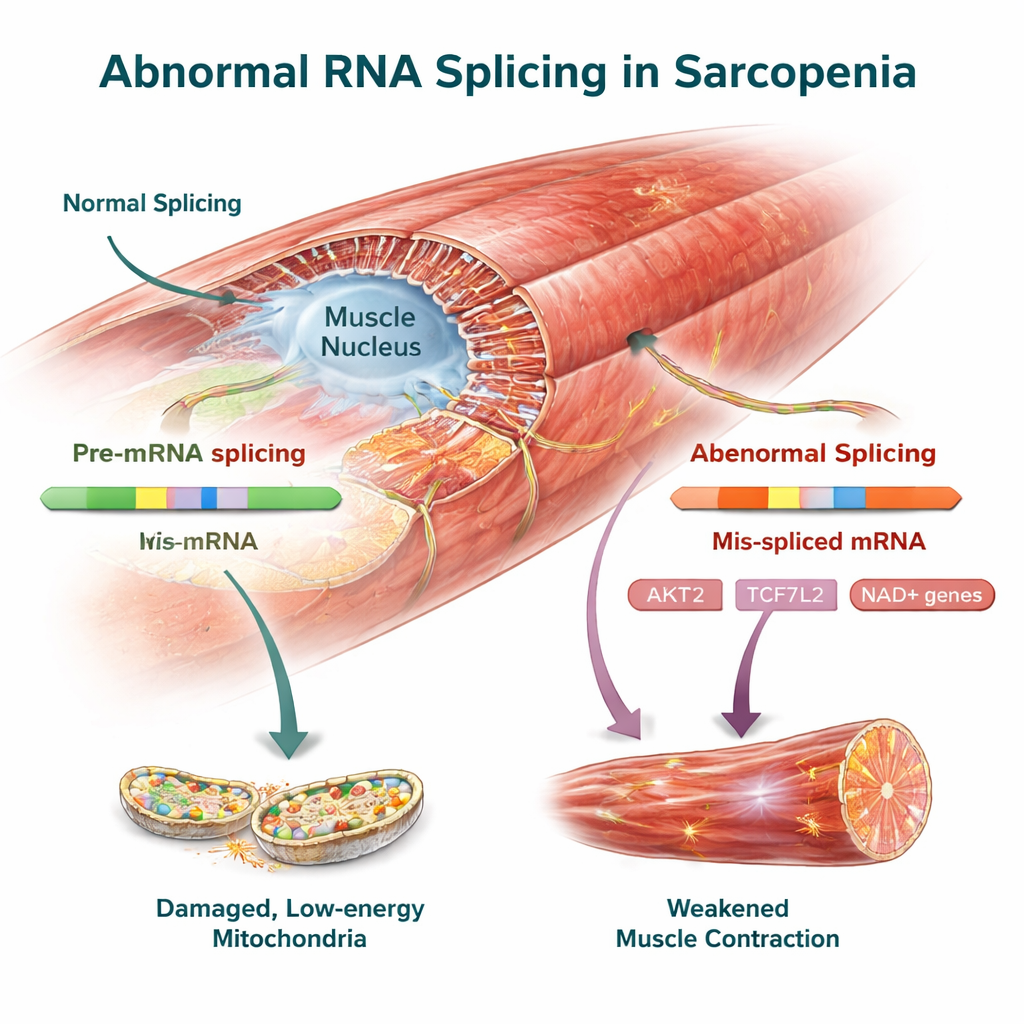
Geni chiave del controllo muscolare come possibili bersagli terapeutici
Tra i cambiamenti conservati tra le specie vi erano diversi geni già collegati alla salute muscolare. AKT2, un regolatore centrale della crescita e della sintesi proteica nel muscolo, mostrava spostamenti nello splicing distinti sia negli esseri umani sia nei topi che potrebbero ridurne la capacità di mantenere la massa muscolare. TCF7L2, parte della via di segnalazione Wnt, insieme a FMNL2 e USP40, che contribuiscono a organizzare l'impalcatura interna del muscolo e il controllo della qualità proteica, presentavano anch'essi varianti di RNA alterate. Il team ha confermato sperimentalmente questi cambiamenti nello splicing nel muscolo dei topi, rafforzando l'ipotesi che siano caratteristiche reali della malattia piuttosto che artefatti dell'analisi dei dati.
Cosa significa per la prevenzione della fragilità
Per i non specialisti, il messaggio è che la sarcopenia non riguarda solo il «logoramento» dei muscoli o l'accensione/spegnimento dei geni. Coinvolge anche un diffuso errore di editing dei messaggi di RNA che guida come le cellule muscolari costruiscono e mantengono i loro meccanismi, in particolare i sistemi che generano energia e percepiscono lo stress. Poiché lo splicing può, in linea di principio, essere corretto con farmaci basati su RNA progettati in modo preciso, gli errori di splicing conservati scoperti qui—in particolare in geni come AKT2 e TCF7L2—offrono una nuova serie di piste per terapie volte ad aiutare i muscoli invecchiati a restare più forti più a lungo.
Citazione: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Parole chiave: sarcopenia, invecchiamento muscolare, splicing dell'RNA, mitocondri, AKT2