Clear Sky Science · it
Modello fenomenologico della stabilizzazione della transtiretina
Perché questo è importante per pazienti e famiglie
L’amiloidosi da transtiretina è una condizione grave in cui una proteina presente nel sangue, la transtiretina (TTR), si sfalda e i suoi frammenti possono aggregarsi formando depositi dannosi nel cuore e nei nervi. Nuovi farmaci come tafamidis e acoramidis sono progettati per mantenere questa proteina nella sua forma sicura a quattro subunità, e hanno già migliorato gli esiti di molte persone. Tuttavia i medici osservano un effetto sorprendente nei pazienti trattati: i livelli plasmatici di TTR aumentano di oltre il 30%, e non è ovvio il perché. Questo articolo impiega un modello semplificato basato sulla matematica per esplorare cosa potrebbe accadere all’interno dell’organismo e cosa ciò implichi sul reale meccanismo d’azione di questi farmaci. 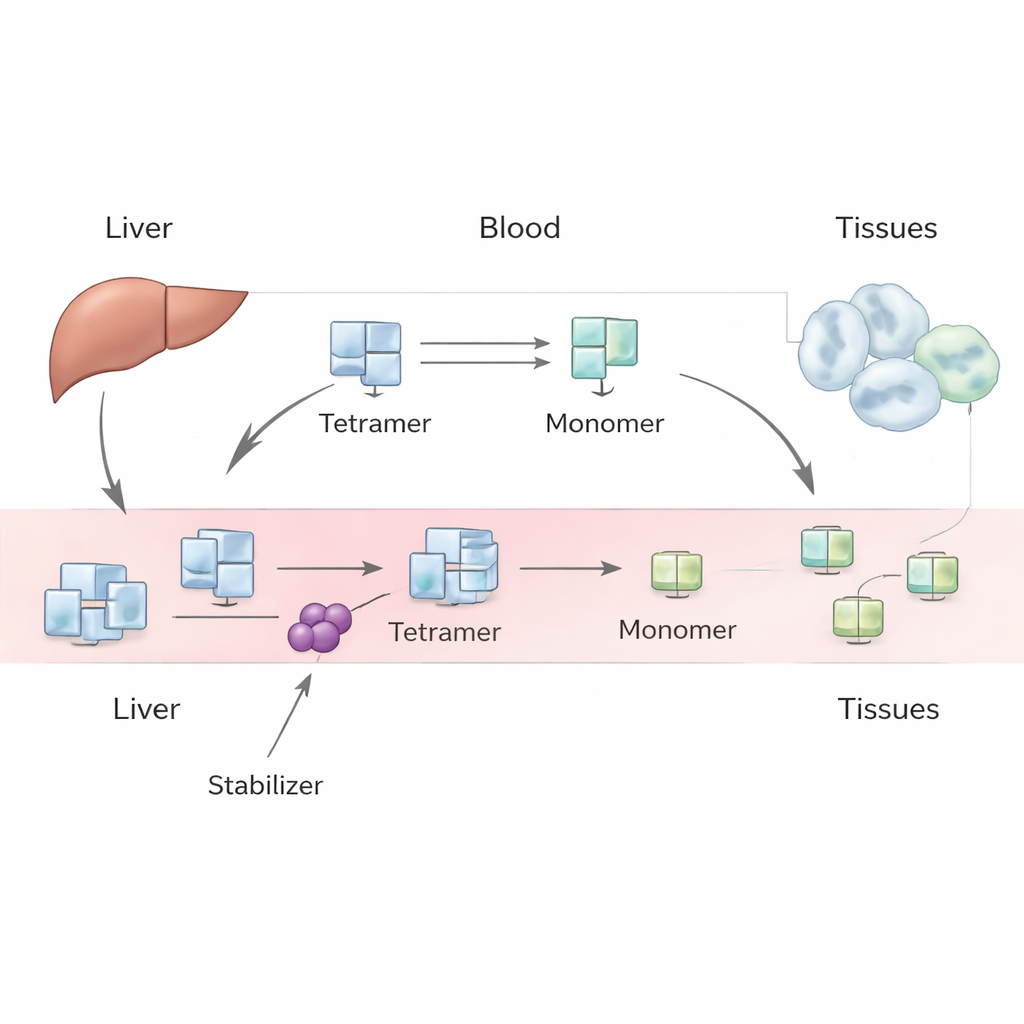
Una proteina che può aiutare o nuocere
La TTR è prodotta principalmente nel fegato e normalmente circola nel sangue come un insieme stabile di quattro subunità identiche, detto tetramero. Trasporta l’ormone tiroideo e la vitamina A. In alcune condizioni, tra cui l’invecchiamento o varianti genetiche ereditarie, questo tetramero può disassemblarsi in singole subunità, o monomeri. Questi monomeri possono ripiegarsi in modo errato e aggregarsi in fibrille amiloidi, che danneggiano i tessuti e portano all’amiloidosi da transtiretina del cuore (cardiomiopatia) o dei nervi (neuropatia). Farmaci come tafamidis e acoramidis sono pensati per legare il tetramero e renderne più difficile la dissociazione, rallentando la progressione della malattia. Tuttavia, quando i pazienti iniziano questi trattamenti, i livelli misurati di TTR nel sangue aumentano in modo costante, e questo aumento è maggiore di quanto suggerirebbero semplici esperimenti di laboratorio.
Costruire un quadro semplice di un sistema complesso
Gli autori affrontano questo enigma con un modello fenomenologico—cioè che si concentra sul comportamento osservabile complessivo piuttosto che su ogni dettaglio microscopico. Nel loro schema, il fegato produce tetrameri di TTR a un ritmo costante, che entrano poi nel circolo sanguigno. Una volta in circolazione, i tetrameri possono dissociarsi in monomeri e riassemblarsi, e sia i tetrameri sia i monomeri possono essere rimossi dal sangue tramite captazione nei tessuti e degradazione. Scrivendo un paio di equazioni di bilancio di massa per tetrameri e monomeri, il gruppo esplora diversi scenari: uno in cui i monomeri si riassemblano prevalentemente in tetrameri, uno in cui vengono rapidamente eliminati, e un caso intermedio in cui entrambi i processi sono rilevanti. Gli autori usano studi storici con traccianti nell’uomo e dati sperimentali moderni per stimare grandezze chiave, come la velocità di clearance dei tetrameri, la rapidità con cui si disfano e quanto efficacemente i farmaci rallentino questa dissociazione.
Perché la sola stabilizzazione del tetramero non basta
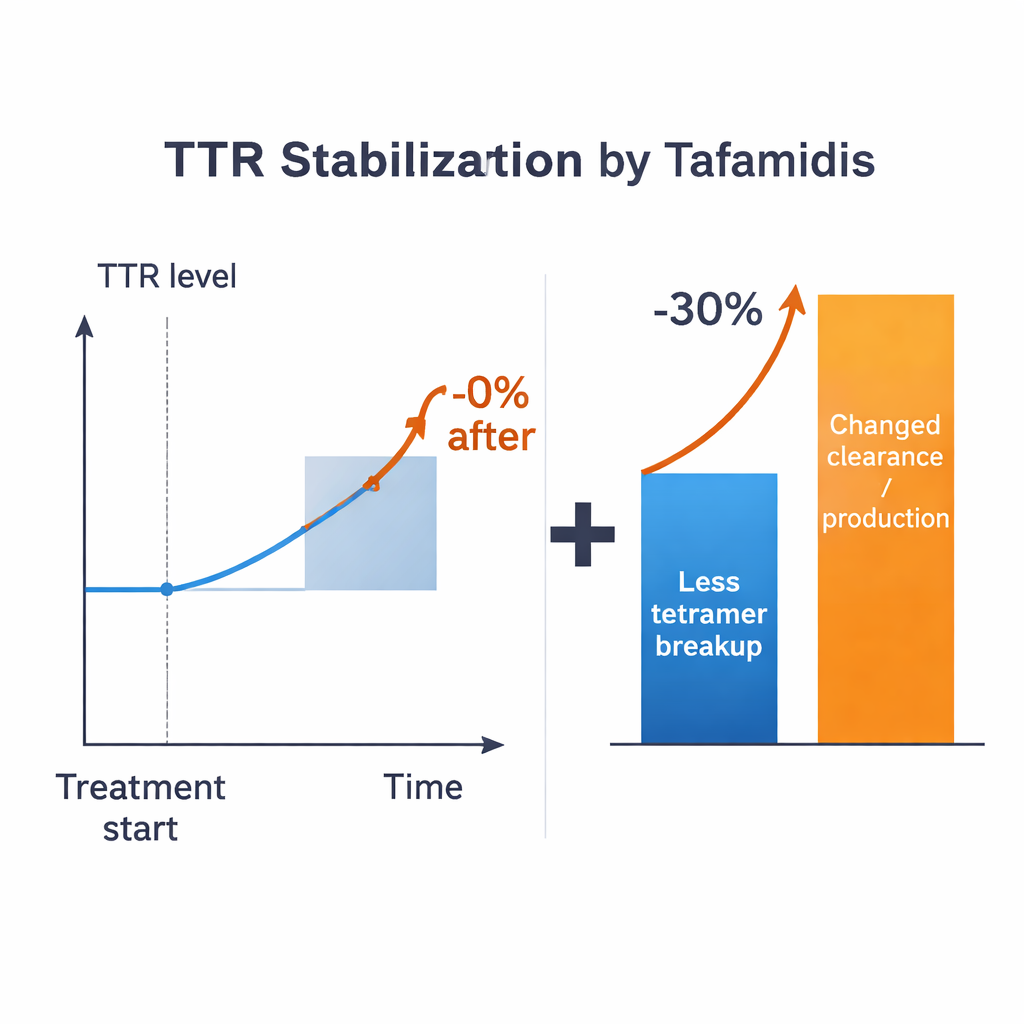
Con queste stime, i ricercatori pongono una domanda puntuale: se un farmaco potesse impedire perfettamente che i tetrameri si separino, di quanto salirebbero i livelli plasmatici di TTR? In tutti i regimi plausibili la risposta è modesta—dell’ordine del 15% al massimo per valori parametrici tipici, e spesso meno, a seconda di come vengono gestiti i monomeri. Ciò è ben al di sotto dell’aumento >30% osservato nei pazienti trattati. La discrepanza rimane anche concedendo ampia incertezza sui parametri noti. Il modello suggerisce quindi che il semplice rallentamento della dissociazione dei tetrameri non possa, da solo, spiegare l’intero effetto clinico. Altri processi che controllano quanto velocemente la TTR viene prodotta, captata dalle cellule o degradata devono anch’essi modificarsi in presenza degli stabilizzatori.
Indizi dai livelli di farmaco e da esperimenti intelligenti
Per mettere in relazione l’esposizione al farmaco con il comportamento della TTR, gli autori combinano un modello farmacocinetico di base del tafamidis (come il farmaco si muove nell’organismo nel tempo) con saggi specializzati di “scambio di subunità”. In questi esperimenti, tetrameri di TTR marcati e non marcati vengono mescolati in plasma umano, e lo scambio graduale di subunità rivela quanto spesso i tetrameri si disfano. Misurare questo processo a diverse concentrazioni di farmaco fornisce un legame diretto e basato sui dati tra livello di tafamidis e stabilità efficace del tetramero, senza la necessità di sapere quanto farmaco sia legato all’albumina o all’ormone tiroideo. Questo collegamento fenomenologico alimenta il modello e aggira in modo pulito molte incognite biochimiche. Tuttavia, anche con questo vantaggio, i calcoli limitano ancora l’aumento atteso della TTR a circa metà dell’incremento osservato clinicamente, rafforzando l’idea che cambiamenti nella clearance, nella internalizzazione, nella degradazione o persino nella sintesi debbano far parte della spiegazione.
Cosa significa per il futuro
Per i non specialisti, il messaggio chiave è che questi farmaci stabilizzanti probabilmente fanno più che semplicemente “incollare” i tetrameri di TTR. Probabilmente influenzano anche come l’organismo produce, rimuove o ricicla la proteina. Gli autori sostengono che modelli semplici e trasparenti come il loro sono potenti perché mettono in luce tali lacune nella nostra comprensione e indicano esperimenti concreti—forse misurare direttamente la velocità di eliminazione dei monomeri, quanto rapidamente le diverse forme di TTR vengono captate dalle cellule, o se la TTR legata al farmaco viene trattata diversamente rispetto alla proteina non legata. Risposte migliori a queste domande non solo migliorerebbero il trattamento dell’amiloidosi da transtiretina ma potrebbero anche rivelare regole generali su altre malattie in cui proteine normali si trasformano in aggregati dannosi.
Citazione: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Parole chiave: amiloidosi da transtiretina, stabilizzazione delle proteine, tafamidis, modellizzazione farmacocinetica, malattie da amiloide