Clear Sky Science · it
La stabilizzazione mirata del fattore inducibile dall'ipossia 1-alpha (HIF1A) durante la maturazione in vitro dei complessi cumulo-oocita bovini aumenta i tassi di blastocisti
Perché modificare la rilevazione dell'ossigeno nelle uova è importante
L'allevamento bovino moderno si basa in larga misura su embrioni prodotti in laboratorio, ma il successo è tutt'altro che garantito: solo circa un terzo degli oociti raggiunge la fase cruciale di blastocisti, quando sono pronti per essere trasferiti in una bovina. Questo studio pone una domanda apparentemente semplice ma di ampia rilevanza per l'allevamento animale e la riproduzione assistita: se riproduciamo più fedelmente le condizioni di basso ossigeno che gli oociti sperimentano naturalmente all'interno dell'ovaio—potenziando in modo controllato una proteina chiave che rileva l'ossigeno—riusciamo ad aiutare un maggior numero di embrioni a svilupparsi con successo?
La vita inizia in una nicchia a basso ossigeno
Nell'ovaio, ogni oocita in sviluppo è avvolto in un ammasso di cellule di sostegno noto come cumulo, insieme formando il complesso cumulo–oocita. Sebbene l'irrorazione sanguigna dell'ovaio aumenti con la crescita dei follicoli, i vasi sanguigni non raggiungono l'immediato intorno dell'oocita. L'ossigeno deve diffondere, creando una zona moderatamente povera di ossigeno, o ipossica, attorno all'oocita che matura. In questa nicchia, un sensore intracellulare chiamato HIF1A aiuta le cellule ad adattarsi modulando metabolismo e produzione ormonale. Lavori precedenti hanno dimostrato che bloccare HIF1A compromette la maturazione dell'oocita e riduce drasticamente la formazione di embrioni, evidenziando questa proteina come coordinatore centrale della competenza oocitaria—la capacità di un oocita di essere fecondato e svilupparsi in un embrione sano.
Usare un farmaco per mettere a punto il sensore d'ossigeno dell'oocita
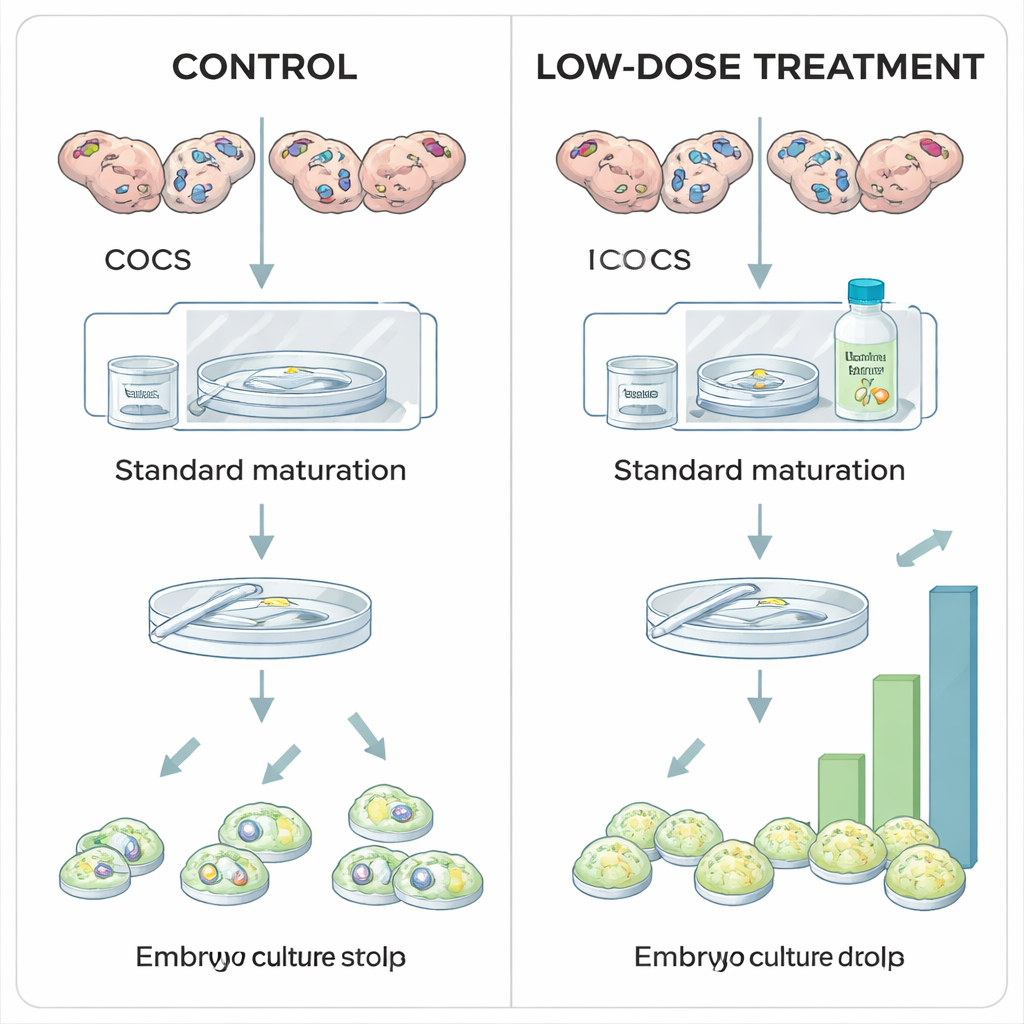
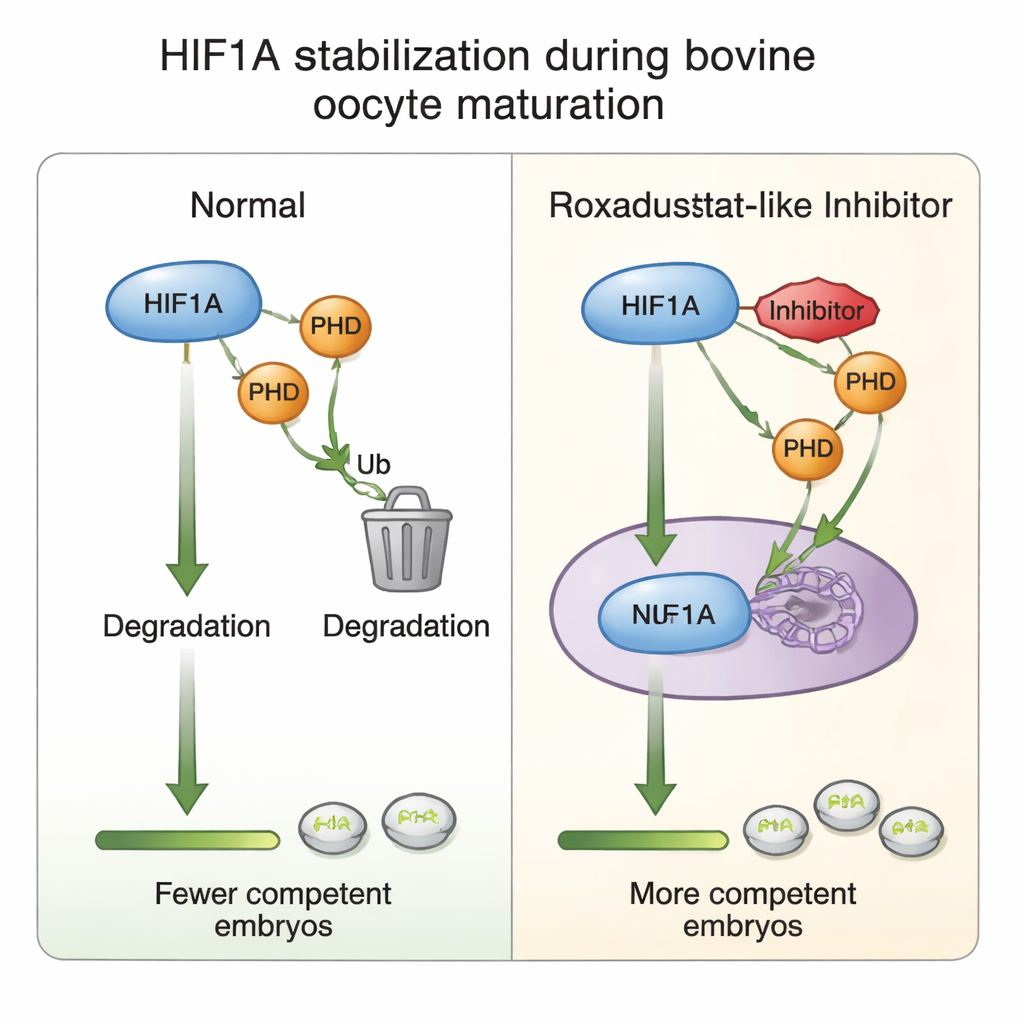
I ricercatori hanno esplorato se stabilizzare moderatamente HIF1A durante la maturazione in vitro degli oociti bovini potesse aumentare la resa di embrioni. Nei protocolli standard in vitro, i complessi cumulo–oocita vengono maturati sotto livelli di ossigeno atmosferico, per ragioni pratiche più che biologiche. In questo lavoro, oociti raccolti da ovaie di macello sono stati divisi in gruppi ed esposti durante le 24 ore di maturazione a diverse dosi di Roxadustat, un farmaco già impiegato in medicina umana per il trattamento dell'anemia. Il Roxadustat agisce bloccando una famiglia di enzimi chiamati prolil idrossilasi (PHD) che normalmente marcano HIF1A per la degradazione quando l'ossigeno è abbondante. Inibendo le PHD, il Roxadustat permette l'accumulo della proteina HIF1A anche a livelli più elevati di ossigeno, ricreando parzialmente il segnale di ipossia che l'oocita percepirebbe in vivo.
Più blastocisti alla dose giusta, danno a dosi più elevate
Quando il team ha esaminato l'andamento di oociti ed embrioni dopo il trattamento, è emerso un quadro chiaro. Una bassa dose di Roxadustat (25 micromolare) non ha modificato quante cellule completavano la maturazione né quante uova fecondate iniziavano la divisione, ma ha aumentato in modo significativo la proporzione che raggiungeva lo stadio di blastocisti. In altre parole, i primi step non sono stati alterati, eppure più embrioni hanno portato a termine con successo il percorso impegnativo fino a diventare blastocisti—suggerendo che una modesta stabilizzazione di HIF1A migliora la qualità intrinseca dell'oocita. Al contrario, la dose più alta (100 micromolare) ha ridotto la percentuale di oociti che maturavano, e quando lo stesso inibitore è stato applicato più tardi, durante il periodo di coltura embrionale di otto giorni, dosi elevate hanno ridotto drasticamente la formazione di blastocisti senza alterare le prime divisioni cellulari. Questi risultati indicano che "la giusta" attività di HIF1A durante la maturazione è benefica, mentre un'attivazione eccessiva o protratta è dannosa.
Cosa succede all'interno delle cellule di supporto dell'oocita
Per comprendere il meccanismo di questa messa a punto chimica, gli autori hanno analizzato le cellule del cumulo che circondano ciascun oocita. Hanno osservato che la maturazione in generale aumenta l'attività genica di HIF1A, ma l'aggiunta di Roxadustat paradossalmente ha ridotto l'mRNA di HIF1A lasciando però invariati i livelli proteici di HIF1A—un indizio che le cellule possono abbassare la produzione genica una volta che la proteina è sufficientemente stabilizzata, una sorta di freno intrinseco contro la sovraattivazione. I livelli di PHD2, l'enzima PHD più sensibile all'ossigeno, sono aumentati in risposta al farmaco, rafforzando il suo ruolo nel circuito di rilevazione dell'ossigeno. A dosi più elevate del farmaco, marker di proliferazione cellulare e della matrice adesiva che aiuta l'espansione delle cellule del cumulo attorno all'oocita sono risultati ridotti, in linea con il calo osservato nella maturazione e nella formazione di embrioni. Tutto ciò supporta l'idea che un'attività di HIF1A finemente bilanciata regoli il dialogo tra oocita e cellule del cumulo, alla base del successo dello sviluppo successivo.
Implicazioni per l'allevamento animale e oltre
Questo lavoro mostra che stabilizzare delicatamente il sensore d'ossigeno dell'oocita durante la breve finestra della maturazione in vitro può aumentare e stabilizzare in modo significativo la resa di blastocisti nel bovino, senza modificare la fecondazione o le prime scissioni. In termini pratici, ciò potrebbe tradursi in una produzione di embrioni più affidabile per i programmi di allevamento, utilizzando un farmaco mirato piuttosto che modifiche grossolane ai livelli di ossigeno o sostanze più tossiche. Lo studio sottolinea anche una lezione più ampia, rilevante per i trattamenti di fertilità umana: imitare l'ambiente sfumato e povero di ossigeno dell'ovaio non significa semplicemente abbassare o aumentare l'ossigeno, ma rispettare l'equilibrio delicato di molecole di segnalazione come HIF1A. Mettere a punto con cura tale equilibrio, anziché spingerlo agli estremi, potrebbe essere una strada chiave per ottenere embrioni più sani.
Citazione: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Parole chiave: produzione di embrioni in vitro, maturazione degli oociti, segnalazione da ipossia, stabilizzazione di HIF1A, riproduzione bovina