Clear Sky Science · it
Verso i gemelli digitali per l’elettrofisiologia cardiaca con un risolutore open source efficiente e scalabile su cluster GPU
Perché costruire cuori virtuali è importante
Quando i medici trattano problemi del ritmo cardiaco, spesso operano in parte al buio: possono misurare segnali elettrici sulla superficie del corpo ma non vedono facilmente come questi segnali si propagano in profondità nel cuore. Questo studio descrive nuovi potenti strumenti informatici in grado di simulare nel dettaglio il battito di un cuore umano, con velocità sufficiente per esplorare molti scenari “e se”. Combinando anatomia cardiaca realistica con processori grafici all’avanguardia, gli autori ci avvicinano a esperimenti virtuali sicuri e a basso costo su copie digitali dei cuori di singoli pazienti.
Dai modelli semplici ai gemelli digitali
Le simulazioni cardiache moderne possono rappresentare l’attività dal livello delle singole cellule fino all’intero organo, ma riprodurre fedelmente come l’elettricità si muove nel cuore è sia matematicamente complesso sia computazionalmente costoso. Un obiettivo chiave per la medicina è il “gemello digitale cardiaco”: un modello informatico personalizzato che imiti il cuore di un paziente specifico e che possa essere usato per testare farmaci, dispositivi o strategie di stimolazione prima di provarli in clinica. Per rendere questo fattibile, il software che esegue queste simulazioni deve essere veloce e accurato, deve includere strutture anatomiche importanti e deve essere disponibile in modo aperto affinché ricercatori di tutto il mondo possano verificarlo, migliorarlo e riutilizzarlo.
Catturare il cablaggio nascosto del cuore
Il lavoro si concentra su un simulatore open source chiamato monoalg3d, che modella come i segnali elettrici viaggiano attraverso il muscolo cardiaco e la sua rete di cablaggio specializzata. Questa rete, nota come sistema di Purkinje, trasmette rapidamente il segnale che innesca il battito dalle vie di conduzione superiori a molti piccoli punti di connessione distribuiti sulla superficie interna dei ventricoli. In ciascuna di queste giunzioni, una sottile fibra di Purkinje deve eccitare una massa molto più grande di muscolo cardiaco, introducendo un ritardo naturale e, in alcune condizioni, il rischio di conduzione bloccata o anomala. Gli autori potenziano monoalg3d in modo da rappresentare questo cablaggio e le sue giunzioni in modo più realistico, inclusa l’asimmetria tra i segnali che viaggiano da Purkinje al muscolo e quelli che ritornano dal muscolo alla rete.
Trasformare supercomputer e GPU in laboratori cardiaci
Per eseguire modelli così dettagliati in tempi brevi, il team reingegnerizza l’uso dell’hardware nel simulatore. Ridisegnano il nucleo numerico in modo che sia la dinamica cellulare locale sia la propagazione del voltaggio attraverso il cuore vengano risolte direttamente sulle unità di elaborazione grafica (GPU), dispositivi originariamente creati per il rendering delle immagini ma oggi ampiamente impiegati per il calcolo scientifico. Organizzando con cura i dati per le librerie GPU ed evitando trasferimenti frequenti tra CPU e GPU, dimostrano che un’architettura completamente basata su GPU può accelerare un benchmark standard di quasi undici volte rispetto a una versione tradizionale solo CPU. Introducono inoltre un nuovo formato di output compatto per ridurre drasticamente le esigenze di archiviazione e una funzione di scambio di messaggi che può avviare centinaia di simulazioni in parallelo su un supercomputer, ciascuna esplorando un diverso insieme di parametri fisiologici.
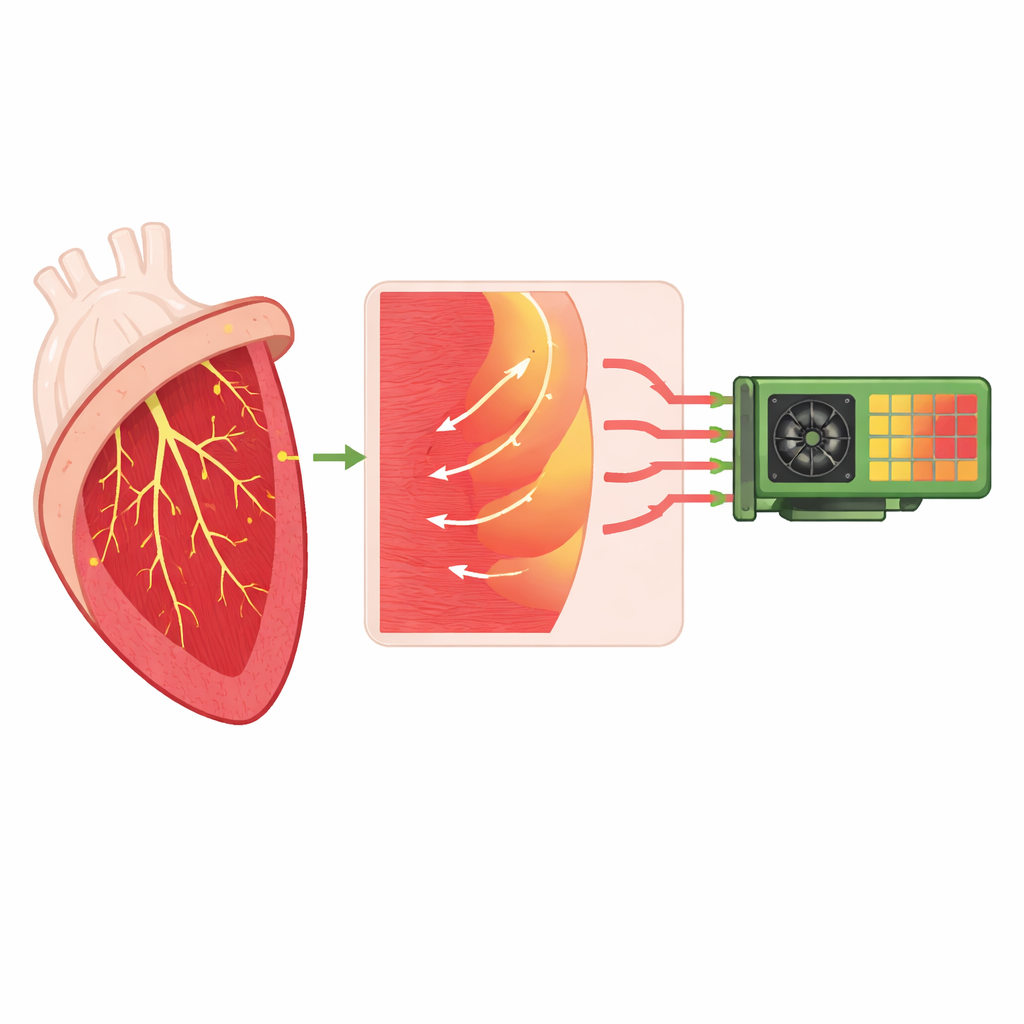
Insegnare ai cuori virtuali a corrispondere ai pazienti reali
Oltre alla semplice velocità, gli autori verificano se il loro risolutore migliorato può supportare simulazioni realistiche specifiche per paziente. Utilizzando una ricostruzione tridimensionale di un cuore umano ottenuta dall’imaging medico, collegano una rete di Purkinje sintetica e regolano parametri chiave delle giunzioni: la resistenza a ciascuna connessione e quante regioni muscolari vicine ciascun terminale di Purkinje eccita. Scandagliano automaticamente centinaia di combinazioni di questi valori, eseguendo simulazioni che partono da uno stimolo nel fascio di conduzione principale, e misurano sia i piccoli ritardi in ciascuna giunzione sia i segnali dell’elettrocardiogramma (ECG) sul torace. Per una mesh cardiaca ad alta risoluzione, individuano scelte di parametri che producono tempi di attivazione e forme d’onda ECG fisiologicamente plausibili e ben correlate con le registrazioni di un paziente reale, mantenendo i tempi delle singole simulazioni nell’ordine di poche ore anche quando 512 esecuzioni vengono lanciate contemporaneamente.
Molti cuori possibili che appaiono uguali dall’esterno
Un risultato interessante è che diverse configurazioni interne di cablaggio e diverse forze delle giunzioni possono condurre a ECG molto simili sulla superficie corporea. In altre parole, diversi cuori digitali distinti possono risultare ugualmente coerenti con gli stessi dati clinici. Gli autori mostrano che alcune giunzioni di Purkinje sono particolarmente influenti, con ritardi locali che variano sostanzialmente tra simulazioni diverse che tutte si adattano altrettanto bene, mentre il tempo di attivazione complessivo nei ventricoli rimane stabile. Questa non unicità suggerisce che i futuri framework per i gemelli digitali avranno bisogno di dati o vincoli aggiuntivi — come immagini più dettagliate o misurazioni invasive — per individuare una singola configurazione interna più probabile per un dato paziente.
Che cosa significa per le cure future
In sintesi, questo studio offre un simulatore libero e accelerato su GPU in grado di gestire anatomia cardiaca dettagliata, cablaggio di conduzione realistico e grandi lotti di simulazioni personalizzate su cluster di calcolo moderni. Per i non specialisti, il messaggio chiave è che sta diventando pratico eseguire esperimenti virtuali sul cuore veloci e ad alta fedeltà che somigliano a pazienti reali, inclusi i sottili ritardi nelle giunzioni del cablaggio interno del cuore. Pur richiedendo ulteriori lavori per personalizzare completamente questi modelli e risolvere le incertezze interne, gli strumenti presentati qui costituiscono un mattone importante per futuri sistemi di diagnosi, valutazione del rischio e pianificazione del trattamento basati sui gemelli digitali in cardiologia.
Citazione: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
Parole chiave: gemello digitale cardiaco, simulazione elettrofisiologia cardiaca, sistema di conduzione di Purkinje, calcolo su GPU, cardiologia personalizzata