Clear Sky Science · it
Visualizzazione in vivo della dinamica extracellulare dell’adenosina cardiaca e della sua modulazione farmacologica in modelli zebrafish di insufficienza cardiaca
Perché questa storia sul cuore dei pesci conta
L’insufficienza cardiaca resta una delle principali cause di morte a livello mondiale e molti pazienti peggiorano nonostante i migliori farmaci disponibili. I ricercatori sanno che le cellule cardiache sotto stress rilasciano nell’ambiente circostante «segnali di pericolo» chimici, ma è stato difficile osservare questi segnali in azione all’interno di un cuore che batte. Questo studio utilizza zebrafish trasparenti, i cui piccoli cuori riproducono fedelmente aspetti chiave dei cuori umani, per osservare in tempo reale quei segnali di allarme e testare un nuovo modo per attenuarli.
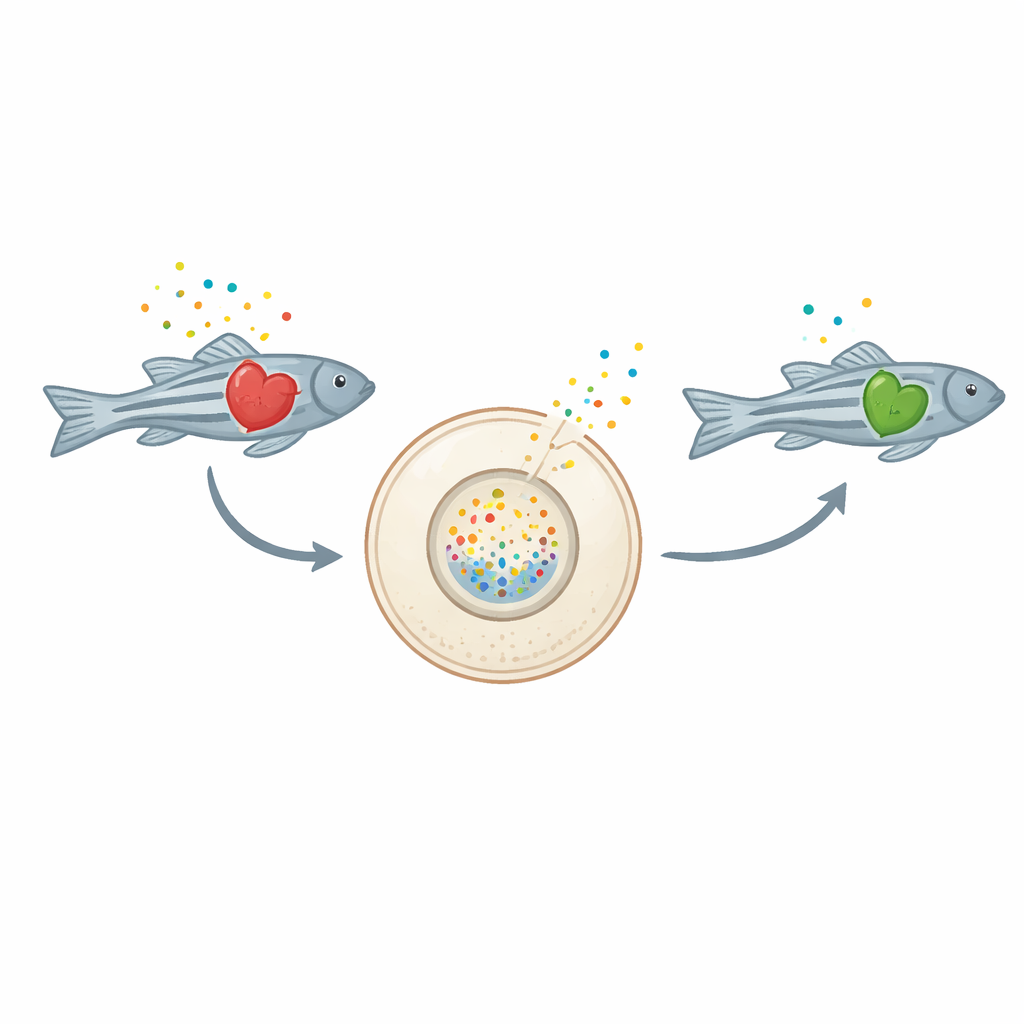
Segnali da un cuore in difficoltà
Quando le cellule cardiache sono danneggiate, rilasciano molecole trasportatrici di energia come l’ATP e il suo prodotto di degradazione, l’adenosina, nello spazio extracellulare. Fuori dalla cellula, queste stesse molecole smettono di agire come carburante e si comportano invece come messaggi urgenti che possono alimentare l’infiammazione. Nell’insufficienza cardiaca cronica, questa risposta infiammatoria può sovraattivarsi, danneggiando ulteriormente il cuore. Fino ad ora, però, mancavano prove dirette in vivo su come queste molecole si comportino nel tempo in un cuore in insufficienza.
Trasformare i zebrafish in fotocamere chimiche viventi
Il team ha ingegnerizzato zebrafish le cui cellule cardiache esprimono sulla superficie una proteina sensore fluorescente speciale chiamata GRABAdo. Quando l’adenosina si accumula fuori dalle cellule, questo sensore si illumina di un verde più intenso, trasformando di fatto ogni piccolo cuore in una propria fotocamera chimica live. I ricercatori hanno quindi indotto l’insufficienza cardiaca nei zebrafish usando la terfenadina, un farmaco noto per alterare il ritmo cardiaco e indebolirne la funzione di pompaggio. Man mano che i pesci sviluppavano chiari segni di insufficienza cardiaca — battito più lento, ventricoli dilatati e più deboli, accumulo di liquidi attorno al cuore e peggioramento delle capacità natatorie — i sensori cardiaci si accendevano, rivelando un marcato aumento dell’adenosina extracellulare. Misurazioni chimiche sull’intero larva confermarono che i livelli totali di adenosina erano più elevati nei cuori in insufficienza.
Bloccare la valvola di rilascio
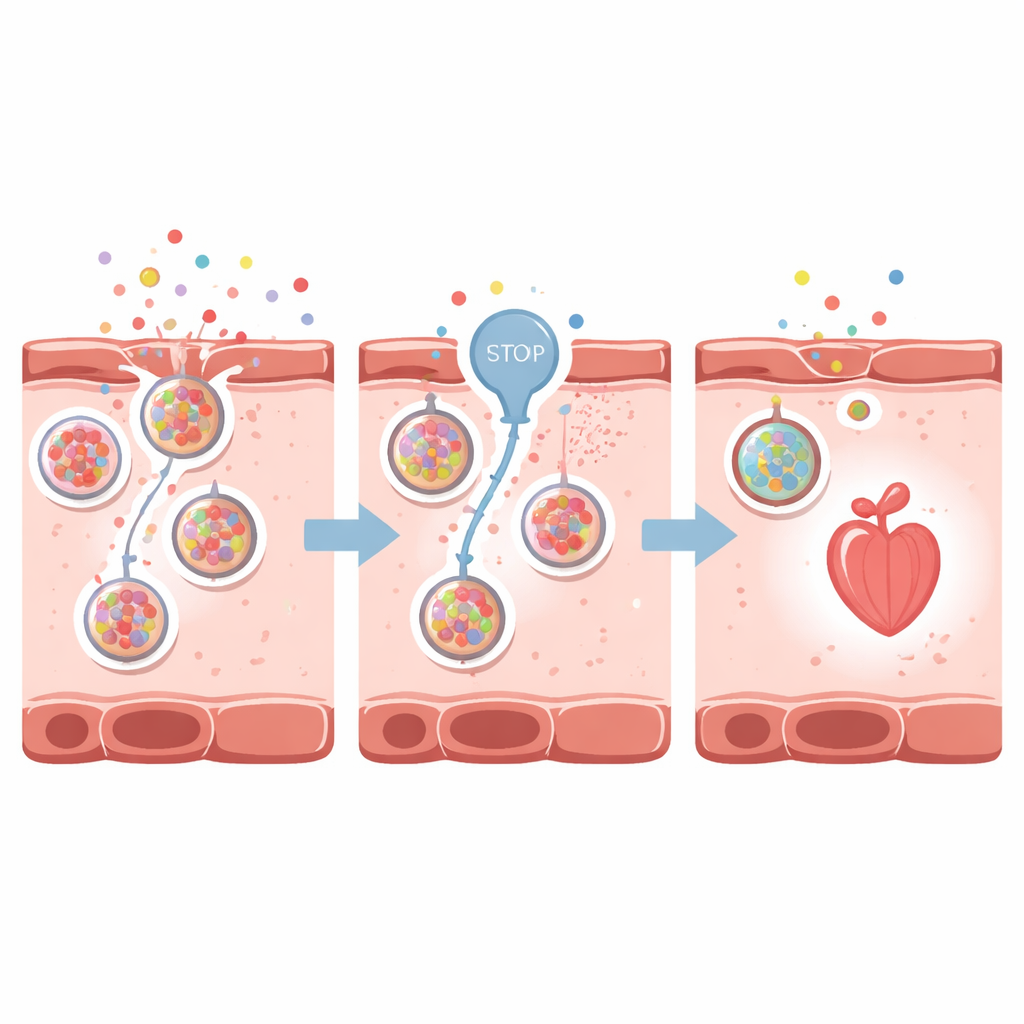
I ricercatori si sono poi chiesti se ridurre questi segnali di pericolo potesse proteggere il cuore. Si sono concentrati su VNUT, un trasportatore che carica l’ATP in piccoli pacchetti cellulari (vescicole) per il rilascio extracellulare. Utilizzando la clodronato, un farmaco che blocca VNUT, hanno ridotto il rilascio di ATP e, indirettamente, l’accumulo di adenosina intorno alle cellule cardiache. Nei zebrafish con insufficienza cardiaca indotta farmacologicamente, l’inibizione di VNUT ha preservato la morfologia cardiaca, ridotto la dilatazione delle camere, migliorato frequenza e forza di pompaggio e mantenuto un migliore flusso sanguigno. Il sensore fluorescente dell’adenosina si è attenuato, mostrando che era presente meno segnale di allarme nell’ambiente extracellulare. Effetti protettivi simili sono apparsi anche in zebrafish adulti con una forma acuta e rapidamente progressiva di insufficienza cardiaca.
Più leve protettive che agiscono insieme
L’insufficienza cardiaca coinvolge più percorsi, quindi i ricercatori hanno testato come il blocco di VNUT interagisse con altri attori noti. Farmaci che bloccano alcuni recettori dell’adenosina e recettori per l’ATP, così come un composto che limita la perdita passiva di ATP attraverso canali di membrana, hanno tutti aiutato i cuori dei zebrafish. Quando combinati con l’inibizione di VNUT, molti di questi trattamenti hanno prodotto benefici additivi, suggerendo che attenuare la segnalazione delle purine in più punti può essere particolarmente efficace. L’inibizione di VNUT ha inoltre contribuito a ripristinare l’equilibrio del calcio nelle cellule cardiache, essenziale per il battito normale, e ha ridotto sia la morte cellulare sia l’attività di geni associati all’infiammazione. Nel complesso, questi risultati ritraggono VNUT come un interruttore centrale che collega rilascio di ATP, infiammazione, alterato gestione del calcio e danno cardiaco progressivo.
Dai vaschetti ai futuri trattamenti
Per i non specialisti, il messaggio chiave è che lo studio visualizza direttamente un segnale chimico di stress in aumento nei cuori in insufficienza e mostra che bloccarne il rilascio può proteggere la funzione cardiaca in un animale vivente. Sebbene i cuori dei zebrafish siano più semplici rispetto a quelli umani, condividono sufficiente biologia da offrire un banco di prova potente per nuove idee. Individuando VNUT come un obiettivo promettente all’incrocio tra infiammazione e instabilità elettrica, questo lavoro suggerisce che le future terapie per l’insufficienza cardiaca potrebbero fare più che sostenere il flusso sanguigno: potrebbero calmare attivamente le conversazioni cellulari dannose che spingono il cuore verso il fallimento.
Citazione: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Parole chiave: insufficienza cardiaca, segnalazione dell’adenosina, modello zebrafish, infiammazione, protezione cardiaca