Clear Sky Science · it
Intermediari della G-quadrupla telomerica svelati da un’analisi complessa con reti di Markov
Nodi nascosti alle estremità del nostro DNA
Alle punte dei nostri cromosomi si trovano cappucci protettivi chiamati telomeri, spesso paragonati alle estremità in plastica dei lacci delle scarpe. In queste regioni, il DNA può annodarsi in modi insoliti formando nodi a quattro filamenti noti come G-quadruple. Queste piccole strutture possono influenzare il comportamento dei geni e determinare come le cellule invecchiano o diventano tumorali. Questo studio dà uno sguardo dietro le quinte di come uno di questi nodi si scioglie gradualmente, usando simulazioni al computer dettagliate e analisi dati avanzate per rivelare forme fugaci quasi impossibili da catturare sperimentalmente.
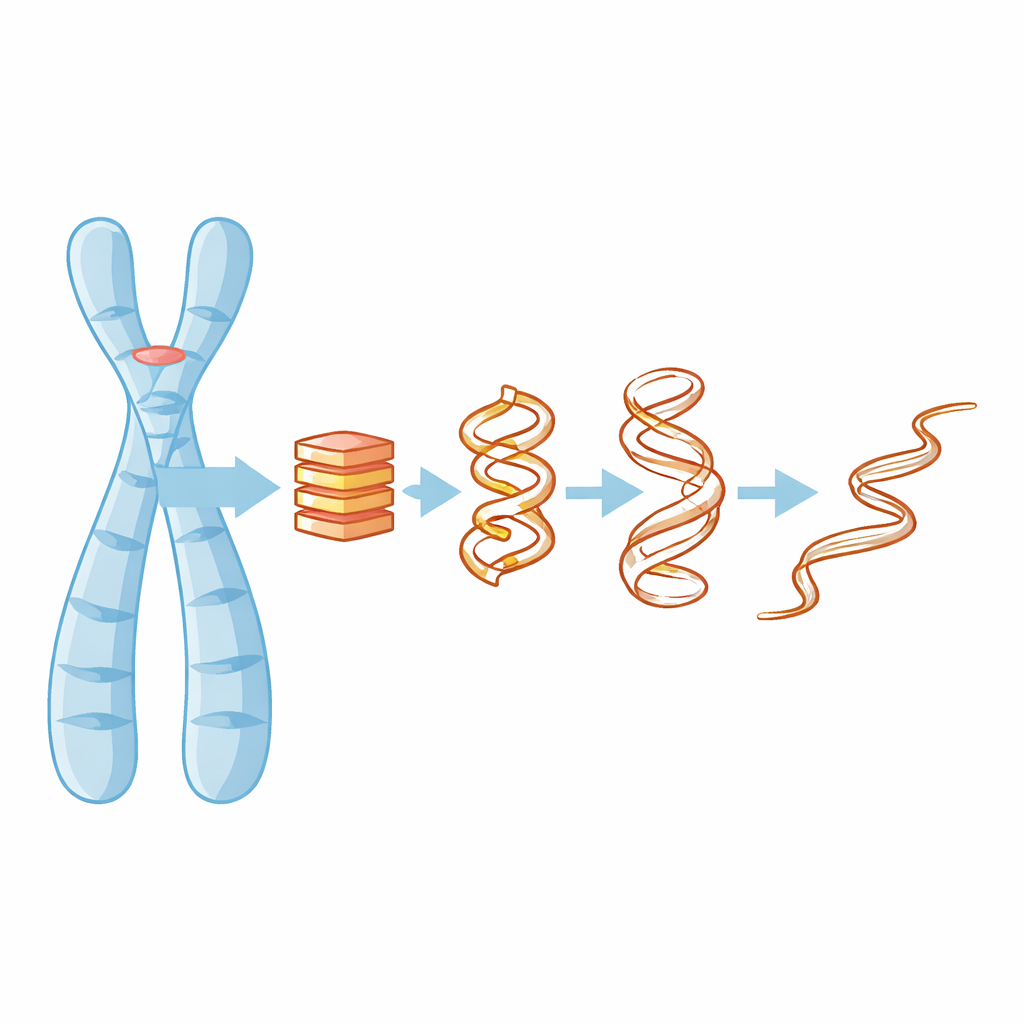
Perché contano i nodi a quattro filamenti del DNA
La maggior parte di noi impara che il DNA è una doppia elica, ma in tratti ricchi di guanine—come quelli dei telomeri—la molecola può ripiegarsi in pile compatte a quattro filamenti chiamate G-quadruple. Queste pile sono tenute insieme da strati planari di basi guaniniche e da piccoli ioni positivi, come il potassio, che si collocano al centro e contribuiscono a incollare il tutto. Quando una G-quadrupla si forma o si disfa, può bloccare o esporre parti del genoma, influenzando l’attività genica, la replicazione del DNA e persino il modo in cui le cellule tumorali mantengono i telomeri. Capire come queste strutture perdono la loro forma è quindi fondamentale per progettare farmaci che le prendano di mira o per prevedere quando potrebbero cedere.
Osservare lo scioglimento di un nodo molecolare
I ricercatori si sono concentrati su una G-quadrupla telomerica umana in cui quattro segmenti di un singolo filamento di DNA si allineano in parallelo e si impilano formando una colonna compatta. Hanno usato simulazioni di dinamica molecolare a livello atomico—esperimenti virtuali che tracciano il movimento di ogni atomo—riscaldando otto copie di questa struttura a temperature prossime al suo punto di fusione. Per aiutare il sistema a esplorare forme diverse, hanno impiegato una strategia chiamata replica exchange, in cui simulazioni a temperature diverse scambiano occasionalmente configurazioni. In sette degli otto casi la G-quadrupla è rimasta intatta; in uno si è completamente disgregata. Quel raro evento di disfazione è diventato un caso di studio dettagliato, mostrando non solo il prima e il dopo, ma un’intera sequenza di forme intermedie lungo il percorso.
Il ruolo cruciale dei piccoli ioni
Un risultato centrale è che i piccoli ioni all’interno della G-quadrupla funzionano come perni di tenuta. Finché almeno un ione rimane annidato tra gli strati di guanine, la struttura resta per lo più integra, forse leggermente allentata ma ancora riconoscibile. Quando entrambi gli ioni abbandonano il canale centrale, tuttavia, la pila si destabilizza rapidamente. Gli strati di guanine si deformano e i filamenti individuali si scollano, rendendo il DNA complessivo più esteso e flessibile. Altre molecole simulate che hanno perso solo un ione hanno raggiunto stati instabili ma ancora parzialmente ordinati, suggerendo che lo srotolamento completo richiede la perdita di entrambi gli ioni stabilizzanti—un indizio del perché alcune G-quadruple siano così ostinatamente robuste nella cellula.
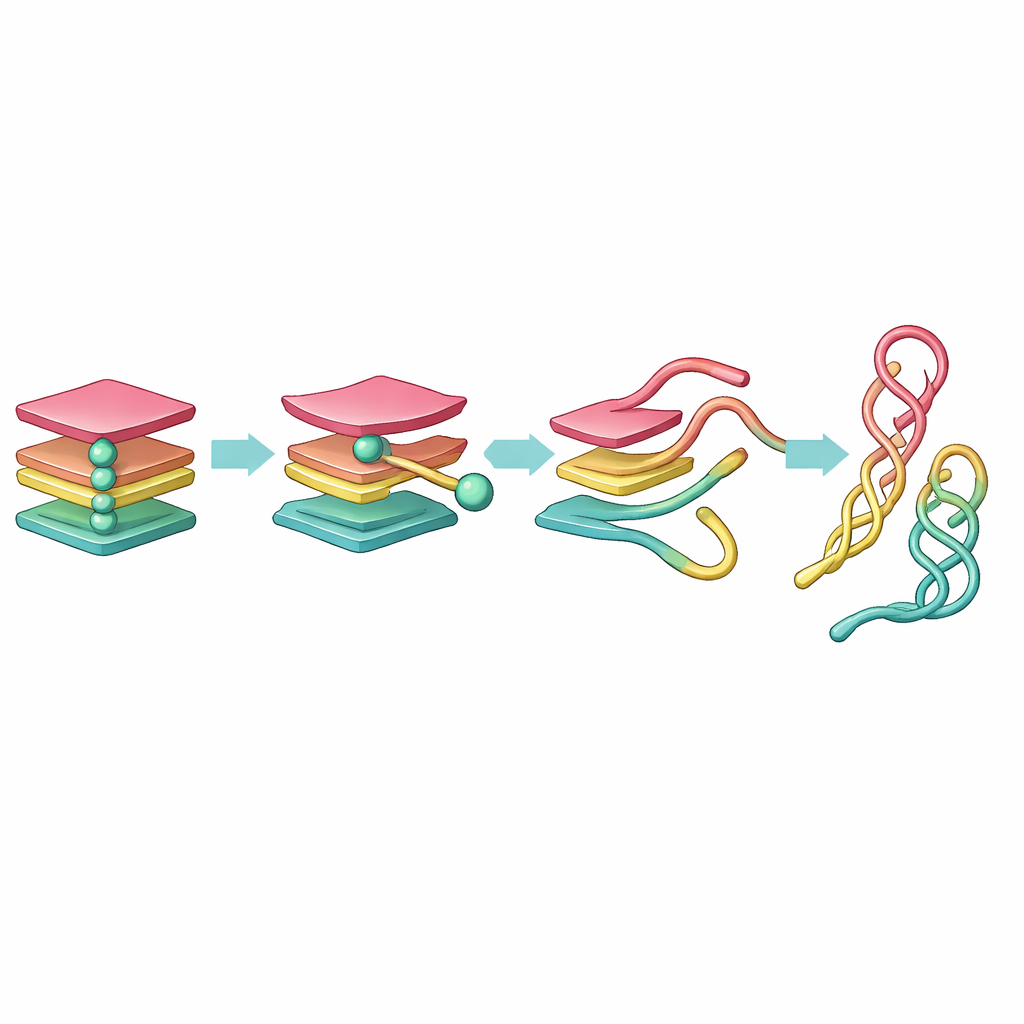
Scoprire tappe nascoste nel percorso
Le simulazioni grezze hanno prodotto una quantità enorme di dati, troppo complessi per essere interpretati a occhio. Per domarli, il team ha prima semplificato il DNA rappresentando ogni base come una singola perla, poi ha usato strumenti matematici per ridurre il movimento a poche coordinate chiave. Hanno applicato due metodi: l’Analisi delle Componenti Principali (PCA), che evidenzia le direzioni di maggiore movimento, e l’Analisi delle Componenti Tempo-Indipendenti (tICA), che filtra i cambiamenti lenti e duraturi che segnano veri spostamenti strutturali. Da queste coordinate ridotte hanno costruito le cosiddette reti conformazionali di Markov, in cui ogni nodo è una forma tipica del DNA e i collegamenti mostrano come la molecola salti da una forma all’altra.
Un percorso preferenziale dal nodo al filamento sciolto
Questa vista in rete ha rivelato un chiaro percorso di disgregazione. Partendo da una G-quadrupla completamente ripiegata, un filamento si stacca per primo, formando uno stato a tre filamenti detto "triplex". Quel triplex si riorganizza poi in un "hairpin" a due filamenti e in una serie di filamenti sciolti vicini. L’hairpin e un assetto correlato a "cross-hairpin" risultano sorprendentemente longevi, agendo come punti di sosta stabili nel passaggio da un nodo compatto a una configurazione del DNA più rilassata. Mentre la PCA suddivide questa progressione in molti stati dall’aspetto simile, la tICA la distilla in un piccolo insieme di passi distinti e cineticamente significativi, mostrando che le forme simili al triplex sono di breve durata, mentre quelle simili all’hairpin persistono molto più a lungo.
Implicazioni per biologia e medicina
Per un non specialista, il messaggio chiave è che le G-quadruple telomeriche non passano semplicemente dallo stato ripiegato a quello disfatto in modo brusco. Invece, si dissolvono attraverso una serie di forme a breve e a lunga durata, con i piccoli ioni che fungono da guardiani della stabilità. Le simulazioni suggeriscono che gli intermedi a tre filamenti sono fugaci, mentre gli hairpin a due filamenti e le forme a croce sono punti di sosta più stabili. Poiché questi stati intermedi possono apparire anche nel verso opposto, quello del ripiegamento, è probabile che siano cruciali nel modo in cui le G-quadruple si formano, cambiano e interagiscono con potenziali farmaci. Mappare questo paesaggio nascosto di forme avvicina gli scienziati alla progettazione di molecole in grado di stabilizzare o destabilizzare selettivamente questi nodi del DNA nella lotta contro il cancro e altre malattie.
Citazione: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Parole chiave: G-quadrupla, DNA telomerico, dinamica molecolare, ripiegamento del DNA senza proteine, terapie antitumorali