Clear Sky Science · it
Un set di dati trascrittomici a singola cellula che profila il trauma cranico e la terapia genica basata su NeuroD1 nei topi
Perché le lesioni cerebrali ci riguardano tutti
Ogni anno milioni di persone subiscono colpi alla testa dovuti a cadute, incidenti, sport o combattimenti. Questi traumi cranici possono lasciare problemi duraturi di memoria, movimento e umore, e i trattamenti attuali in gran parte gestiscono i sintomi più che riparare veramente il cervello. Questo studio esplora un promettente approccio genetico nei topi che mira non solo a limitare il danno, ma ad aiutare il cervello a ricostruirsi dall’interno, mappando questi cambiamenti cellula per cellula per creare una risorsa pubblica per terapie future.
Uno sguardo all’interno del cervello lesionato
Quando il cervello è ferito, non si limita a lividirsi come un muscolo. Si scatena una complessa reazione a catena: i neuroni muoiono, il flusso sanguigno viene disturbato e le cellule di supporto chiamate astrociti e le cellule immunitarie accorrono. Gli astrociti normalmente aiutano a nutrire i neuroni e a mantenere l’equilibrio della segnalazione cerebrale, ma dopo il trauma possono formare una cicatrice densa e alimentare un’infiammazione prolungata. Gli autori hanno impiegato una ferita controllata alla corteccia dei topi per imitare alcune forme di lesione penetrante del cervello, quindi hanno esaminato come ogni tipo cellulare principale nel tessuto colpito rispondeva nel tempo. Hanno applicato una tecnica chiamata sequenziamento dell’RNA a singola cellula, che legge quali geni sono attivi in decine di migliaia di singole cellule, permettendo un censimento dettagliato di come la comunità cellulare del cervello cambia dopo la lesione.
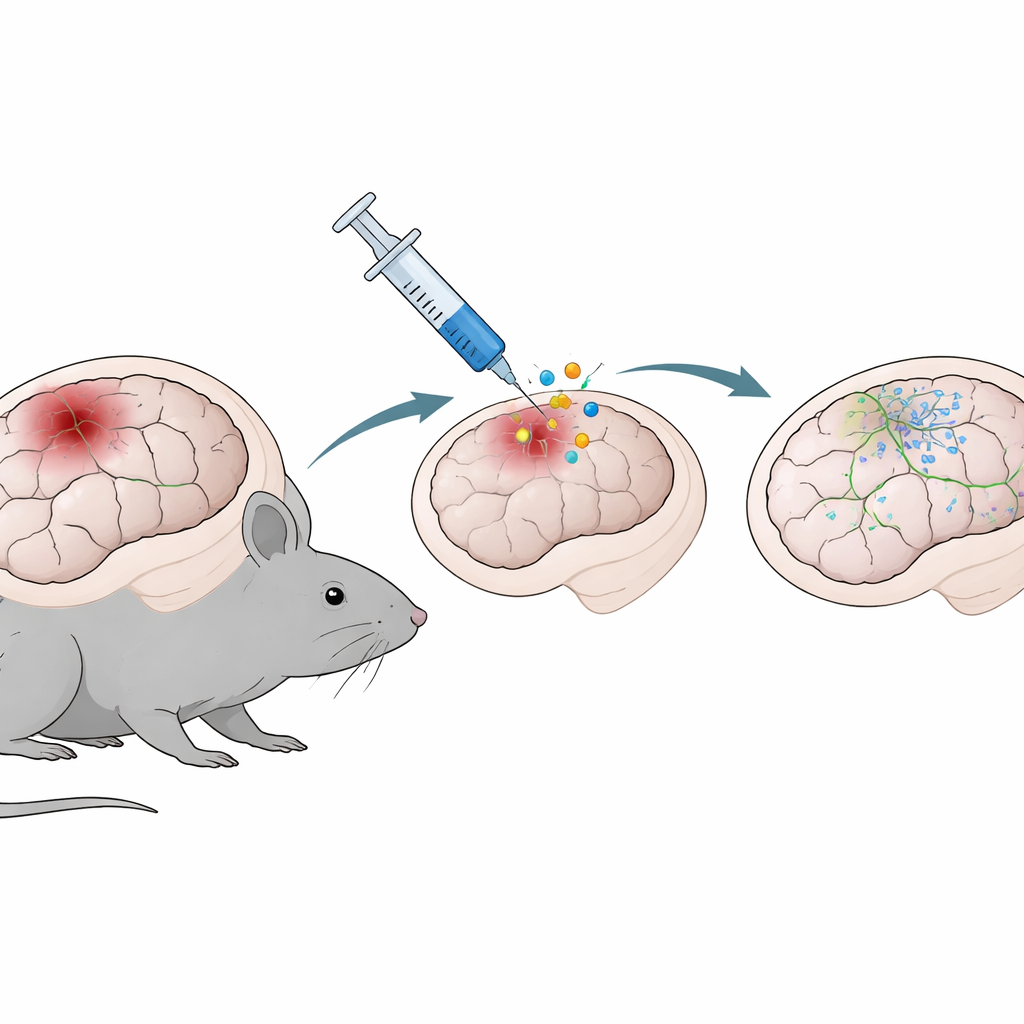
Una terapia genica che recluta le cellule di supporto del cervello
Poiché gli astrociti sono abbondanti e presenti proprio nel sito della lesione, rappresentano bersagli attraenti per strategie di riparazione. Il gruppo ha testato una terapia genica basata su NeuroD1, un gene noto per spingere le cellule verso uno stato simile ai neuroni. Utilizzando un vettore virale innocuo iniettato nell’area corticale danneggiata tre giorni dopo la lesione, hanno consegnato agli astrociti un marcatore neutro (GFP) o NeuroD1. Quando i cervelli sono stati esaminati una e due settimane dopo, i topi trattati con NeuroD1 mostravano cavità tissutali più piccole nei punti di danno e meno cellule immunitarie attivate chiamate microglia intorno alla lesione. In altre parole, la terapia non solo riduceva il danno strutturale visibile ma attenuava anche la risposta infiammatoria locale.
Tracciare i tipi cellulari uno per uno
Per capire cosa stava alla base di questi miglioramenti, i ricercatori hanno confrontato tre gruppi di campioni corticali: topi sani, topi lesionati trattati con il virus di controllo e topi lesionati trattati con il virus NeuroD1. Hanno sequenziato complessivamente più di 97.000 singole cellule e le hanno raggruppate in base ai loro schemi di attività genica in residenti cerebrali familiari, inclusi neuroni, astrociti, oligodendrociti (che isolano le fibre nervose), microglia e cellule che rivestono i vasi sanguigni e le cavità cerebrali. La sola lesione spostava questo equilibrio verso più astrociti e microglia e meno neuroni e cellule produttrici di mielina, riflettendo cicatrizzazione e infiammazione. Con il trattamento NeuroD1, questo sbilanciamento cominciava a invertire: le frazioni di neuroni, oligodendrociti e cellule epiteliali del plesso coroideo aumentavano, mentre astrociti e microglia diventavano meno dominanti nella zona lesionata.
Il lavoro nascosto dei sottotipi di astrociti
Gli astrociti si sono rivelati non essere una popolazione uniforme. Rianalizzandoli separatamente, il gruppo ha identificato sette sottocluster distinti di astrociti, ognuno con la propria firma genica e comportamento attraverso le tre condizioni. Alcuni sottocluster erano comuni nel tessuto sano ma quasi scomparivano dopo la lesione, mentre altri apparivano solo dopo il trauma. Nei cervelli lesionati trattati con il virus di controllo, diversi gruppi di astrociti attivavano programmi coinvolti nella costruzione e rimodellamento delle sinapsi — le giunzioni dove i neuroni comunicano — mentre riducevano l’espressione di geni legati alla produzione di energia nei mitocondri. Questo schema suggeriva che, dopo la lesione, gli astrociti favorivano cambiamenti di cablaggio anomali pur funzionando con una ridotta potenza metabolica.
Come NeuroD1 riequilibra energia cellulare e cablaggio
Il trattamento con NeuroD1 ha rimodellato questi sottocluster di astrociti in una direzione diversa. In diversi gruppi di astrociti associati alla lesione, i geni legati all’attività mitocondriale, alla respirazione cellulare e al metabolismo energetico generale sono stati nuovamente potenziati, mentre i geni collegati alla costruzione eccessiva di sinapsi e al rimodellamento della mielina sono stati attenuati. In altre parole, NeuroD1 sembrava ripristinare i motori energetici di queste cellule e temperare i tentativi incontrollati di ricollegamento che altrimenti potrebbero contribuire alla disfunzione. Alcuni sottotipi di astrociti che si erano espansi drasticamente dopo la lesione si sono ridotti in presenza di NeuroD1, mentre altri associati a funzioni più sane sono aumentati. Questi cambiamenti a livello fine forniscono indizi su quali stati di astrociti sono dannosi e quali potrebbero sostenere la riparazione.
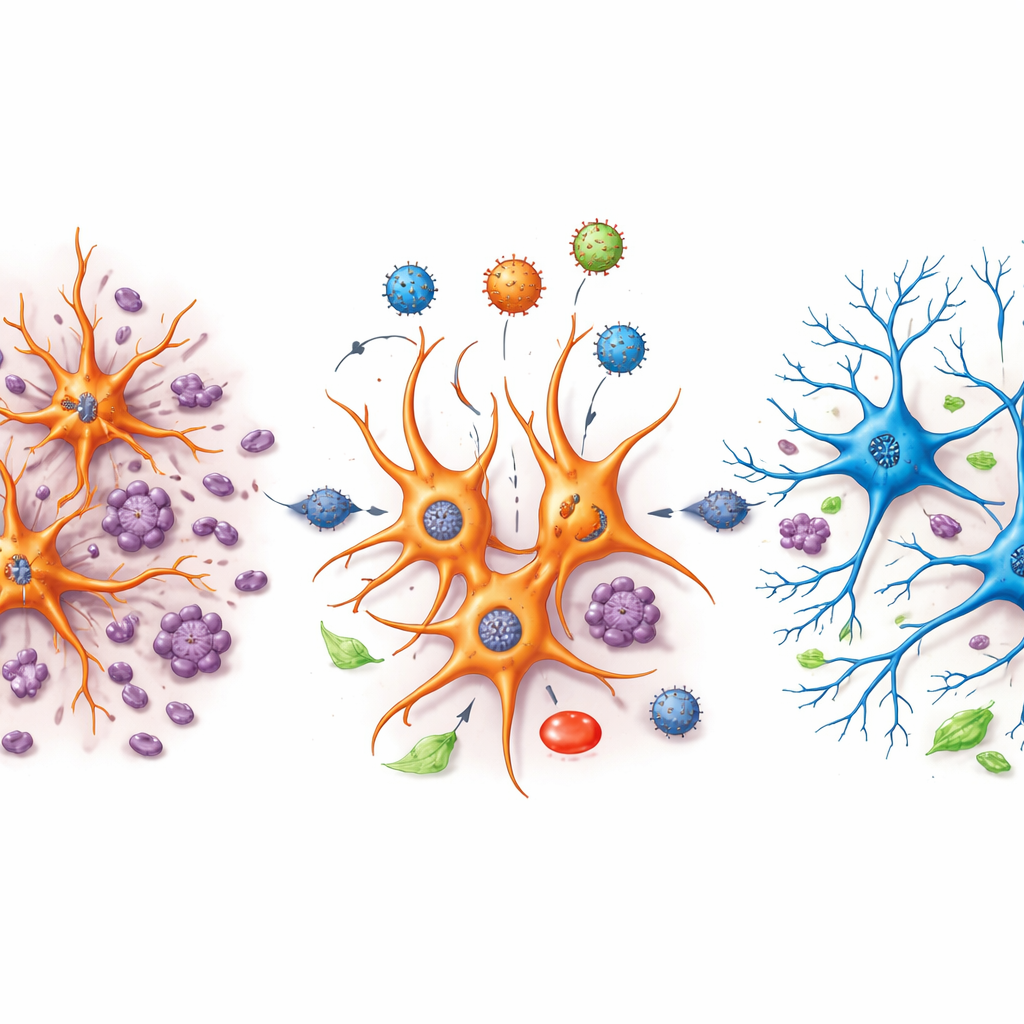
Che cosa significa questo per la riparazione cerebrale futura
Questo lavoro non offre ancora una cura pronta per il trauma cerebrale umano, ma fornisce due importanti avanzamenti. Primo, dimostra in un cervello mammifero vivo che una terapia genica mirata può ridurre la perdita di tessuto e l’infiammazione mentre spinge le popolazioni cellulari e l’uso di energia verso uno stato più sano. Secondo, rende disponibile un ricco dataset pubblico a singola cellula che altri scienziati possono esplorare per individuare specifici tipi cellulari, geni e vie che guidano il danno o il recupero dopo il trauma. Per i lettori fuori dal laboratorio, il messaggio chiave è che le cellule di supporto del cervello possono potenzialmente essere reclutate e riprogrammate per aiutare a ricostruire circuiti lesionati, avvicinandoci a trattamenti che ripristinano, piuttosto che semplicemente stabilizzare, la funzione cerebrale dopo un colpo traumatico.
Citazione: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Parole chiave: trauma cranico, terapia genica, astrociti, sequenziamento a singola cellula, NeuroD1