Clear Sky Science · it
Un set di dati annotato di colorazioni di Gram da emocolture positive
Perché le risposte rapide alle infezioni sono importanti
Quando batteri o funghi entrano nel flusso sanguigno, ogni ora senza il trattamento appropriato può fare la differenza tra la vita e la morte. I medici si affidano a un esame di laboratorio rapido chiamato colorazione di Gram per identificare il tipo di microrganismo presente e scegliere gli antibiotici iniziali. Ma leggere questi vetrini colorati al microscopio è un lavoro manuale e specializzato che richiede tempo e può variare da un tecnico all’altro. Questo studio descrive una nuova raccolta di immagini reali di vetrini di emocoltura, attentamente annotate, pensata per aiutare i computer a imparare a leggere automaticamente le colorazioni di Gram e supportare cure più rapide e affidabili.
Trasformare i vetrini ospedalieri reali in dati
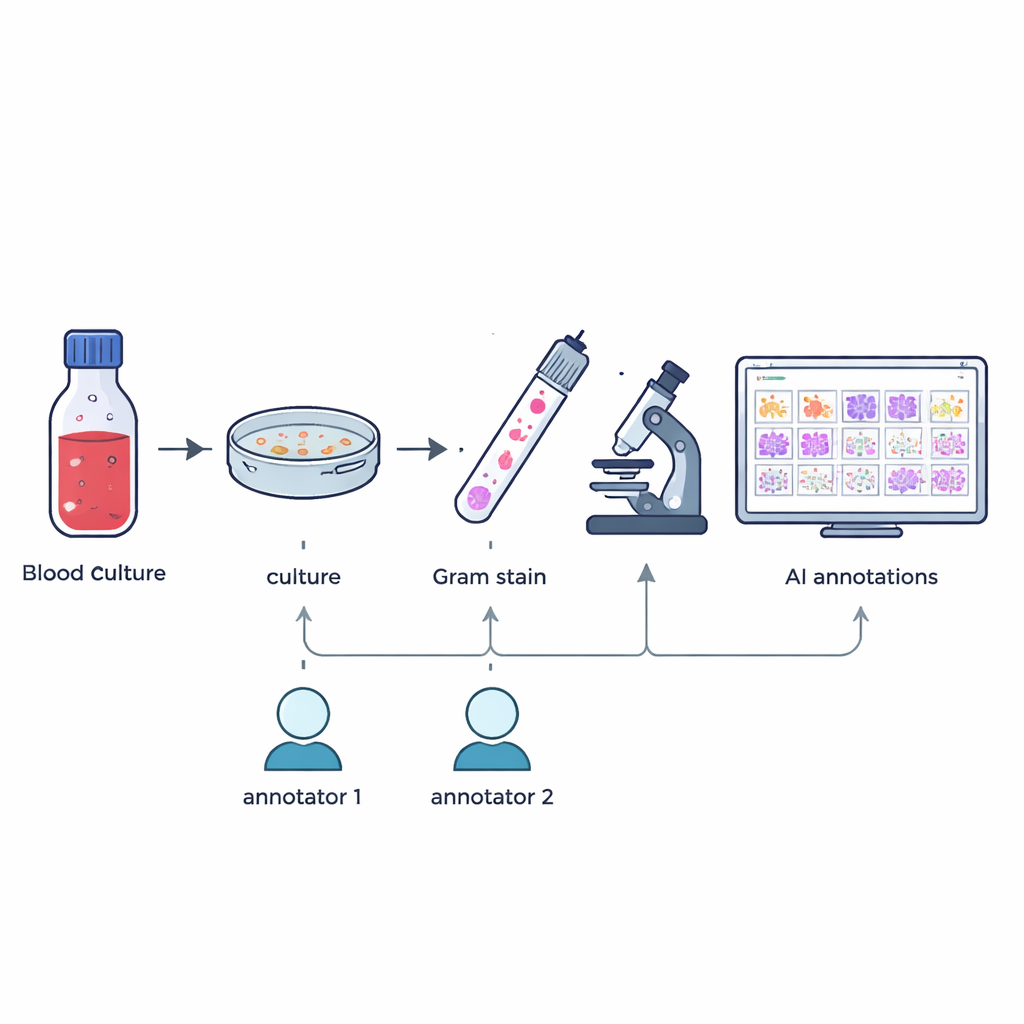
I ricercatori hanno raccolto 57 diversi tipi di batteri e funghi coltivati da flaconi di emocoltura positivi prelevati durante il lavoro ospedaliero quotidiano. Da gennaio a maggio 2024, ogni volta che un’emocoltura segnalava positività, il personale preparava degli strisci sulle vetrini colorati con la tecnica di Gram e confermava la specie esatta mediante un metodo di identificazione ad alta precisione chiamato spettrometria di massa MALDI-TOF. Senza modificare le routine normali o raccogliere campioni aggiuntivi, il team ha quindi acquisito immagini digitali ad alta risoluzione di campi rappresentativi al microscopio a immersione in olio 100×, ottenendo 505 immagini a colori di grande formato che rispecchiano ciò che i tecnici osservano nella pratica reale.
Annotazioni accurate di forme microscopiche
Costruire un set didattico utile per l’intelligenza artificiale richiede di sapere esattamente dove si trova ogni microbo in ciascuna immagine. Due tecnici di microbiologia esperti hanno tracciato in modo indipendente delle scatole attorno a cellule microbiche individuali o a gruppi in ogni immagine, guidati solo da ciò che vedevano al microscopio. Un software personalizzato ha confrontato i due insiemi di marcature: le scatole che si sovrapponevano sufficientemente sono state unite e eventuali incongruenze o disaccordi sono stati segnalati. Un esperto senior con oltre 20 anni di esperienza ha poi riesaminato questi casi manualmente. Questo processo in più fasi ha prodotto 7.528 annotazioni verificate che evidenziano cocchi (cellule tonde), bacilli (cellule a forma di bastoncello) e funghi, escludendo oggetti parziali o dubbi.
Contenuto del set di dati
La risorsa finale combina diversi livelli di informazione. Tutte le 505 immagini sono fornite come file JPEG ad alta risoluzione e le scatole finali verificate dagli esperti sono memorizzate nel formato JSON COCO standard, ampiamente usato nella ricerca in visione artificiale. File aggiuntivi collegano ogni immagine alla specie microbica, al fatto che sia Gram-positiva o Gram-negativa, al gruppo morfologico ampio, al tipo di flacone di emocoltura di provenienza e al tempo impiegato perché la coltura risultasse positiva. Poiché ogni immagine contiene una sola specie, tutte le scatole all’interno della stessa immagine condividono gli stessi tratti biologici. Gli utenti possono scegliere tra un unico file di annotazioni grande o file separati per immagine, e viene incluso un semplice script Python per visualizzare qualsiasi immagine con le rispettive scatole sovrapposte.
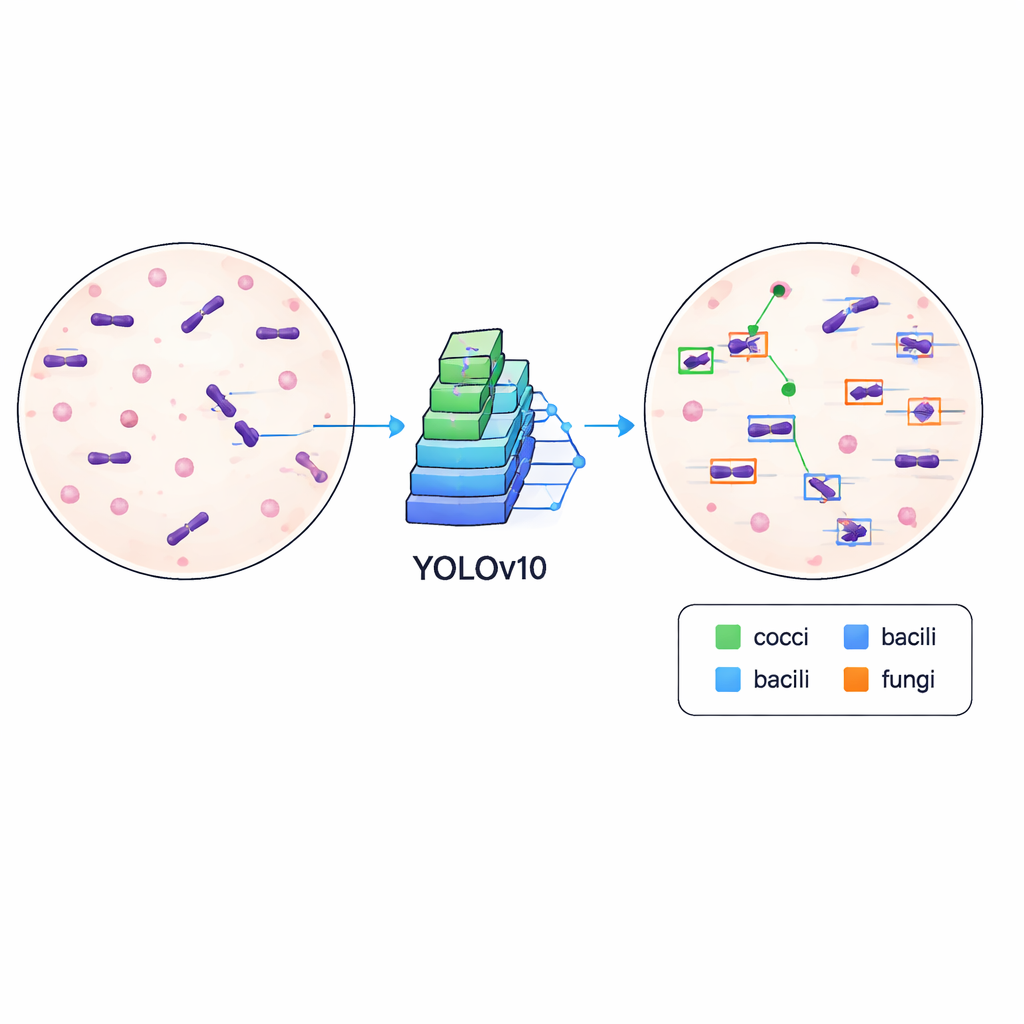
Insegnare ai computer a riconoscere i germi
Per dimostrare che il set di dati è non solo ordinato ma anche pratico, gli autori hanno addestrato un moderno algoritmo di rilevamento oggetti noto come YOLOv10 per trovare e classificare i microbi nelle immagini. Hanno suddiviso i dati in set di addestramento e di validazione e hanno eseguito il modello per 500 epoche di addestramento su una scheda grafica di fascia alta, monitorando quanto riuscisse a tracciare scatole accurate e a distinguere tra i diversi tipi cellulari. Il sistema addestrato ha raggiunto una precisione media (mean average precision) di circa il 84,6% a una soglia di corrispondenza standard, indicando che può localizzare e etichettare i microbi in modo affidabile attraverso variazioni nell’aspetto dei vetrini, inclusi differenze nell’intensità della colorazione, detriti di fondo e messa a fuoco.
Come può essere usata questa risorsa
Poiché i dati seguono formati comuni, possono integrarsi in molte pipeline di visione artificiale esistenti. I ricercatori potrebbero prima addestrare un sistema a distinguere i veri microbi dai detriti, aiutando i laboratori a filtrare segnali di coltura falsi positivi. Possono anche raggruppare i microbi in forme ampie, corrispondenti a quanto serve ai clinici per un primo referto di tipo "Tier 1" che guida le scelte antibiotiche iniziali. Un obiettivo più ambizioso è distinguere specie individuali tramite sottili segnali visivi. Gli autori rilevano dei limiti: alcune cellule sono raggruppate, alcune immagini provengono da una sola fonte per specie e la messa a fuoco può variare—proprio come nella realtà. Tuttavia, ogni scatola inclusa è stata accuratamente verificata, rendendo il set di dati un punto di partenza affidabile.
Cosa significa questo per i pazienti
In termini semplici, questo lavoro trasforma i vetrini di emocoltura di routine in un terreno comune di addestramento per software intelligenti. Rendendo pubbliche sia le immagini sia le marcature degli esperti, lo studio abbassa la barriera per gruppi di tutto il mondo che vogliano costruire e testare strumenti di IA in grado di leggere rapidamente e in modo coerente le colorazioni di Gram. Pur non sostituendo i microbiologi umani, tali sistemi potrebbero aiutare a segnalare più presto infezioni pericolose, ridurre errori di interpretazione e supportare un uso più appropriato degli antibiotici. Per i pazienti, ciò potrebbe tradursi in trattamenti più rapidi e più precisi quando è più importante.
Citazione: Yi, Q., Gou, X., Zhu, R. et al. An annotated dataset of Gram stains from positive blood cultures. Sci Data 13, 294 (2026). https://doi.org/10.1038/s41597-026-06651-3
Parole chiave: infezioni ematiche, colorazione di Gram, set di dati di imaging medico, intelligenza artificiale, diagnostica microbiologica