Clear Sky Science · it
Dati di espressione genica multiomici temporali durante la differenziazione di cellule polormonali derivate da cellule staminali embrionali umane
Come le cellule imparano a diventare organi
I nostri corpi iniziano come piccole masse di cellule identiche che in qualche modo apprendono a trasformarsi in tessuti molto diversi, dal cervello al pancreas. Questo studio segue in laboratorio quel processo di apprendimento, usando cellule staminali embrionali umane guidate a diventare cellule pancreatiche precoci. Seguendo l’attività di migliaia di geni nel tempo e su più livelli, il lavoro crea una mappa di riferimento ricca che può aiutare gli scienziati a comprendere meglio lo sviluppo umano e, a lungo termine, migliorare strategie per trattare malattie come il diabete.
Osservare le cellule mentre scelgono un percorso
Le cellule staminali embrionali umane sono particolari perché possono trasformarsi in quasi qualsiasi tipo di cellula del corpo. In questo studio i ricercatori hanno indirizzato queste cellule verso un destino specifico: una linea pancreatica chiamata cellule polormonali, capaci di produrre ormoni chiave come insulina e glucagone. Hanno riprodotto lo sviluppo precoce in coltura variando progressivamente il mezzo di crescita, trasferendo le cellule prima in uno stato primitivo simile all’intestino chiamato endoderma, e poi verso cellule pancreatiche produttrici di ormoni nell’arco di 17 giorni. I campioni sono stati raccolti in dieci punti temporali scelti con cura per catturare l’intero passaggio dalla cellula staminale flessibile alla cellula specializzata produttrice di ormoni. 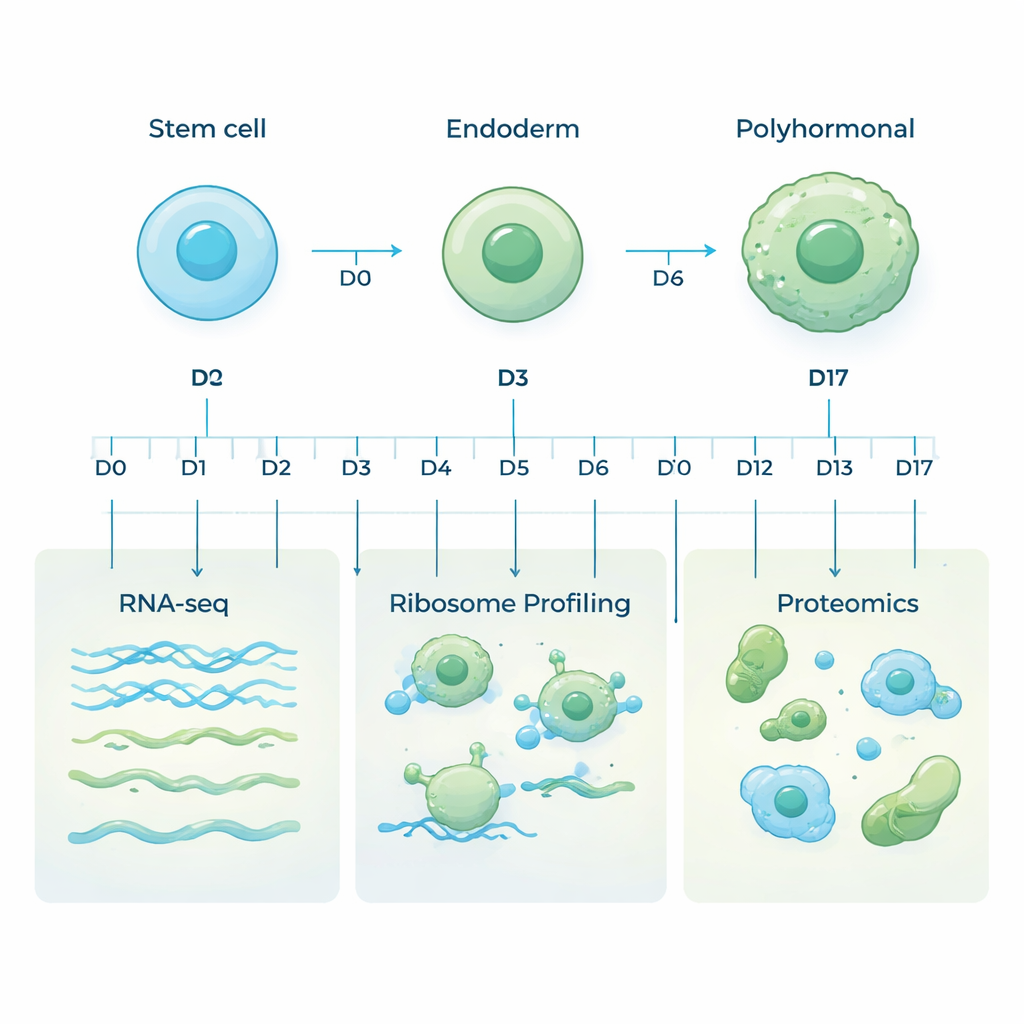
Guardare sotto il cofano a tre livelli
La maggior parte degli studi si concentra solo sull’RNA messaggero (mRNA), le molecole che trasportano le istruzioni dei geni. Ma l’mRNA è solo parte della storia: non tutti i messaggi vengono tradotti in proteine, e le proteine stesse possono essere sintetizzate o degradate a velocità diverse. Per avere una visione più completa, il team ha impiegato tre approcci complementari sugli stessi campioni. Il sequenziamento dell’RNA ha misurato quali geni venivano trascritti in mRNA. Il profiling dei ribosomi ha monitorato quali messaggi venivano attivamente letti dalle macchine cellulari di sintesi proteica. La proteomica basata su spettrometria di massa ha quindi misurato le proteine effettivamente presenti. Insieme, questi strati rivelano come l’attività genica venga regolata mentre le cellule cambiano identità.
Seguire segnali chiave dell’identità cellulare
Per verificare che le cellule avessero effettivamente seguito il percorso di sviluppo previsto, gli scienziati hanno monitorato noti geni marker. All’inizio, marcatori classici di cellule staminali come OCT4 e NANOG erano elevati e poi si sono attenuati con il progredire della differenziazione. Quando le cellule entrarono nello stadio di endoderma, marker come KIT e SOX17 aumentarono. Nelle fasi finali, i marker polormonali insulina (INS) e glucagone (GCG) comparvero in modo marcato sia a livello di RNA sia di proteina, confermando che le cellule avevano assunto un’identità simile a quella di cellule pancreatiche produttrici di ormoni. Sebbene una delle repliche biologiche abbia attraversato queste fasi leggermente più lentamente dell’altra, entrambe seguirono lo stesso percorso generale, riflettendo piccole differenze naturali piuttosto che problemi tecnici. 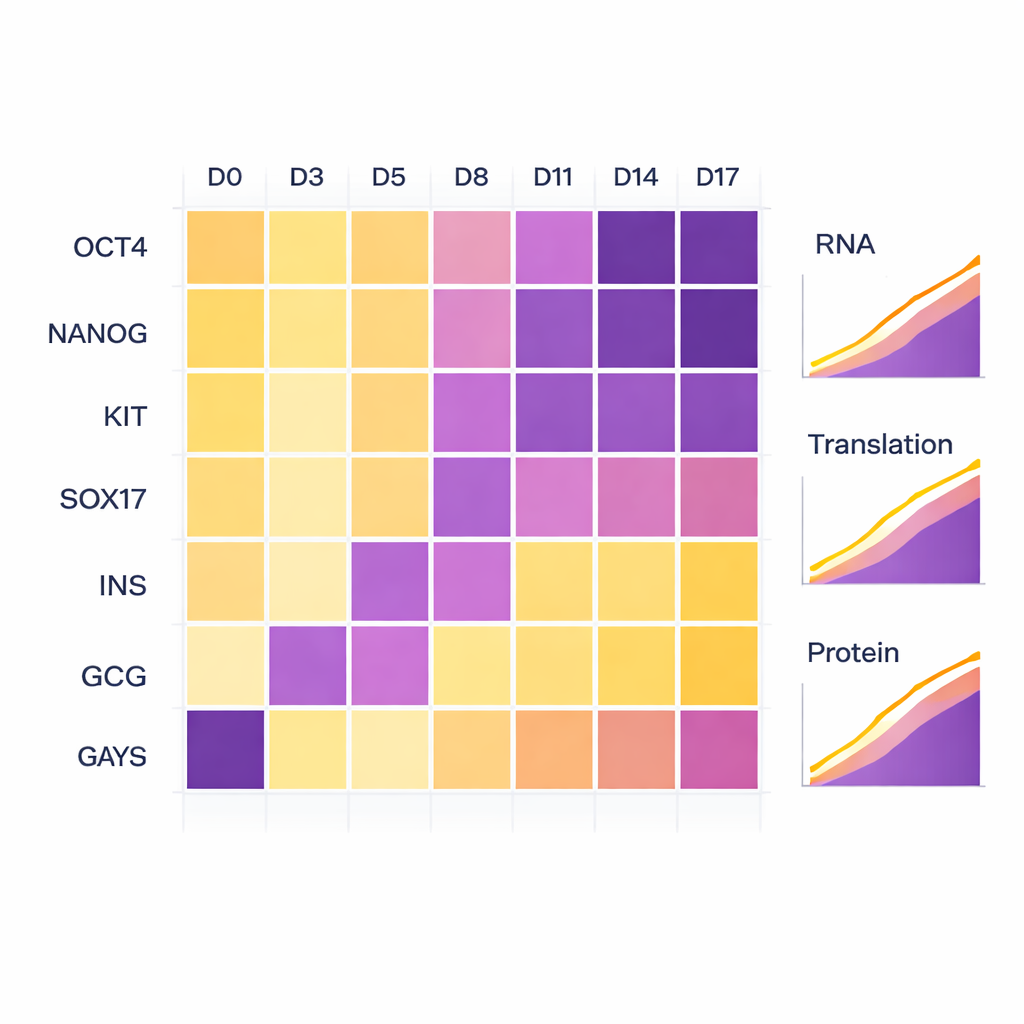
Controlli di qualità per una risorsa affidabile
Dato che questo lavoro è pensato per servire come risorsa per la comunità, gli autori hanno dedicato ampi sforzi a verificare la qualità e la coerenza dei dati. Per ciascuno dei tre metodi hanno valutato l’accuratezza delle sequenze e delle misurazioni, la copertura dei geni e quanto concordassero esperimenti ripetuti. Gli stadi di cellula staminale e polormonale mostrarono differenze chiare e riproducibili a livello di RNA, traduzione e proteine. Le analisi delle componenti principali—mappe statistiche che raggruppano campioni simili—mostrarono che i punti temporali si disponevano in ordine, con stadi precoci e tardivi chiaramente separati e le repliche biologiche che si raggruppavano strettamente. I dati di proteomica da soli hanno seguito in modo affidabile quasi 7.500 proteine attraverso tutti i punti temporali, con relativamente poche misurazioni mancanti, sottolineando la profondità del dataset.
Una base per scoperte future
Gli autori rendono disponibili tutti i dati grezzi e processati, insieme agli script di analisi e ai file di riferimento, in modo che altri ricercatori possano riutilizzare e rianalizzare il dataset. Oltre a descrivere come un tipo cellulare diventi un altro, questo lavoro offre un quadro dettagliato e risolto nel tempo di come i messaggi genici, la loro traduzione e le proteine risultanti interagiscano durante una transizione di sviluppo importante. Per i non specialisti, il punto chiave è che il destino cellulare è controllato da più livelli di regolazione che operano insieme nel tempo, e che questo dataset fornisce un “film” ad alta risoluzione di quei cambiamenti. I ricercatori possono ora usare questa risorsa per indagare perché alcuni geni cambiano presto e altri tardi, come organi diversi possano seguire regole simili o distinte, e come guidare meglio le cellule staminali verso destini utili in ambito medico.
Citazione: Keskin, A., Shayya, H.J., Patel, A. et al. Temporal multiomics gene expression data across human embryonic stem cell-derived polyhormonal cell differentiation. Sci Data 13, 278 (2026). https://doi.org/10.1038/s41597-026-06606-8
Parole chiave: cellule staminali, sviluppo del pancreas, espressione genica, multiomica, cellule polormonali