Clear Sky Science · it
Un dataset TC con misurazioni RECIST e maschere di segmentazione complete per tumori e linfonodi
Perché questa risorsa di imaging oncologico è importante
La cura del cancro dipende sempre più dalle immagini mediche per valutare se i trattamenti stanno funzionando. Tuttavia, le misurazioni accurate effettuate dai medici fetta per fetta sulle TC richiedono tempo e possono variare tra esperti diversi. Questo articolo presenta una nuova collezione di TC di pazienti oncologici, resa pubblica, con tumori e linfonodi meticolosamente delineati e misurati secondo un regolamento clinico largamente utilizzato. È pensata per aiutare i ricercatori a sviluppare e testare programmi informatici che un giorno potrebbero assumere gran parte di questo lavoro ripetitivo e rendere il monitoraggio del trattamento del cancro più rapido e coerente a livello mondiale.
Come i medici attualmente monitorano i tumori
Per giudicare se una terapia oncologica è efficace, i radiologi seguono spesso uno standard chiamato RECIST 1.1. In pratica, ciò significa scegliere una manciata di lesioni «target» nelle TC del paziente e registrare il diametro massimo visibile di ciascuna in millimetri. Nel tempo, confrontano la somma di questi diametri con esami precedenti per decidere se la malattia è regredita, rimasta stabile o progredita. Pur avendo portato ordine negli studi clinici, questo approccio presenta svantaggi: dipende molto dalla selezione delle lesioni, si basa su misure unidimensionali invece che sulla reale dimensione 3‑D e richiede tipicamente più di 10 minuti per paziente per valutazione. Con l’aumento dei casi di cancro nel mondo, questi limiti esercitano una pressione reale sui servizi di radiologia.
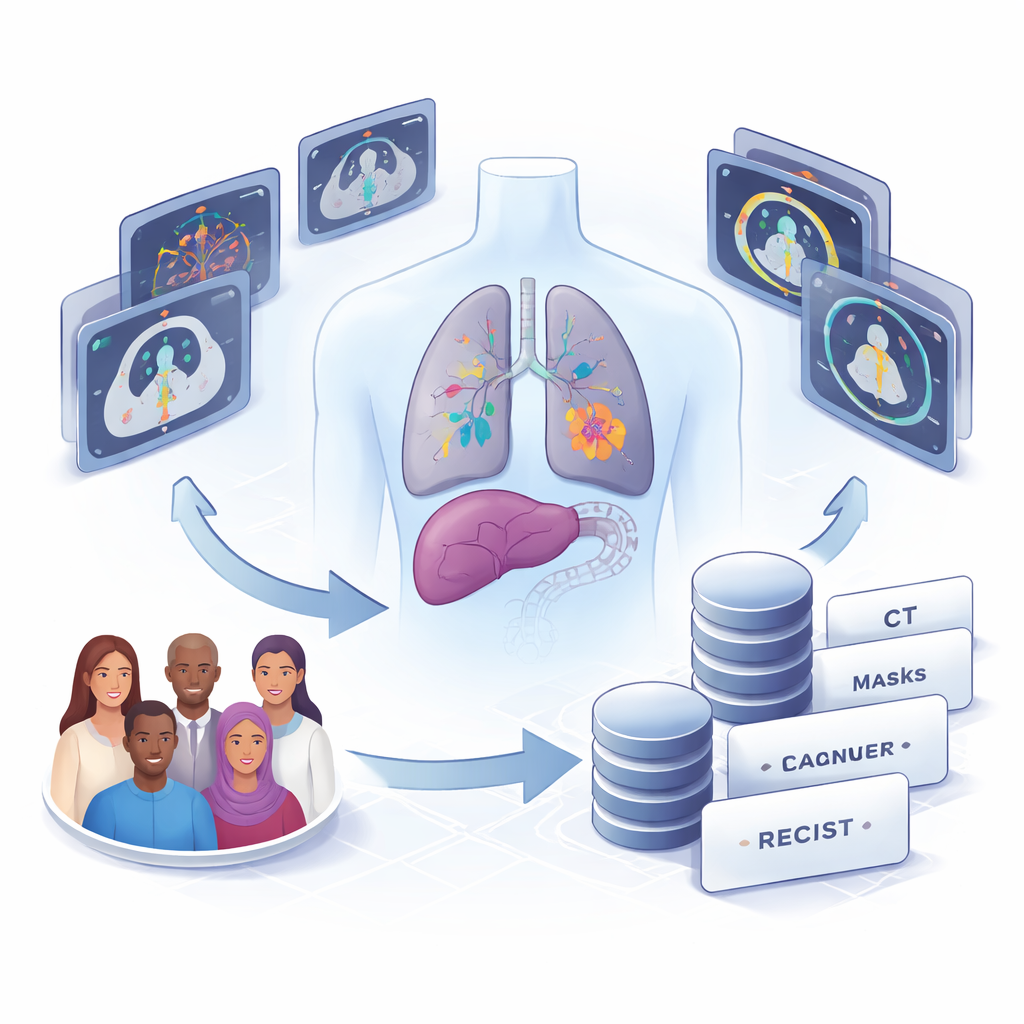
Cosa contiene il nuovo dataset TC
Gli autori hanno raccolto TC di 22 adulti trattati per vari tipi di cancro presso l’Hospital Clínico dell’Università del Cile, inclusi tumori del polmone, del fegato, del colon-retto, della mammella, dell’ovaio, dello stomaco, della colecisti, della vescica e melanoma. Da 58 serie di esami toracici e addominali eseguite tra il 2017 e il 2023, hanno identificato ogni tumore solido o linfonodo ingrossato sufficientemente grande da essere misurato. In totale, hanno delineato manualmente 1.246 lesioni individuali: 1.148 metastasi (tumori che si sono diffusi), 93 linfonodi ingrossati e 5 tumori primari. Per 82 di queste lesioni hanno inoltre incluso le misurazioni RECIST ufficiali riportate nelle cartelle cliniche, permettendo un confronto diretto tra la pratica routinaria e i metodi automatizzati.
Come hanno collaborato esperti e IA
Produrre delineamenti così dettagliati sarebbe normalmente troppo lento, quindi il team ha adottato una strategia «human‑in‑the‑loop». Radiologi esperti e specializzandi hanno tracciato scatole 3‑D approssimative attorno ai sospetti tumori, e un potente modello di segmentazione chiamato MedSAM ha proposto confini iniziali. I residenti hanno quindi corretto questi contorni, e i radiologi senior hanno effettuato una revisione finale. Dopo ogni lotto di esami completato, il modello IA è stato riaddestrato sui delineamenti migliorati e usato per assistere il lotto successivo. A ogni ciclo, le sue prestazioni si sono avvicinate a quelle accettate dagli esperti umani, riducendo lo sforzo necessario per ulteriori correzioni pur mantenendo l’accuratezza.
Cosa rivelano i dati sui tumori
Poiché ogni lesione nelle scansioni è stata delineata in tre dimensioni, gli autori hanno potuto studiarne dimensioni e densità in dettaglio. La maggior parte dei tumori si trovava nei polmoni e nel fegato. I tumori polmonari tendevano ad avere piccoli volumi ma spesso diametri relativamente lunghi, mentre i linfonodi mostravano volumi maggiori ma diametri principali più corti rispetto ai tumori epatici. Il team ha anche esaminato quanto queste regioni apparissero chiare o scure nelle TC, una proprietà legata alla densità tissutale. I tumori polmonari, circondati dall’aria, hanno mostrato pattern di intensità molto diversi rispetto ai tumori epatici e ai linfonodi, suggerendo che semplici caratteristiche numeriche estratte dalle immagini TC potrebbero aiutare a distinguere i tipi di lesione. Importante, lo studio ha confermato una forte relazione tra il diametro massimo di una lesione e il suo vero volume 3‑D, sostenendo l’idea che regole basate sul diametro come RECIST possano costituire un sostituto pratico alle misurazioni volumetriche complete quando applicate con attenzione.
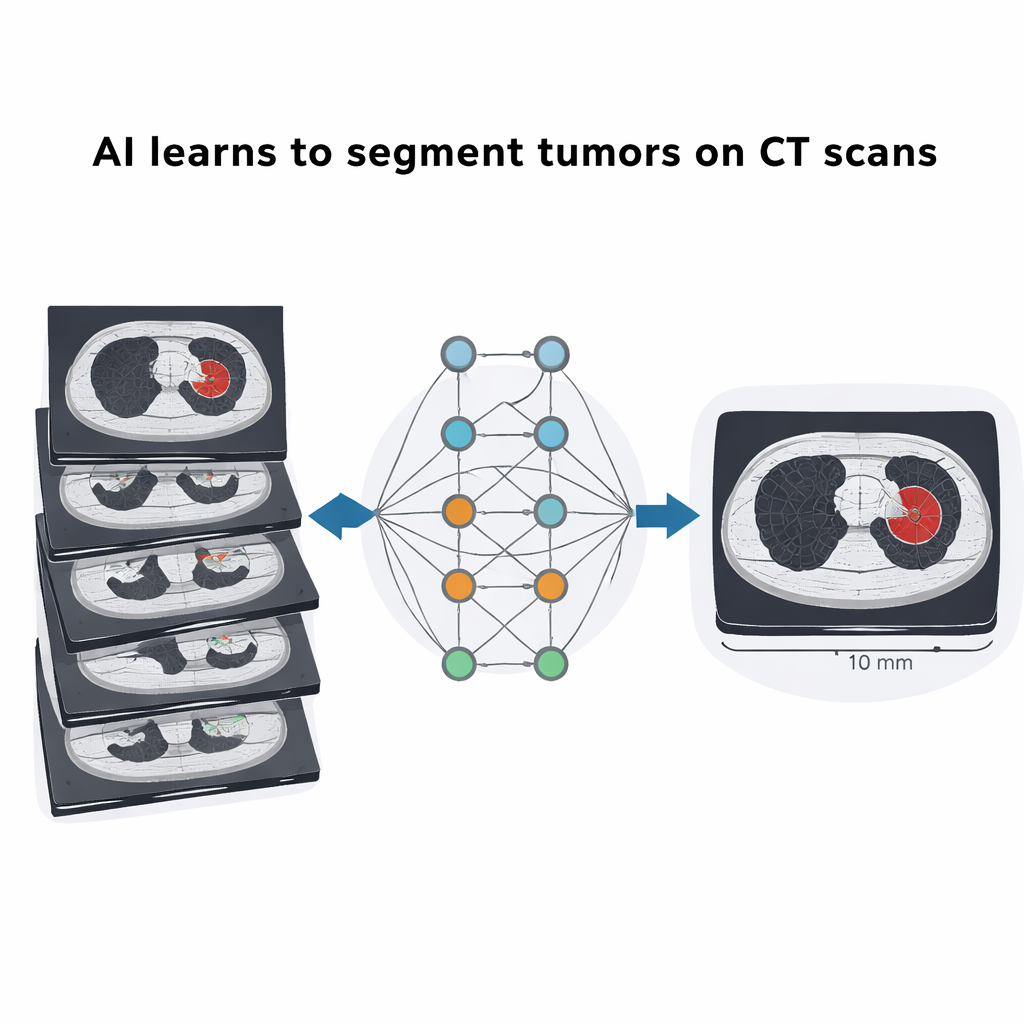
Mettere il dataset alla prova con il deep learning
Per dimostrare l’utilizzo del dataset, i ricercatori hanno addestrato e perfezionato due tipi di sistemi di deep learning. Innanzitutto hanno ottimizzato MedSAM per segmentare automaticamente i tumori a partire da semplici box di delimitazione, ottenendo punteggi di sovrapposizione con i delineamenti degli esperti nello stesso intervallo di quelli riportati su dataset internazionali molto più grandi. In secondo luogo hanno adattato un framework ampiamente usato chiamato nnUNet, partendo da modelli addestrati su challenge internazionali di imaging polmonare ed epatico e poi raffinando questi modelli sui nuovi dati cileni. Dopo il fine‑tuning, i sistemi hanno eguagliato o superato le prestazioni originali, in particolare per i tumori polmonari, nonostante la coorte di pazienti fosse relativamente piccola. Ciò dimostra che dati locali accuratamente curati possono aumentare significativamente l’affidabilità degli strumenti IA in un ambito ospedaliero specifico.
Cosa significa per la futura assistenza oncologica
Per i non specialisti, il messaggio chiave è che questo dataset è uno strumento abilitante, non un prodotto diagnostico di per sé. Condividendo apertamente TC in cui ogni tumore visibile e linfonodo è stato delineato e, in molti casi, misurato con precisione, gli autori forniscono un terreno realistico di addestramento per algoritmi che mirano ad automatizzare il monitoraggio delle lesioni. Strumenti del genere potrebbero aiutare i radiologi a dedicare meno tempo a misurazioni manuali e più tempo a giudizi complessi, riducendo al contempo la variabilità tra lettori. Poiché i dati provengono da un ospedale latino‑americano e sono rilasciati con una licenza permissiva, contribuiscono anche a garantire che la futura IA medica sia testata su pazienti più diversi, migliorando le probabilità che il monitoraggio automatizzato del cancro funzioni in modo affidabile per persone in tutto il mondo.
Citazione: Rojas-Pizarro, R., Vásquez-Venegas, C., Pereira, G. et al. A CT Dataset with RECIST Measurements and Comprehensive Segmentation Masks for Tumors and Lymph Nodes. Sci Data 13, 270 (2026). https://doi.org/10.1038/s41597-026-06597-6
Parole chiave: imaging oncologico, tomografie TC, segmentazione dei tumori, RECIST, dataset per AI medica