Clear Sky Science · it
Il metabolismo della vitamina B2 promuove la stabilità di FSP1 per prevenire la ferroptosi
Come una vitamina comune aiuta le cellule a scegliere tra vita e morte
Le nostre cellule camminano costantemente su un filo tra sopravvivenza e autodistruzione. Una forma drammatica di morte cellulare, chiamata ferroptosi, ha attirato l’attenzione perché può uccidere selettivamente le cellule tumorali resistenti ad altri trattamenti. Questo studio rivela che un nutriente di uso quotidiano — la vitamina B2, o riboflavina — inclina silenziosamente l’equilibrio stabilizzando una proteina protettiva fondamentale. Capire questo collegamento nascosto tra dieta, metabolismo cellulare e morte delle cellule tumorali potrebbe aiutare i ricercatori a progettare terapie più intelligenti e a raffinare i futuri consigli nutrizionali.
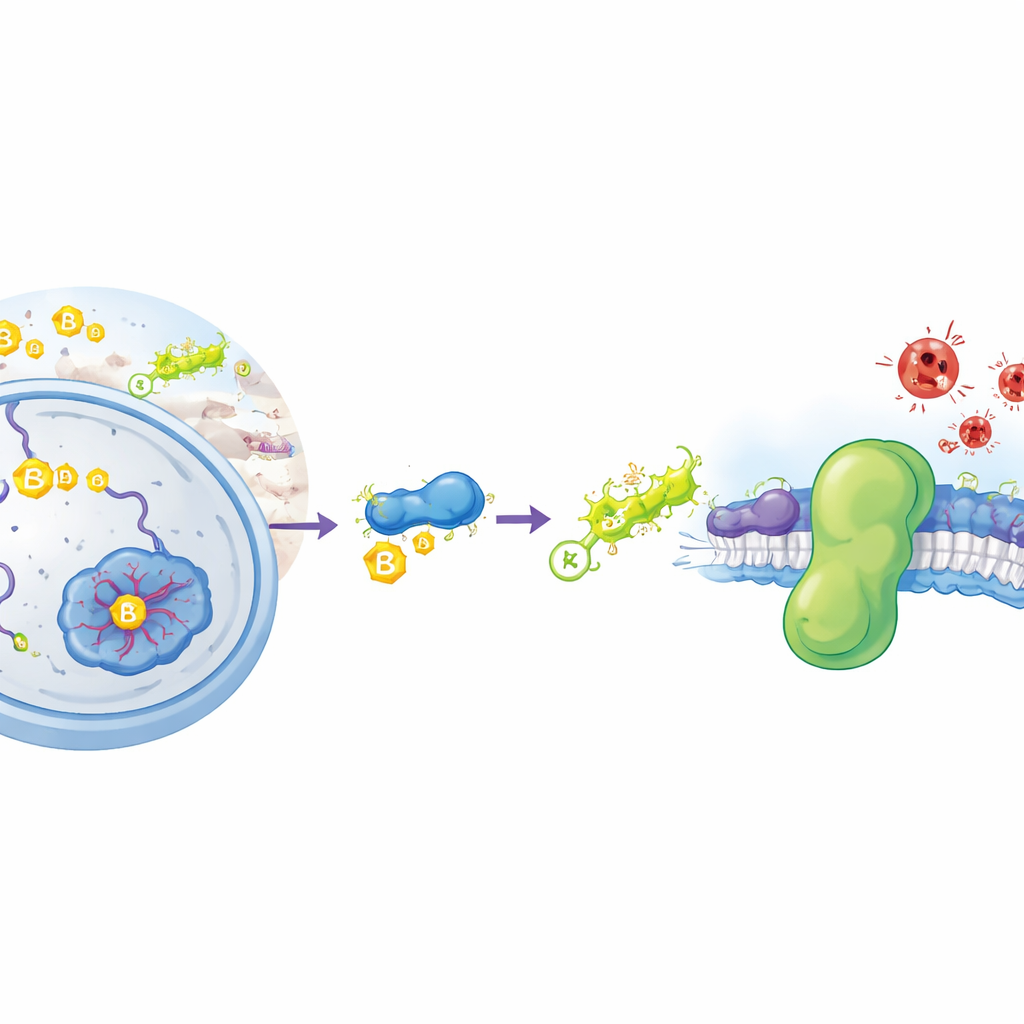
Una forma speciale di ruggine all’interno delle cellule
La ferroptosi è un tipo di morte cellulare guidato da un processo chimico non dissimile dalla ruggine dei metalli: l’ossidazione incontrollata dei lipidi nelle membrane cellulari. Quando questi lipidi si degradano, le membrane perdono integrità e le cellule si rompono. Normalmente le cellule dispongono di diverse difese per evitare che ciò accada. Uno scudo principale è un enzima chiamato GPX4, che usa una piccola molecola, il glutatione, per disattivare i perossidi lipidici dannosi. Un secondo scudo parallelo è una proteina chiamata FSP1, che si trova sulle membrane cellulari e utilizza piccole molecole lipofile per intercettare i radicali distruttivi prima che si propaghino. Le cellule tumorali spesso aumentano l’espressione di FSP1 per evitare la ferroptosi, rendendo questa proteina un obiettivo prioritario per nuovi farmaci anticancro. Tuttavia, fino ad ora gli scienziati non sapevano come le cellule regolassero la quantità di FSP1 prodotta e la sua durata di vita.
Costruire un “indicatore di carburante” cellulare per un blocco della morte
Per scoprire i gestori nascosti di FSP1, i ricercatori hanno prima modificato geneticamente cellule umane di un tumore osseo per portare un indicatore fluorescente. Hanno marcato la proteina FSP1 naturale con un segnale di luce verde e l’hanno accoppiata a un segnale blu che riferisce quanto messaggio di FSP1 la cellula sta producendo. Questo design intelligente ha permesso di distinguere i cambiamenti nell’attività genica (blu) da quelli nella stabilità della proteina (verde). Con questo sistema a due colori, hanno usato CRISPR–Cas9 per interrompere sistematicamente quasi ogni gene del genoma e poi hanno ordinato le cellule con livelli di FSP1 alti o bassi. Confrontando quali guide RNA erano arricchite in ciascun gruppo, hanno mappato centinaia di geni che aumentano o diminuiscono FSP1, agendo a livello di controllo genico o turnover proteico.
Il compito nascosto della vitamina B2: creare una presa stabilizzante
Tra i risultati più sorprendenti c’erano due enzimi, la riboflavina chinasi (RFK) e la FAD sintasi (FLAD1), che convertono la vitamina B2 in un cofattore chiamato FAD. FSP1 è una flavoproteina che normalmente lega saldamente FAD per svolgere le sue reazioni chimiche. Quando RFK o FLAD1 venivano rimossi, o quando le cellule erano cresciute in un mezzo carente di vitamina B2, i livelli della proteina FSP1 calavano bruscamente nonostante l’attività del suo gene rimanesse simile. Il gruppo ha dimostrato che questa perdita rendeva le cellule molto più vulnerabili alla ferroptosi quando GPX4 era bloccato. È importante notare che la vitamina B2 in sé non agiva come un classico antiossidante: in un test sensibile in provetta non è riuscita a fermare l’ossidazione lipidica, a differenza della vitamina E. Invece, l’aggiunta di FAD (e in parte del suo precursore FMN) a cellule carenti ha ripristinato sia i livelli di FSP1 sia la resistenza alla morte per ferroptosi, mentre l’ulteriore vitamina B2 da sola non ha aiutato se gli enzimi di processamento mancavano.
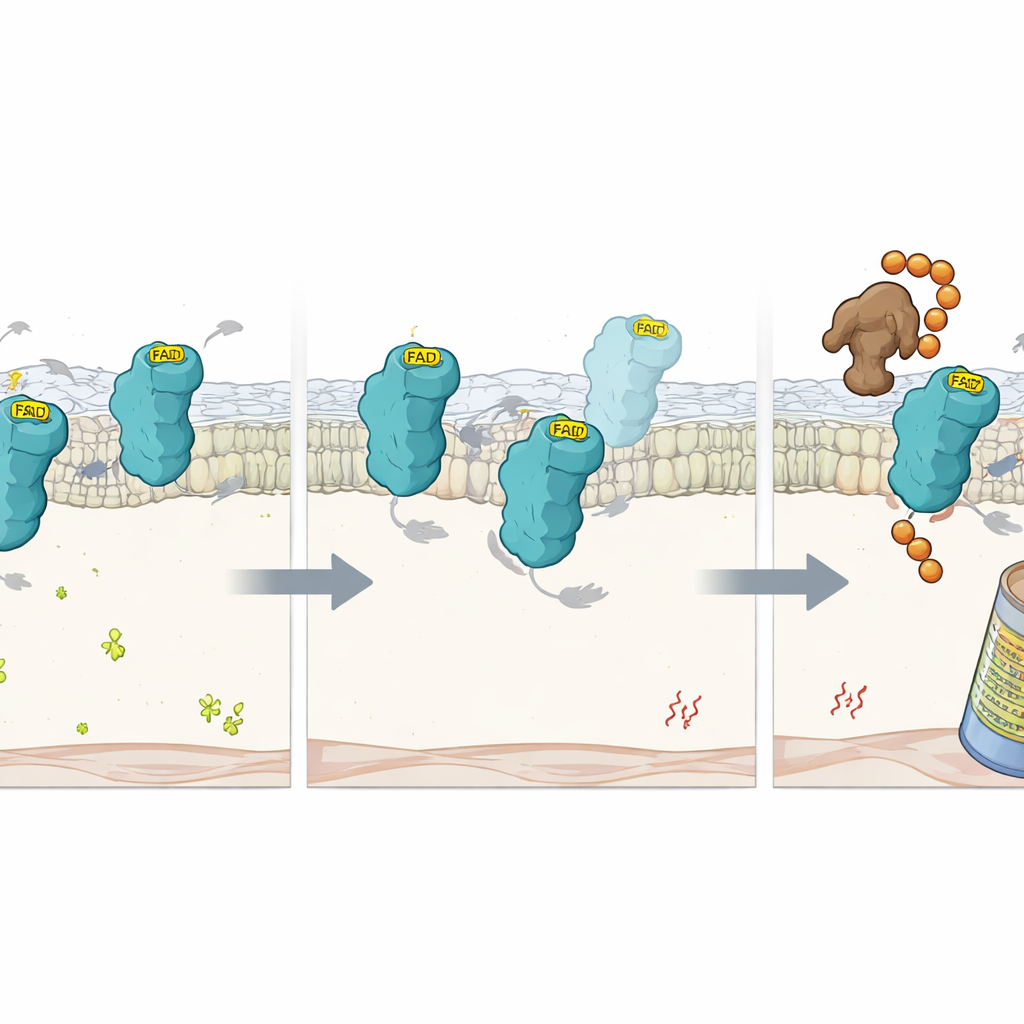
Cosa succede quando manca il cofattore
Per approfondire, gli scienziati hanno studiato mutazioni precise in FSP1 che ne compromettevano la capacità di trattenere FAD. Queste proteine mutanti si piegavano ancora in strutture in gran parte normali ma avevano perso FAD e l’attività catalitica. All’interno delle cellule, si degradavano molto più rapidamente rispetto alla FSP1 normale, a meno che il proteasoma — la macchina cellulare che frammenta le proteine — non fosse bloccato. Ciò suggerisce che il legame con FAD funge da maniglia stabilizzante che protegge FSP1 dall’essere marcata come difettosa. Usando un altro screen CRISPR mirato in condizioni di basso FAD, il team ha identificato una ligasi E3 chiamata RNF8 come fattore chiave che riconosce FSP1 priva di FAD. Quando RFK veniva eliminata, RNF8 attaccava catene di ubiquitina alla proteina vuota, destinandola alla distruzione da parte del proteasoma. Rimuovere RNF8 rallentava il turnover di FSP1 nelle cellule povere di FAD, sebbene non potesse ripristinarne la funzione protettiva perduta senza il cofattore.
Dai circuiti molecolari alle idee per terapie contro il cancro
Mettendo insieme questi pezzi, gli autori propongono un modello semplice ma potente. La vitamina B2, dopo essere convertita in FAD da RFK e FLAD1, si lega a FSP1 ed è essenziale sia per la sua attività biochimica sia per la sua longevità. Quando la fornitura di vitamina B2 o il suo processamento falliscono, la FSP1 appena sintetizzata non riesce a legare FAD, viene segnalata da RNF8 e viene rapidamente smantellata dal proteasoma, lasciando le cellule più esposte ai danni da ferroptosi. Dati tumorali suggeriscono che i tumori con maggiore espressione di RFK sono più resistenti ai farmaci che inducono la ferroptosi, sottolineando la rilevanza di questo percorso nel mondo reale. Per i non specialisti, il messaggio chiave è che una vitamina familiare fa molto più che agire come semplice antiossidante: aiuta a decidere se una potente proteina anti-morte resta di guardia o viene spazzata via. Modulare il metabolismo della vitamina B2 o la stabilità di FSP1 potrebbe permettere a future terapie di sfruttare meglio la ferroptosi per eliminare le cellule tumorali risparmiando i tessuti sani.
Citazione: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Parole chiave: ferroptosi, vitamina B2, FSP1, morte delle cellule tumorali, metabolismo cellulare