Clear Sky Science · it
Cartografia, origine e ruolo dei chimeri elemento trasponibile–gene nel potenziare la plasticità del trascrittoma
Passeggeri nascosti nel nostro DNA
Gran parte del nostro DNA è composta da antichi passeggeri virali chiamati elementi trasponibili—frammenti di codice genetico che un tempo saltavano nei genomi come parassiti autostoppisti. Questo studio dimostra che questi vecchi frammenti virali non sono solo rifiuti silenti: possono inserirsi nei nostri geni per creare messaggi ibridi, aiutare le cellule ad adattarsi a condizioni mutevoli e talvolta alimentare malattie. Mappando questi ibridi attraverso lo sviluppo, l'invecchiamento e il cancro, gli autori rivelano un modo sorprendente in cui il DNA virale continua a plasmare la biologia umana oggi.
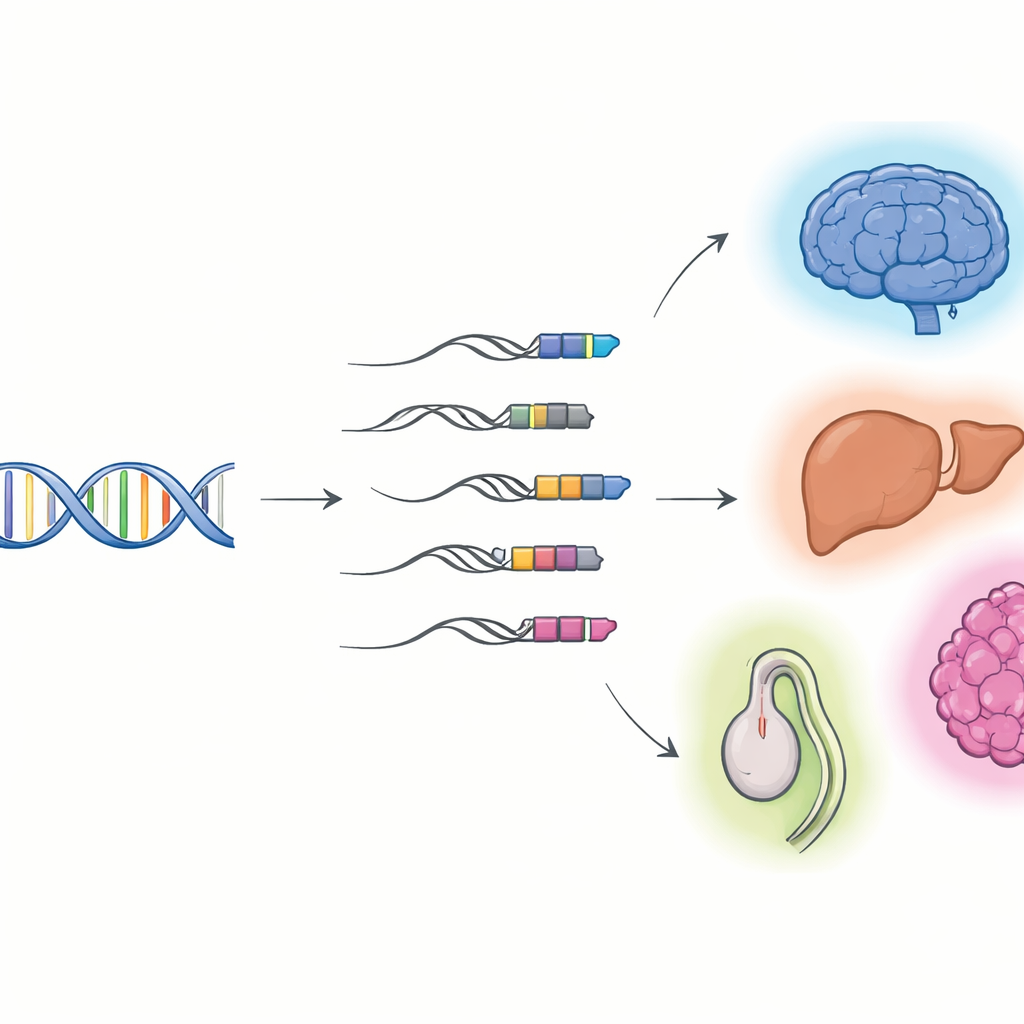
Quando il DNA virale diventa parte dei nostri geni
I ricercatori si sono concentrati sui “chimeri TE–gene”: molecole di RNA che iniziano in un elemento trasponibile e poi proseguono in un gene ospite. Usando il sequenziamento a lettura lunga, che può catturare interi RNA da un capo all'altro, combinato con il consueto sequenziamento a lettura corta, hanno costruito cataloghi dettagliati di questi ibridi in cellule e organi di topo e uomo. Hanno trovato migliaia di trascritti chimerici precedentemente sconosciuti, la maggior parte dei quali sono RNA non codificanti piuttosto che modelli per proteine. Molti iniziano in una classe di residui virali chiamati long terminal repeat (LTR), che spesso si trovano davanti ai geni e possono funzionare come interruttori alternativi di accensione/spegnimento. Tessuti e organi diversi usano insiemi diversi di questi chimeri, con attività particolarmente ricca nel cervello, nel fegato e nei testicoli, e il loro uso cambia mentre i tessuti si sviluppano da fasi fetali ad adulte.
Chimeri nell'invecchiamento e nel cancro
Per capire come si comportano questi ibridi virali–ospite nelle popolazioni reali, il gruppo ha analizzato grandi dataset umani che coprono dozzine di tessuti di centinaia di persone, oltre a campioni tumorali. Hanno identificato diverse centinaia di chimeri ad alta confidenza che ricorrono tra gli individui. La loro espressione varia non solo tra gli organi ma anche con l'età: in tessuti come sangue e cervello, alcuni chimeri guidati da LTR diminuiscono negli adulti più anziani, mentre in certi tessuti periferici aumentano. In molti tipi di cancro, questi ibridi basati su LTR risultano ampiamente upregolati nei tumori rispetto al tessuto normale circostante, e i pazienti i cui tumori esprimono di più questi elementi tendono ad avere esiti peggiori. In dataset di persone resistenti a chemioterapia o immunoterapia, i geni interessati da nuovi esoni guidati da LTR spesso appartengono a vie collegate al meccanismo d'azione di quei farmaci, suggerendo che i chimeri TE possono aiutare i tumori a riorientarsi sotto la pressione terapeutica.
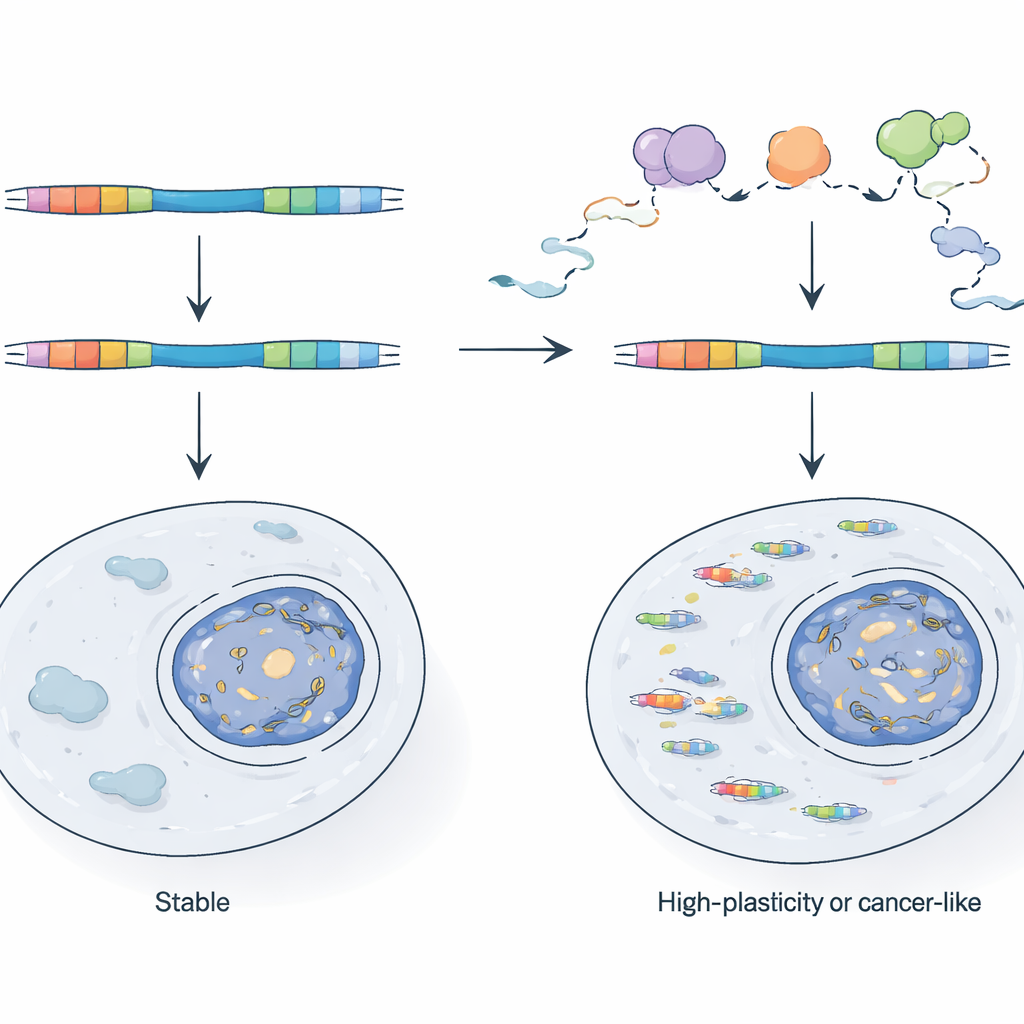
Come le cellule tengono sotto controllo gli ibridi virali
Data la loro potenza, perché i chimeri TE non sovrastano le cellule normali? Gli autori mostrano che le cellule fanno affidamento su un sistema di controllo qualità dell'RNA, incentrato sul complesso esossoma nucleare, per pattugliare e distruggere molti di questi trascritti mentre vengono prodotti. Quando compromettono geneticamente un componente chiave dell'esossoma nelle cellule staminali di topo, i promotori guidati da LTR diventano molto più attivi e gli RNA chimerici aumentano in modo marcato. Confrontando l'RNA appena sintetizzato con l'RNA stabile, dimostrano che alcuni LTR sono normalmente tenuti sotto controllo perché i loro trascritti vengono degradati rapidamente, mentre altri sono regolati a livello della frequenza di inizio della trascrizione. Questi LTR attivi tendono a trovarsi in regioni del genoma già accessibili e frequentemente trascritte, indicando che il semplice trovarsi vicino a un gene attivo o a un trascritto antisenso può aiutare un frammento virale a sfuggire al silenziamento epigenetico tradizionale.
Splicing, plasticità delle cellule staminali e un “interruttore maestro” virale
La storia si fa più intricata quando la macchina dello splicing cellulare viene perturbata. Gli autori riducono l'espressione di diversi fattori di splicing core o inibiscono chimicamente lo spliceosoma e osservano un esito condiviso con la perdita dell'esossoma: un forte aumento dei chimeri guidati da LTR e di geni corti, poveri di introni. Tra i protagonisti c'è MERVL, un retrovirus endogeno attivo nelle primissime fasi dell'embrione di topo. Quando la sequenza interna di MERVL e i fattori di trascrizione a valle vengono sovraregolati, le cellule staminali si spostano verso uno stato più «totipotente-simile», simile alle prime cellule embrionali in grado di formare tutti i tessuti. Al contrario, degradare l'RNA di MERVL con oligonucleotidi antisenso attenua questo spostamento e riduce l'attività dei promotori LTR, indicando che MERVL agisce come un interruttore maestro in grado di innescare una rete più ampia di chimeri TE e di plasticità degli stati cellulari.
Innovazione virale attraverso l'evoluzione
Analizzando molti genomi di mammiferi, il gruppo ricostruisce quando diverse famiglie di TE hanno iniziato a donare esoni ai geni ospiti. Sia negli esseri umani sia nei topi, le famiglie di LTR relativamente giovani sono particolarmente propense a formare chimeri in orientamento «sense» che possono essere letti come parte dei trascritti dell'ospite. Questo schema suggerisce che nuove ondate di inserzioni di TE hanno ripetutamente fornito materiale grezzo alle reti regolatorie geniche nel corso dell'evoluzione. Piuttosto che essere puramente dannose, queste inserzioni possono essere messe alla prova dai meccanismi di trascrizione e degradazione della cellula: la maggior parte viene silenziata o degradata, ma una minoranza si trova nella posizione e nel contesto giusto per essere cooptata come elementi regolatori utili o nuovi inizi di gene.
Perché questi residui virali sono importanti
Per un non specialista, questo lavoro mostra che una porzione ampia e un tempo sottovalutata del nostro genoma sta attivamente plasmando il modo in cui i geni vengono letti, come le cellule cambiano identità e come progrediscono le malattie. Sequenze virali antiche possono essere trasformate in «porte d'ingresso» alternative dei geni, producendo RNA ibridi che normalmente sono sorvegliati dai sistemi di pulizia cellulare. Quando quel controllo o lo splicing normale viene meno, questi ibridi possono esplodere, spingendo le cellule staminali verso stati più flessibili o aiutando i tumori ad adattarsi e a resistere alle terapie. Nel corso di milioni di anni, l'evoluzione ha ripetutamente smanettato con questi frammenti virali, trasformando molti da parassiti genomici in mattoni della complessità regolatoria—lasciandoci con un trascrittoma molto più plastico e dinamico di quanto una semplice lista di geni suggerirebbe.
Citazione: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Parole chiave: elementi trasponibili, trascritti chimerici, sorveglianza dell'RNA, plasticità delle cellule staminali, evoluzione del cancro