Clear Sky Science · it
Adattamento allo stress dell’importazione proteica mitocondriale tramite degradazione di DNAJC15 mediata da OMA1
Come le nostre cellule reagiscono quando le loro centrali sono sotto stress
Ogni cellula del corpo dipende da piccole strutture chiamate mitocondri per convertire il cibo in energia utilizzabile. Come miniere officine, i mitocondri importano costantemente nuovi componenti — proteine prodotte altrove nella cellula — per mantenere in funzione la loro macchina. Questo articolo rivela come, quando i mitocondri sono sotto stress o danneggiati, la cellula riduca deliberatamente questo flusso di importazione proteica. In tal modo si protegge dal sovraccarico e si coordina una risposta allo stress più ampia che coinvolge non solo i mitocondri, ma anche un altro compartimento chiave, il reticolo endoplasmatico.
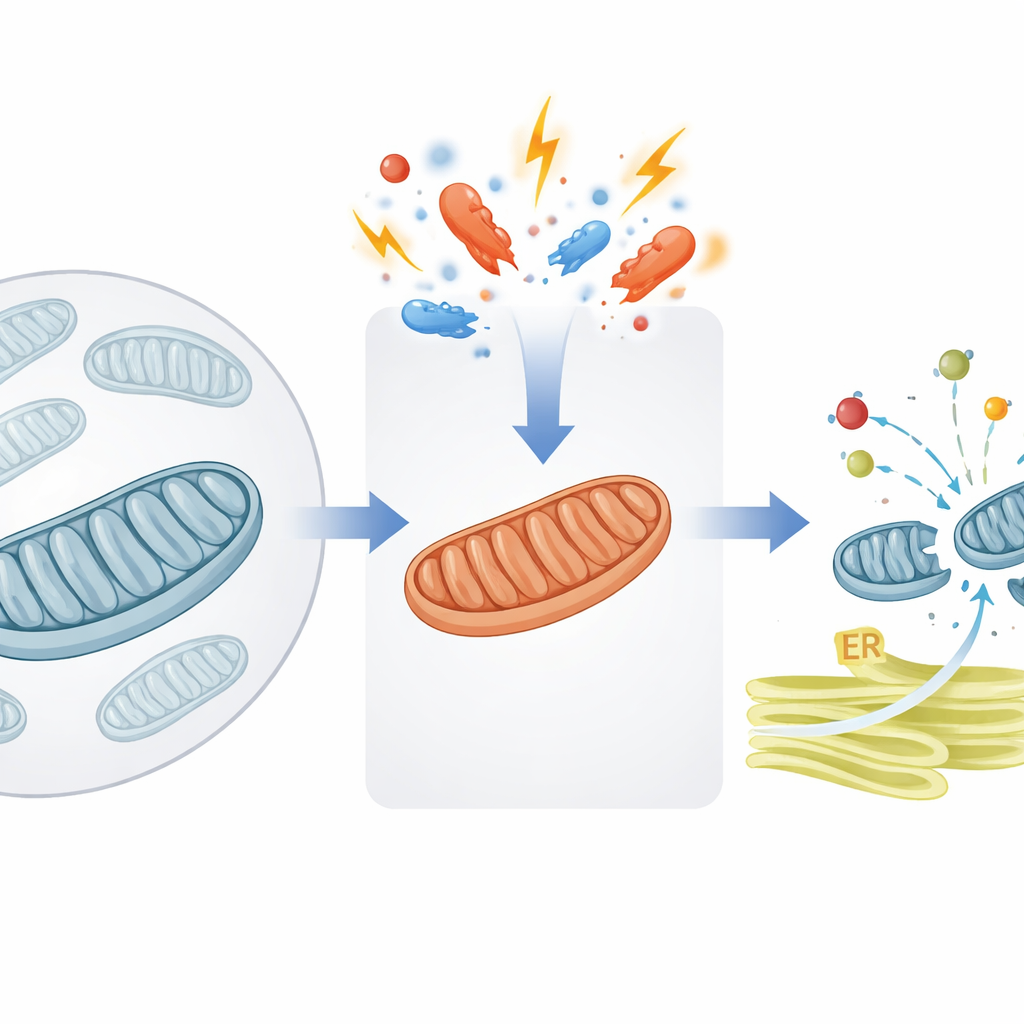
Una valvola di sicurezza per il traffico proteico mitocondriale
I mitocondri dipendono da migliaia di proteine che vengono prima sintetizzate nel compartimento principale della cellula e poi convogliate all’interno. Gli autori si concentrano su un passaggio cruciale nella membrana interna mitocondriale, assistito da una proteina coadiuvante chiamata DNAJC15. In condizioni normali, DNAJC15 agevola il trascinamento dei nuovi «pacchetti» proteici attraverso il canale di importazione verso l’interno mitocondriale, dove molte di queste proteine vanno a comporre la macchina produttiva di energia nota come fosforilazione ossidativa (OXPHOS). Lo studio mostra che quando i mitocondri subiscono stress — per esempio una ridotta produzione di energia o alterazioni delle proprietà di membrana — la cellula attiva un interruttore molecolare che modifica la quantità di proteine che l’organello è disposto ad accogliere.
OMA1: il tagliatore attivato dallo stress
Al centro di questo interruttore c’è un enzima sensibile allo stress chiamato OMA1, incastonato nella membrana interna mitocondriale. Quando i mitocondri incontrano problemi, OMA1 si attiva e recide DNAJC15 in una posizione specifica vicina all’estremità iniziale. Questo taglio genera una versione più corta di DNAJC15 che viene rapidamente degradata da un altro complesso enzimatico mitocondriale, la proteasi m-AAA. Di conseguenza si perde la forma a lunghezza intera di DNAJC15, competente per l’importazione. Gli autori mostrano che le cellule prive di DNAJC15, o in cui DNAJC15 viene rapidamente eliminata dopo l’attivazione di OMA1, hanno una capacità ridotta di introdurre nuove proteine nei mitocondri, in particolare quelle necessarie per assemblare e mantenere i complessi OXPHOS.
Rallentare l’assemblaggio energetico in base allo stato di salute mitocondriale
Utilizzando misure proteomiche su larga scala e saggi di importazione, il gruppo ha scoperto che DNAJC15 è particolarmente importante per fornire all’interno mitocondriale proteine coinvolte nell’espressione genica e nell’assemblaggio della catena respiratoria. Quando DNAJC15 manca, queste proteine si accumulano più lentamente all’interno dei mitocondri e la capacità degli organelli di consumare ossigeno e alimentare la produzione energetica — misurata in mitocondri isolati — diminuisce, soprattutto per il complesso I della catena respiratoria. Un altro componente del canale di importazione, TIMM17A, lavora in sinergia con DNAJC15: la perdita di entrambi provoca difetti particolarmente pronunciati nei livelli delle proteine ribosomiali mitocondriali e dei componenti OXPHOS. Nel loro insieme, questi risultati suggeriscono che la distruzione mediata da OMA1 di DNAJC15 è un modo per ridurre temporaneamente la costruzione di nuova apparecchiatura energetica finché l’organello non si è ripreso.
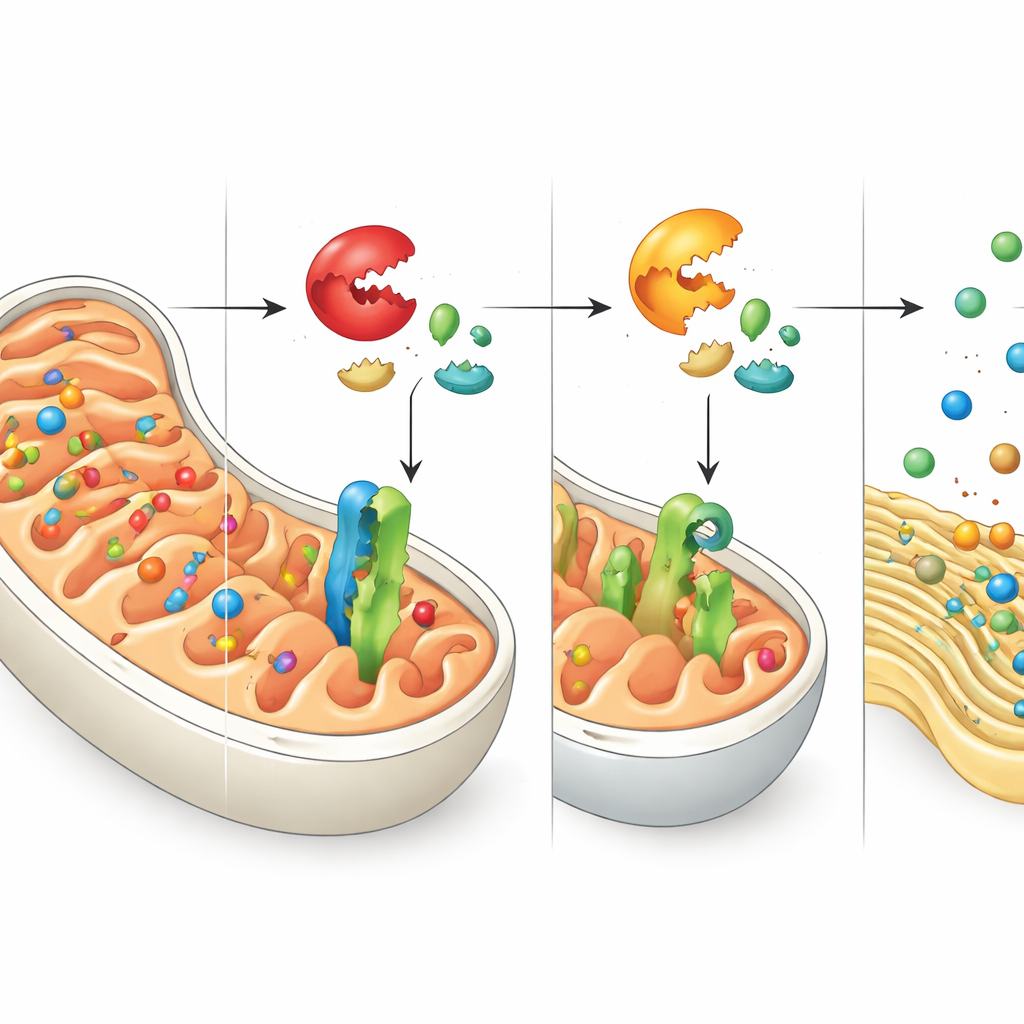
Pacchetti smistati male e un appello d’aiuto al reticolo endoplasmatico
La disattivazione di DNAJC15 non impedisce alla cellula di sintetizzare proteine mitocondriali: limita principalmente il loro arrivo alla destinazione prevista. Gli autori hanno tracciato dove finiscono queste proteine rimaste a terra e hanno scoperto che molte si localizzano al reticolo endoplasmatico (ER), una rete di membrane che normalmente aiuta a ripiegare e processare insiemi diversi di proteine. Queste proteine mitocondriali deviate si inseriscono nelle membrane dell’ER, disturbando l’equilibrio del controllo qualità dell’ER stesso. In risposta, la cellula attiva un programma protettivo noto come risposta alle proteine mal ripiegate, specificamente attraverso un ramo controllato dal sensore ATF6. Questa risposta aumenta la capacità dell’ER di gestire proteine mal ripiegate o mal localizzate, rivelando una stretta coordinazione tra i sistemi di stress mitocondriale e dell’ER.
Un rallentamento coordinato per proteggere la cellula
Complessivamente, lo studio dipinge il quadro di un sistema frenante integrato per la biogenesi mitocondriale. Quando i mitocondri sono sotto stress, OMA1 taglia e indirettamente porta alla distruzione di DNAJC15, riducendo il flusso di nuove proteine legate all’energia verso organelli compromessi. Alcune di queste proteine vengono temporaneamente tamponate dall’ER, che mette in atto la propria risposta protettiva. Collegando la capacità di importazione mitocondriale alla salute degli organelli e coinvolgendo l’ER come sito di riserva per le proteine in eccesso, le cellule possono evitare di intasare mitocondri danneggiati e guadagnare tempo per ripararli o rimuoverli del tutto. Per un osservatore non specialista, questo lavoro mostra quanto siano profondamente integrate le nostre reti di controllo qualità cellulare: anche i più piccoli errori in un compartimento vengono percepiti e compensati da altri per mantenere la produzione di energia — e la vita stessa — in equilibrio.
Citazione: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Parole chiave: stress mitocondriale, importazione proteica, controllo qualità cellulare, fosforilazione ossidativa, reticolo endoplasmatico