Clear Sky Science · it
Struttura e funzione del supercomplesso sensore degli amminoacidi SEAC–EGOC nel lievito
Come le cellule decidono quando crescere
Ogni cellula deve decidere continuamente se può permettersi di crescere o se è meglio conservare risorse. Questa decisione dipende in larga misura dagli amminoacidi, i mattoni delle proteine e una fonte chiave di azoto. Questo articolo svela, con dettagli strutturali notevoli, come le cellule di lievito percepiscono la disponibilità di amminoacidi attraverso un gigantesco assemblaggio molecolare e usano quell'informazione per accendere o spegnere un importante regolatore della crescita, chiamato TORC1. Poiché lo stesso circuito è conservato nelle cellule umane e legato a cancro e metabolismo, le scoperte nel lievito offrono una finestra su come anche le nostre cellule valutano quando le condizioni sono favorevoli alla crescita.
Un hub intricato sul centro di riciclaggio della cellula
Nel lievito, un complesso decisionale centrale chiamato SEAC si trova sulla membrana della vacuola, un organello che funge da centro di riciclaggio cellulare. Lì incontra un altro complesso, EGOC, che trasmette informazioni sui livelli di amminoacidi. Insieme inviano segnali a TORC1, l'interruttore principale della crescita. SEAC è formato da due metà funzionali: SEACIT, che può spegnere TORC1, e SEACAT, a lungo ritenuta responsabile del controllo di SEACIT. Gli autori hanno utilizzato la crio–microscopia elettronica ad alta risoluzione per visualizzare il SEAC completo legato a EGOC, catturando un'istantanea di questo hub molecolare proprio dove avviene la segnalazione, sulla superficie della vacuola. 
Vedere da vicino l'architettura molecolare
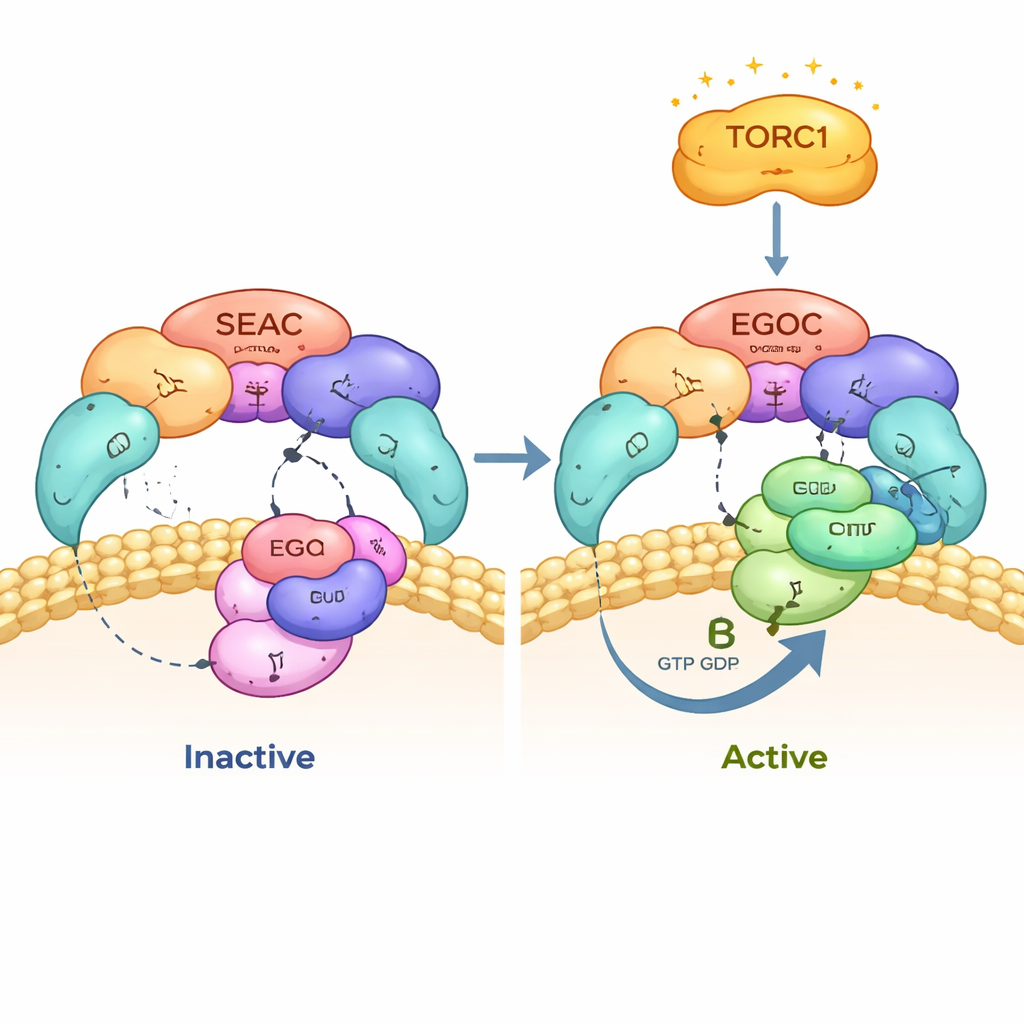
La struttura mostra SEAC come un grande nucleo composto da subunità SEACAT, dal quale si estendono due «ali» flessibili di SEACIT. Ciascuna ala può legare un complesso EGOC, perciò un singolo SEAC può ricevere due ingressi di segnalazione contemporaneamente. È evidente che EGOC si attacca solo alle ali e non al nucleo, e la forma complessiva di SEAC cambia pochissimo quando EGOC è presente. Questo indica che SEACAT non ostruisce fisicamente il sito attivo di SEACIT e non impedisce l'associazione di EGOC. L'orientamento del complesso sulla membrana della vacuola posiziona inoltre il nucleo di SEAC rivolto verso il citoplasma, dove può interagire con regolatori aggiuntivi, mentre le ali si trovano vicine alla membrana, ideale per contattare EGOC e altri partner ancorati alla membrana.
Come SEAC sceglie il segnale giusto
Gli autori hanno analizzato in dettaglio i contatti tra SEAC ed EGOC e hanno scoperto che SEAC riconosce solo la versione «attiva» di EGOC, nella quale una delle piccole GTPasi, Gtr1, porta una nucleotide simile al GTP, mentre la sua compagna, Gtr2, è legata al GDP. SEACIT fornisce un «dito» catalitico che raggiunge la tasca della nucleotide di Gtr1 e accelera l'idrolisi del GTP, trasformando EGOC dallo stato attivo a quello inattivo. Mappe crio-EM ad alta risoluzione ed esperimenti di mutagenesi mostrano che questo dito catalitico e un residuo ausiliario vicino sono essenziali per l'interazione e per la lettura corretta dello stato nucleotidico. Quando gli autori hanno alterato questi residui chiave, SEAC non si localizzava più correttamente alla vacuola e EGOC non poteva interagire in modo produttivo.
Controllo rapido versus lento dell'interruttore di crescita
Per capire cosa ciò significhi nella cellula vivente, i ricercatori hanno seguito l'attività di TORC1 nel tempo quando gli amminoacidi sono stati rimossi e poi reintrodotti. Nelle cellule normali, TORC1 si spegne rapidamente entro pochi minuti di carenza di azoto e poi si riaccende altrettanto rapidamente quando gli amminoacidi ritornano. Quando il dito catalitico di SEACIT è stato disattivato, o subunità di SEACIT sono state cancellate, TORC1 ha mostrato scarsa risposta in questa finestra temporale precoce. Lo stesso effetto si è osservato con la rimozione di entrambi Gtr1 e Gtr2, dimostrando che la coppia SEAC–EGOC è la via dominante e rapida per il controllo amminoacidico di TORC1. Tuttavia, a tempi più lunghi—intorno alla mezz'ora—l'attività di TORC1 si è adattata lentamente anche in questi mutanti, indicando che esiste anche una via separata e più lenta verso TORC1, indipendente da questo sistema di GTPasi.
Un ruolo sorprendente per una subunità distante
Una scoperta particolarmente intrigante riguarda Sea2, una componente di SEACAT con un dominio «elica» flessibile che sporge dal nucleo. La rimozione di Sea2, o solo della sua elica, ha prodotto difetti di segnalazione quasi identici a quelli osservati quando l'attività catalitica di SEAC è venuta meno: TORC1 rispondeva con lentezza sia al prelievo che al reintegro degli amminoacidi. Eppure Sea2 si trova lontana dal sito catalitico e non tocca direttamente l'ala SEACIT, rendendo improbabile un semplice meccanismo di blocco. Esperimenti genetici che combinavano la perdita di Sea2 con una variante cataliticamente inattiva di SEAC suggeriscono che avere l'attività GAP completamente attiva o completamente spenta compromette entrambe la risposta rapida, mentre è necessaria una regolazione intermedia. Gli autori propongono che l'elica di Sea2 funzioni da piattaforma di aggancio per un fattore sconosciuto che modera l'attività di SEACIT, permettendo alle cellule di modulare finemente TORC1 invece di spegnerlo definitivamente.
Cosa significa per le decisioni sulla crescita cellulare
Nel complesso, lo studio ridisegna il ruolo di SEAC non come due assemblaggi opposti ma come una macchina unica e integrata la cui ala catalitica (SEACIT) e il nucleo strutturale (SEACAT) collaborano per percepire gli amminoacidi e regolare rapidamente l'interruttore di crescita TORC1. L'azione enzimatica di SEACIT su EGOC fornisce il controllo rapido e preciso, mentre l'elica di Sea2 probabilmente recluta regolatori che modulano questa attività. Allo stesso tempo, vie parallele più lente assicurano che TORC1 rifletta comunque lo stato dei nutrienti anche se il sensore principale è compromesso. Poiché complessi strettamente imparentati svolgono lo stesso ruolo nelle cellule umane, queste intuizioni dal lievito chiariscono come le nostre cellule bilancino crescita e disponibilità di nutrienti, con implicazioni per la comprensione delle malattie in cui la segnalazione TORC1 è alterata.
Citazione: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Parole chiave: rilevamento degli amminoacidi, segnalazione TORC1, complesso SEAC GATOR, controllo della crescita cellulare, crio-microscopia elettronica