Clear Sky Science · it
Meccanismo e ricostruzione della trascrizione circadiana nei cianobatteri
Perché gli orologi biologici contano, anche per i batteri
Tutti gli esseri viventi, dagli esseri umani ai minuscoli microbi, tengono il tempo. Questi orologi interni aiutano gli organismi a prevedere l’alba e il tramonto, programmando attività come l’alimentazione, la riparazione e la crescita. Questo articolo esplora come un semplice batterio fotosintetico, Synechococcus elongatus, usa un orologio proteico per accendere e spegnere i geni con notevole precisione su un ciclo di circa 24 ore. Ricostruendo questo sistema temporale in provetta, i ricercatori svelano una versione essenziale di un orologio biologico che potrebbe ispirare nuovi strumenti per la biotecnologia e la biologia sintetica.
Un piccolo orologio che funziona con la chimica
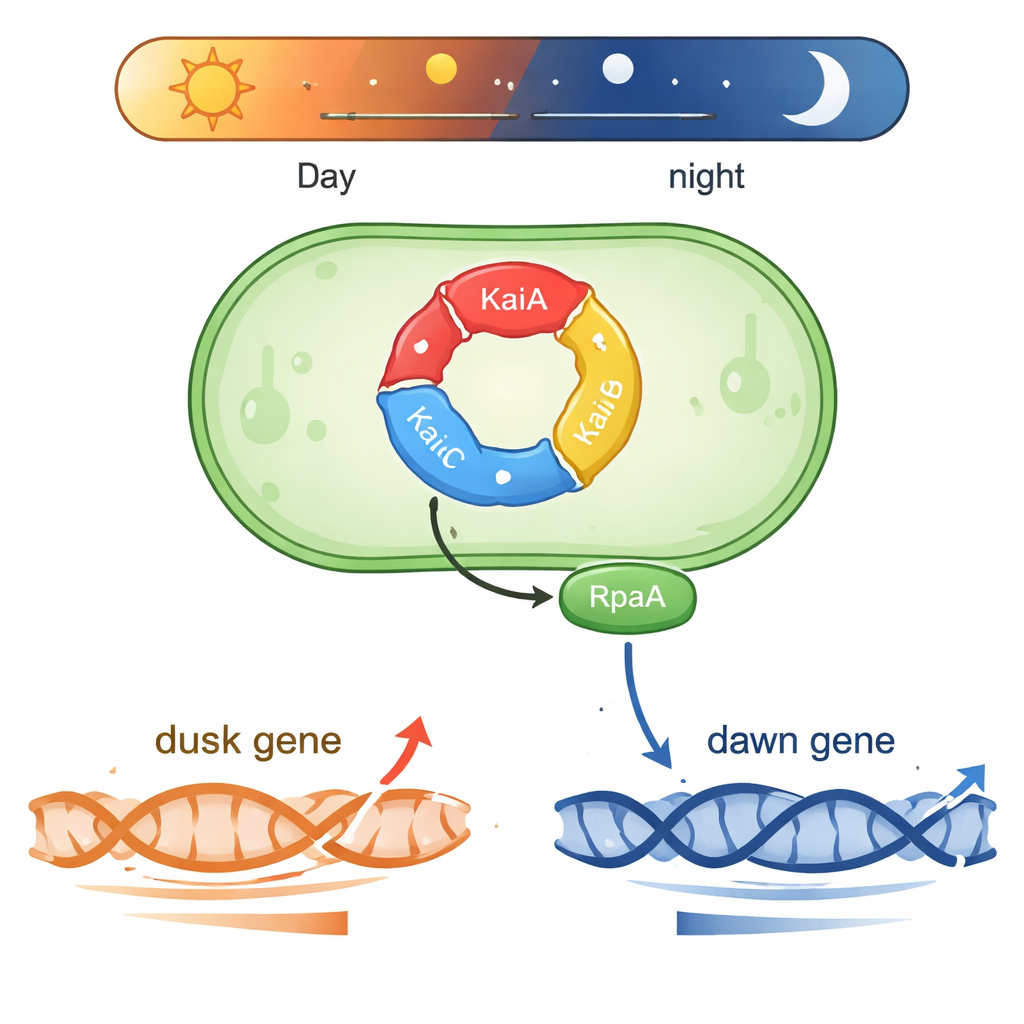
Synechococcus vive in acque illuminate dal sole e ha bisogno di prevedere i cambiamenti quotidiani di luce. Al suo centro c’è una macchina proteica in tre parti composta da KaiA, KaiB e KaiC. Queste proteine trasferiscono gruppi fosfato in un ciclo ripetuto che dura circa 24 ore, formando un “treno di ingranaggi” biochimico che tiene il tempo anche al di fuori della cellula. Altre due proteine, SasA e CikA, leggono lo stato di fosforilazione di KaiC e lo usano per controllare un’altra proteina, RpaA. Quando RpaA è fosforilata, si lega al DNA e funge da interruttore principale per centinaia di geni che oscillano verso l’alto o verso il basso attorno al “mattino” o alla “sera” soggettivi in condizioni di luce costante.
Una proteina, due programmi genici opposti
Un enigma nella biologia circadiana è come un singolo fattore di output, RpaA, possa coordinare geni che raggiungono il picco in momenti molto diversi della giornata. Gli autori si sono concentrati su due regioni di controllo del DNA rappresentative (promotori): kaiBC, che è più attivo al tramonto, e purF, che picca all’alba. In reazioni controllate usando RNA polimerasi cianobatterica purificata e RpaA, hanno dimostrato che RpaA fosforilata aumenta la trascrizione dal promotore kaiBC riducendo allo stesso tempo la trascrizione dal promotore purF. Esperimenti dettagliati di footprinting hanno mappato esattamente dove RpaA si lega su ciascun frammento di DNA, rivelando che la sua posizione rispetto agli elementi standard del promotore determina se agisce come acceleratore o come freno.
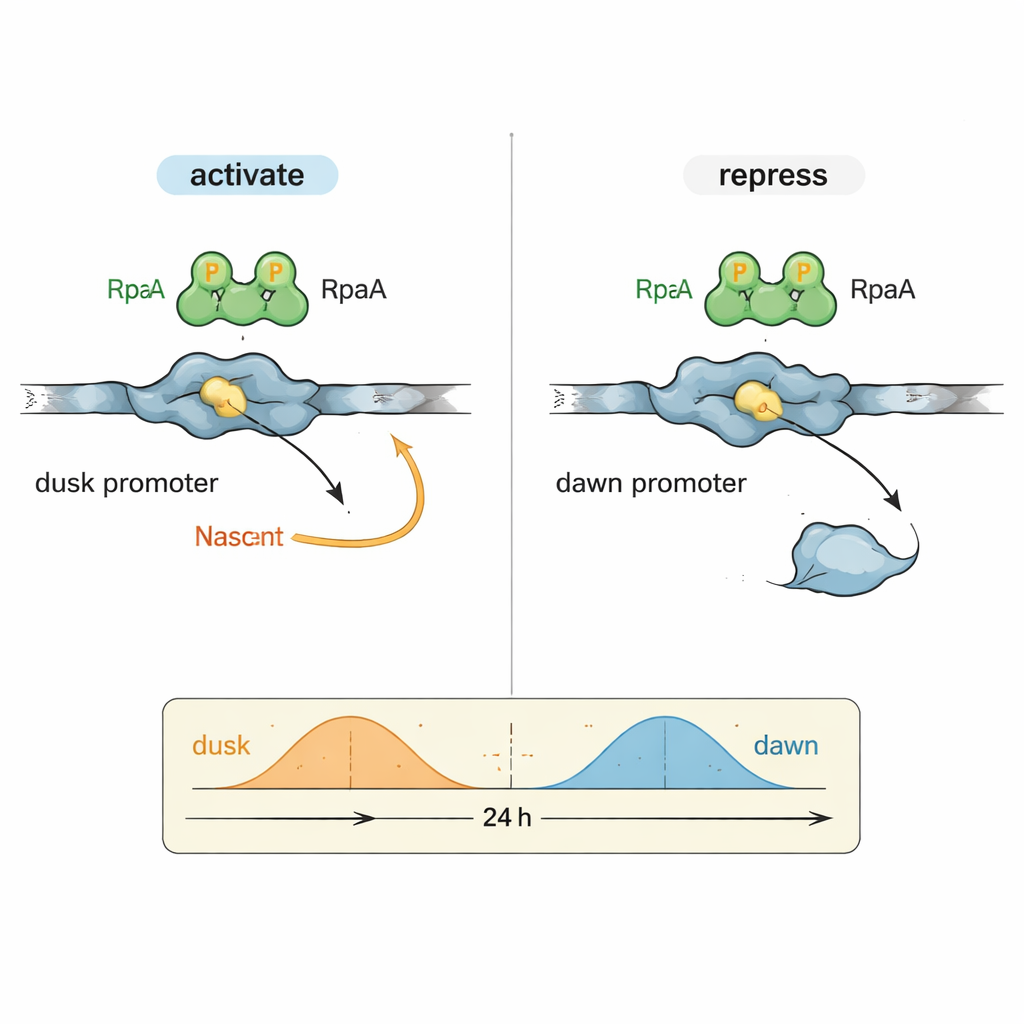
Osservare l’interruttore dell’orologio in dettaglio atomico
Per comprendere questo comportamento duale a livello molecolare, il gruppo ha utilizzato la crio–microscopia elettronica ad alta risoluzione per catturare la struttura di RpaA legato al promotore kaiBC insieme all’RNA polimerasi. Le immagini mostrano RpaA che afferra il DNA come una coppia asimmetrica e che entra in contatto con due parti chiave dell’enzima: la coda della subunità alfa e una regione del fattore sigma che normalmente riconosce le sequenze del promotore. Questi contatti piegano il DNA e aiutano a posizionare l’RNA polimerasi su un sito di inizio della trascrizione leggermente ridefinito. Mutazioni accuratamente scelte che indeboliscono uno qualsiasi di questi punti di contatto riducono o aboliscano l’attivazione di kaiBC, sia in vitro sia nelle cellule viventi, confermando che il reclutamento fisico dell’RNA polimerasi è alla base dell’attivazione genica nella fase serale.
Costruire un gene guidato dall’orologio da zero
Poiché l’RNA polimerasi cianobatterica nativa è complessa e difficile da mantenere attiva per giorni, i ricercatori si sono rivolti alla molto più semplice polimerasi del batteriofago T7, largamente usata nei laboratori. RpaA non può reclutare questo enzima non correlato, ma può comunque bloccarlo posizionandosi sul DNA. Il gruppo ha progettato un modello di DNA sintetico in cui un promotore T7 guida un reporter RNA fluorescente “Broccoli”, con un sito di legame per RpaA posizionato a valle. Quando hanno combinato questo modello con l’orologio KaiA–KaiB–KaiC, la chinasi/fosfatasi CikA, RpaA e la polimerasi T7 in un unico buffer ottimizzato, hanno osservato tassi di trascrizione che aumentavano e diminuivano con un periodo di circa 24 ore. Il ritmo poteva essere resettato cambiando il rapporto ATP/ADP e manteneva quasi lo stesso periodo su un intervallo di temperature: caratteristiche classiche di un vero orologio circadiano.
Da orologi semplici a sistemi di cronometraggio ingegnerizzati
Lo studio dimostra che bastano sei proteine per collegare un pacemaker chimico a un output genico ritmico: le tre proteine Kai dell’orologio, CikA, RpaA e un’RNA polimerasi. Modificando dove RpaA si posiziona sul DNA, la stessa molecola può far piccare alcuni geni al tramonto e altri all’alba, contribuendo a spiegare le complesse ondate di attività genica osservate nei cianobatteri. Poiché il progetto basato sulla repressione funziona anche con una polimerasi estranea come la T7, dovrebbe essere possibile trapiantare questo modulo di orologio minimo in altri microbi o in sistemi cell-free, permettendo agli scienziati di programmare l’accensione e lo spegnimento dei geni con ritmi giornalieri per ricerca, produzione industriale o future applicazioni terapeutiche.
Citazione: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Parole chiave: orologio circadiano, cianobatteri, regolazione della trascrizione, RpaA, biologia sintetica