Clear Sky Science · it
Indicatori multicolore di nuova generazione per l’imaging in vivo della norepinefrina
Vedere un messaggero cerebrale nascosto
La norepinefrina è una sostanza chimica nel cervello che modula silenziosamente come ci risvegliamo, prestiamo attenzione, formiamo ricordi e reagiamo allo stress. Fino a poco tempo fa, gli scienziati potevano solo intravedere la sua attività con strumenti lenti o imprecisi. Questo articolo presenta una nuova coppia di marcatori fluorescenti che permettono ai ricercatori di osservare il flusso della norepinefrina nel cervello vivente, in tempo reale e con grande dettaglio. Questi progressi potrebbero approfondire la nostra comprensione del sonno, dell’ansia, dell’apprendimento e delle malattie neurodegenerative.
Perché tracciare questo segnale è stato così difficile
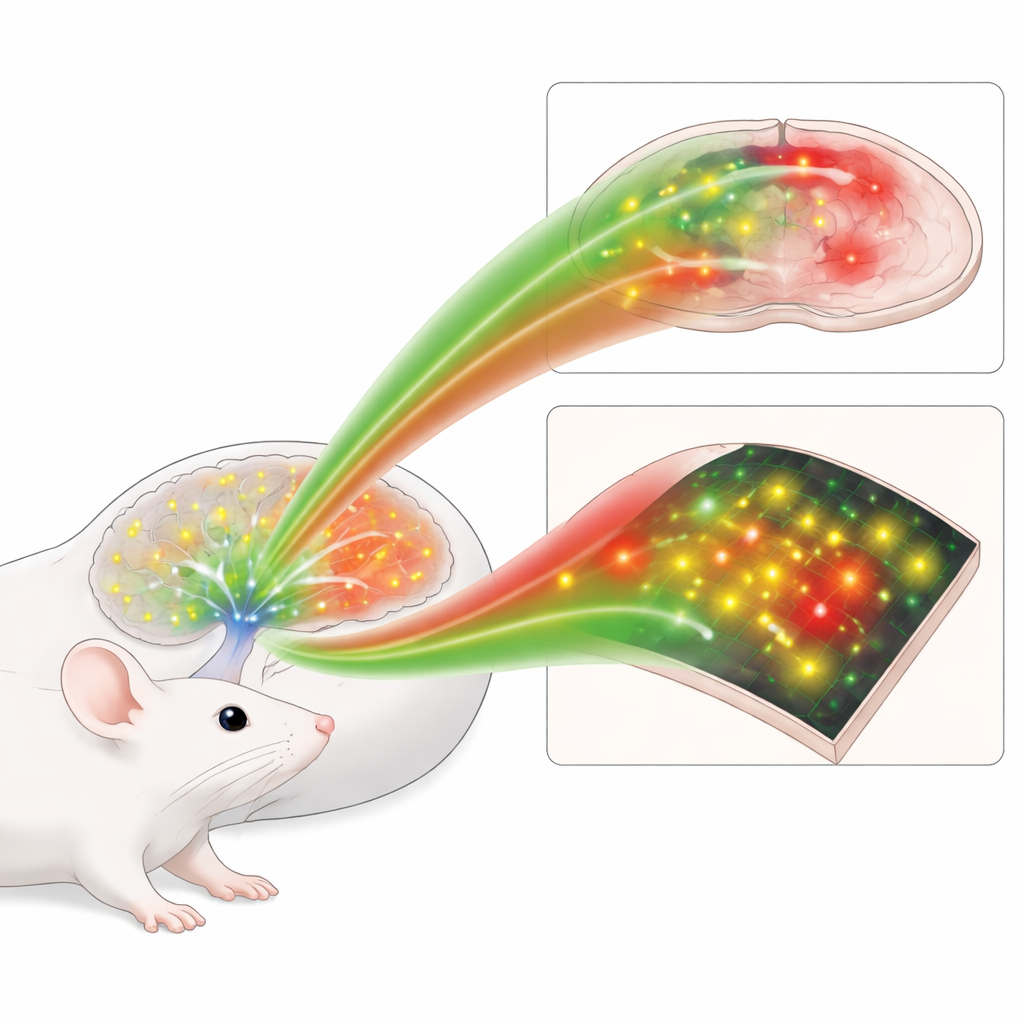
La norepinefrina viene rilasciata da un piccolo gruppo di cellule nel tronco encefalico che inviano fibre in tutto il cervello, modificando il comportamento dei circuiti più che semplicemente accenderli o spegnerli. I metodi classici di misurazione, come minuscole sonde chimiche o cellule impiantate che rispondono alla norepinefrina, sfocano gli eventi su scale di molti secondi o non la distinguono nettamente da molecole correlate. Una strategia più recente usa recettori di membrana modificati che aumentano la luminosità quando legano la norepinefrina, permettendo una lettura ottica. Ma le versioni di prima generazione erano relativamente deboli, specialmente nella parte rossa dello spettro, e non erano abbastanza flessibili per esperimenti che richiedevano la combinazione di più colori contemporaneamente.
Costruire guardiani verdi e rossi più luminosi
Gli autori hanno progettato indicatori verdi e rossi migliorati, chiamati nLightG2 e nLightR2, combinando frammenti di sensori precedenti per dopamina e norepinefrina e testando sistematicamente dozzine di mutazioni. Queste modifiche hanno reso i sensori molto più luminosi in presenza di norepinefrina, senza alterare molto la loro luminosità di base. In colture cellulari, i nuovi strumenti hanno mostrato risposte più ampie di diversi ordini di grandezza rispetto alle versioni precedenti, hanno reagito entro decine di millisecondi e si sono resettati in meno di un secondo. Rispondevano anche pochissimo ad altri neurotrasmettitori, come la dopamina, e non attivavano le vie di segnalazione interne delle cellule, un controllo di sicurezza importante per garantire che siano osservatori e non partecipanti.
Dimostrarne l’efficacia nel tessuto cerebrale
Successivamente, il team ha introdotto i sensori in fette di cervello di topo e ha usato la microscopia two-photon, che può penetrare in profondità nel tessuto, per confrontare i design vecchi e nuovi. Quando la norepinefrina veniva spruzzata sul tessuto, o quando le fibre locali erano stimolate elettricamente per rilasciarla in modo naturale, nLightG2 e nLightR2 producevano lampi molto più grandi e facilmente rilevabili rispetto ai sensori precedenti. Gli strumenti verde e rosso mostravano una velocità simile, il che significa che la scelta del colore non comporta più un compromesso sulla rapidità. Questa maggiore sensibilità ha permesso ai ricercatori di mappare dove la norepinefrina si diffondeva nello spazio, invece di limitarsi a sapere che era stata rilasciata da qualche parte nel campo visivo.
Osservare stati cerebrali, paura e navigazione in azione
La vera promessa di questi strumenti risiede negli animali viventi. Utilizzando fibre ottiche sottilissime, gli autori hanno combinato l’indicatore rosso per la norepinefrina con un sensore verde per il calcio che segnala l’attività neuronale. Nel centro del sonno del cervello, hanno osservato che scoppi di attività nelle cellule produttrici di norepinefrina durante il sonno profondo erano seguiti da aumenti locali di norepinefrina, evento dopo evento. Nell’amigdala, una regione cerebrale importante per le emozioni, il sensore verde per la norepinefrina ha rivelato che un tono innocuo cominciava a provocare un aumento sostenuto di norepinefrina una volta associato a una lieve scossa, rispecchiando il rafforzamento della memoria della paura. Nell’ippocampo, che aiuta a mappare lo spazio, il sensore rosso è stato immaginato insieme a un sensore di calcio verde per gli astrociti mentre i topi correvano attraverso un corridoio virtuale per ricevere ricompense d’acqua. Qui, l’attività degli astrociti vicino a un sito di ricompensa era strettamente collegata a picchi locali di norepinefrina, suggerendo un dialogo tra questo neuromodulatore e le cellule di supporto durante esperienze gratificanti.
Rivelare minuscole sacche di attività nella corteccia visiva
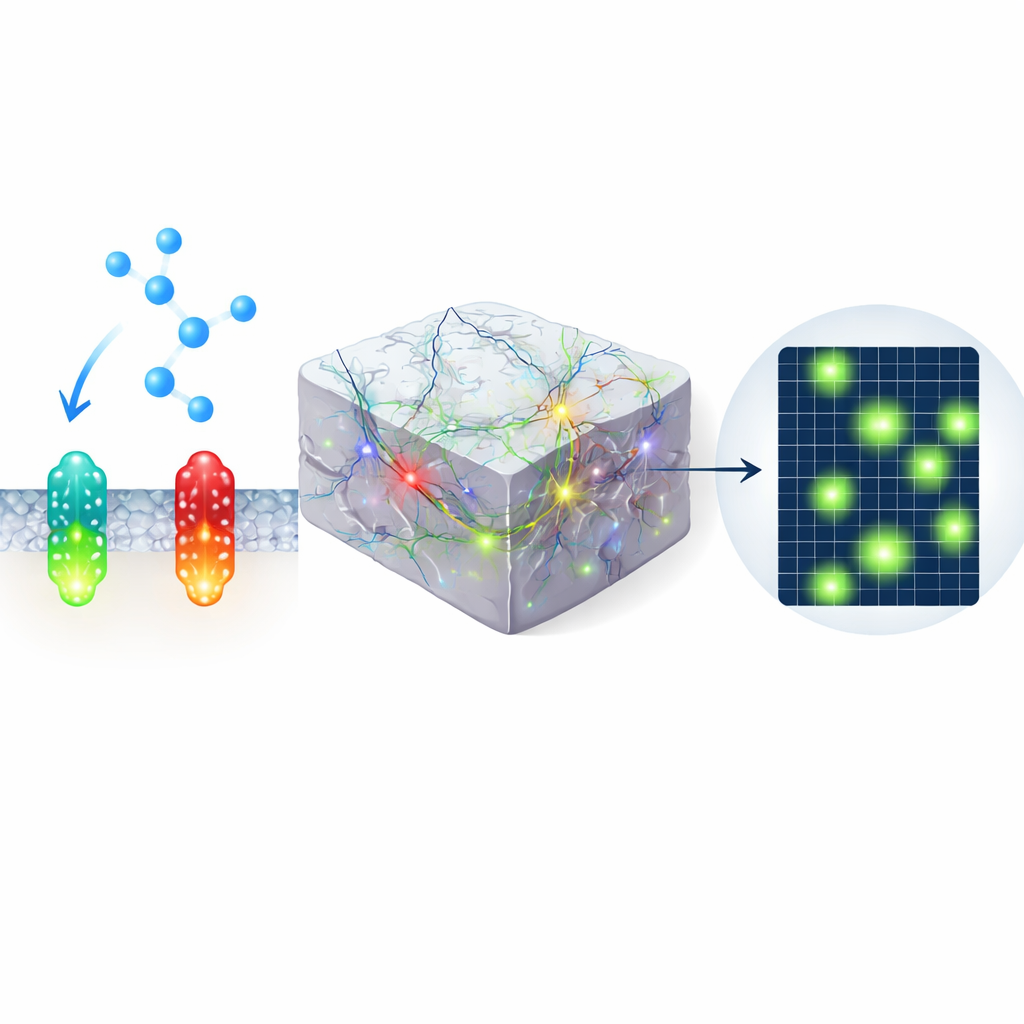
In un altro insieme di esperimenti, gli autori hanno espresso il sensore verde nella corteccia visiva di topi svegli e lo hanno immaginato con microscopia two-photon mentre gli animali osservavano stimoli in avvicinamento e alternavano riposo e corsa. Invece di un segnale uniforme, hanno trovato brevi patch altamente localizzate di aumento della fluorescenza—microdomini—sparse nel campo visivo. Alcuni microdomini rispondevano preferenzialmente alla minaccia visiva, altri al movimento, e molti si accendevano spontaneamente. Questi pattern erano in gran parte invisibili usando un sensore verde più vecchio o un controllo mutato non legante, sottolineando la sensibilità migliorata di nLightG2 e suggerendo che la norepinefrina modella l’attività cerebrale in modo molto più fine di quanto si pensasse prima.
Cosa significa per la ricerca cerebrale
Complessivamente, questi risultati mostrano che nLightG2 e nLightR2 costituiscono un potente kit per osservare la norepinefrina nel cervello vivente, su scale che vanno dai singoli microdomini a interi stati comportamentali. Poiché sono disponibili in colori distinti e possono essere combinati con altri reporter fluorescenti, gli scienziati possono ora tracciare la norepinefrina insieme a segnali elettrici o di calcio in tipi cellulari specifici, durante il sonno, l’apprendimento o lo stress. Questa capacità di vedere quando e dove agisce questo neuromodulatore chiave potrebbe alla fine chiarire come supporti attenzione e memoria sane e come la sua alterazione contribuisca a condizioni quali ansia, depressione e malattie neurodegenerative.
Citazione: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
Parole chiave: norepinefrina, neuromodulazione, sonde codificate geneticamente, imaging two-photon, sonno e apprendimento