Clear Sky Science · it
Distribuzione di massa di azitromicina e resistenza agli antibiotici nell’intestino e nel rinofaringe: uno studio randomizzato per cluster
Perché una singola compressa data a molti bambini conta
In alcune aree dell’Africa occidentale, un unico antibiotico, l’azitromicina, è stato impiegato in campagne di massa per ridurre il numero di giovani bambini che muoiono per infezioni. La strategia funziona, ma solleva una preoccupazione importante: stiamo silenziosamente selezionando microbi più resistenti nei corpi dei bambini? Questo studio, svolto in centinaia di villaggi in Niger, esamina da vicino l’interno degli intestini e dei nasi dei bambini per capire come trattamenti ripetuti a livello comunitario rimodellino il loro mondo microbico nascosto e la resistenza agli antibiotici.
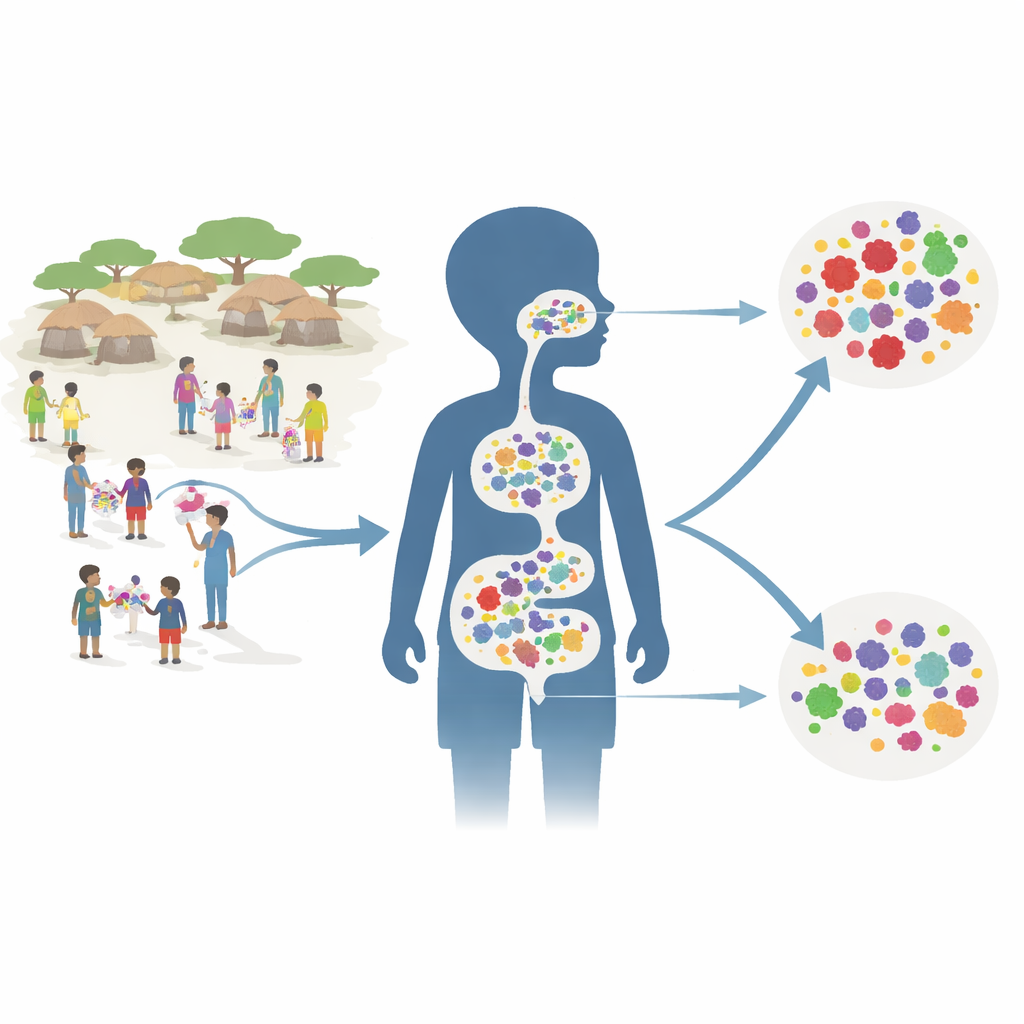
Valutare un piano terapeutico a livello comunitario
I ricercatori hanno inserito il loro lavoro all’interno di un grande trial chiamato AVENIR, che aveva già mostrato che somministrare azitromicina ogni sei mesi a tutti i bambini da 1 a 59 mesi poteva ridurre la mortalità in questa fascia d’età. Per lo studio sulla resistenza, si sono concentrati su 150 villaggi scelti casualmente. Ogni villaggio apparteneva a uno dei tre gruppi: tutti i bambini piccoli ricevevano azitromicina; solo i lattanti fino a 11 mesi ricevevano azitromicina mentre i bambini più grandi ricevevano placebo; oppure tutti i bambini ricevevano placebo. A due anni dall’avvio del programma—sei mesi dopo il quarto ciclo di trattamento—il team ha raccolto tamponi rettali e nasali profondi da circa 30 bambini per villaggio.
Una finestra su intestino e naso
Invece di far crescere i germi in coltura, gli scienziati hanno poolato i campioni per ciascun villaggio e usato moderne tecniche di sequenziamento del DNA. Questo ha consentito loro di catalogare quali batteri erano presenti e contare i marcatori genetici che segnalano la resistenza a diverse famiglie di antibiotici. Hanno prestato particolare attenzione ai macrolidi—the famiglia di farmaci a cui appartiene l’azitromicina—esaminando al contempo la resistenza a molti altri tipi di antibiotici largamente usati, come i beta-lattamici. Sono stati analizzati l’intestino e il rinofaringe (la parte superiore della gola dietro il naso) perché entrambi sono importanti serbatoi dove i geni di resistenza possono accumularsi e potenzialmente diffondersi.
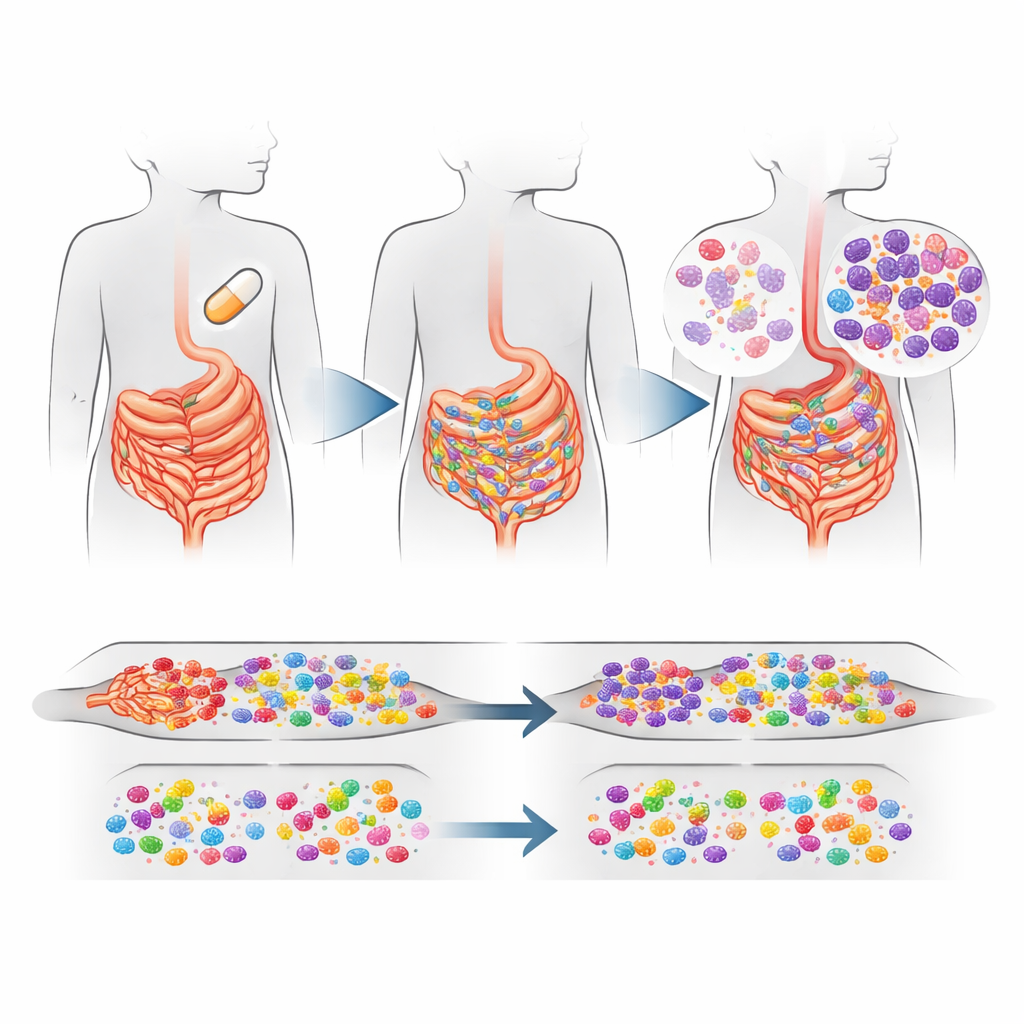
Cosa è cambiato nell’intestino dei bambini
Il segnale più netto è venuto dall’intestino. Nei villaggi in cui tutti i bambini hanno ricevuto azitromicina si è osservato un aumento modesto ma statisticamente significativo—circa il 16% in più complessivamente—dei geni di resistenza ai macrolidi nei batteri intestinali rispetto ai villaggi trattati con placebo. L’aumento è stato trainato in larga misura da un singolo gene di resistenza, chiamato ermF, che aiuta a proteggere i batteri dai macrolidi. Questo gene è spesso portato da comuni batteri intestinali come Bacteroides e Prevotella, che normalmente vivono in modo innocuo nell’intestino ma possono talvolta causare malattie. È interessante notare che i geni di resistenza contro altre importanti famiglie di antibiotici non sono aumentati, e la composizione e la diversità complessiva dei batteri intestinali è risultata in larga misura simile tra i gruppi di trattamento, anche se alcune specie specifiche sono diventate più o meno comuni.
Cosa è rimasto invariato nel naso
Al contrario, le vie nasali hanno raccontato una storia più tranquilla. Lo studio non ha trovato differenze chiare e statisticamente solide nei geni di resistenza ai macrolidi tra i gruppi di trattamento nel rinofaringe, né prove che si stesse selezionando resistenza ad altre classi di antibiotici in quella sede. I tipici residenti nasali—generi come Moraxella, Haemophilus e Streptococcus—sono rimasti dominanti. Alcuni batteri legati alla cavità orale associati a malattie gengivali sono diventati più comuni nelle comunità trattate con azitromicina, e alcuni di questi possono anch’essi portare geni di resistenza, ma il carico complessivo di resistenza nel naso non ha subito la stessa variazione osservata nell’intestino.
Bilanciare i guadagni di oggi con i rischi di domani
Nel complesso, i risultati mostrano che somministrare azitromicina a tutti i bambini piccoli di una comunità può salvare vite, ma spinge anche i batteri intestinali verso una maggiore resistenza a questa famiglia di farmaci, principalmente attraverso l’espansione di specifici geni di resistenza come ermF. Lo studio non ha riscontrato, nel periodo di due anni, una ricaduta sulla resistenza ad altre classi di antibiotici né forti cambiamenti nel serbatoio nasale, ma gli autori avvertono che i batteri resistenti intestinali e i loro geni possono diffondersi nel tempo e tra le persone. Sostengono che qualsiasi programma antibiotico esteso per la sopravvivenza infantile dovrebbe includere un monitoraggio accurato e a lungo termine della resistenza, in modo che i responsabili sanitari possano continuare a bilanciare il beneficio immediato di meno morti infantili con il costo più lento e meno visibile di un rafforzamento dei microrganismi resistenti ai farmaci.
Citazione: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Parole chiave: azitromicina, mortalità infantile, resistenza agli antibiotici, microbioma intestinale, somministrazione di massa di farmaci