Clear Sky Science · it
Fuga antigenica multimodale agli engager delle cellule T mirati su GPRC5D nel mieloma multiplo
Quando il cancro supera l’immunoterapia di precisione
Nuovi farmaci immunologici potenti stanno trasformando il trattamento del mieloma multiplo, un tumore del sangue che resta incurabile per la maggior parte dei pazienti. Queste terapie funzionano rimandando le cellule T del corpo a cercare e distruggere le cellule tumorali contrassegnate da specifici “segnali” sulla loro superficie. Un segnale promettente è una molecola chiamata GPRC5D. Tuttavia, come spesso accade con le terapie mirate, i tumori possono evolvere e sfuggire al trattamento. Questo studio scioglie, in dettagli insoliti, come le cellule del mieloma modificano o nascondono il segnale GPRC5D per eludere farmaci molto efficaci che coinvolgono le cellule T.
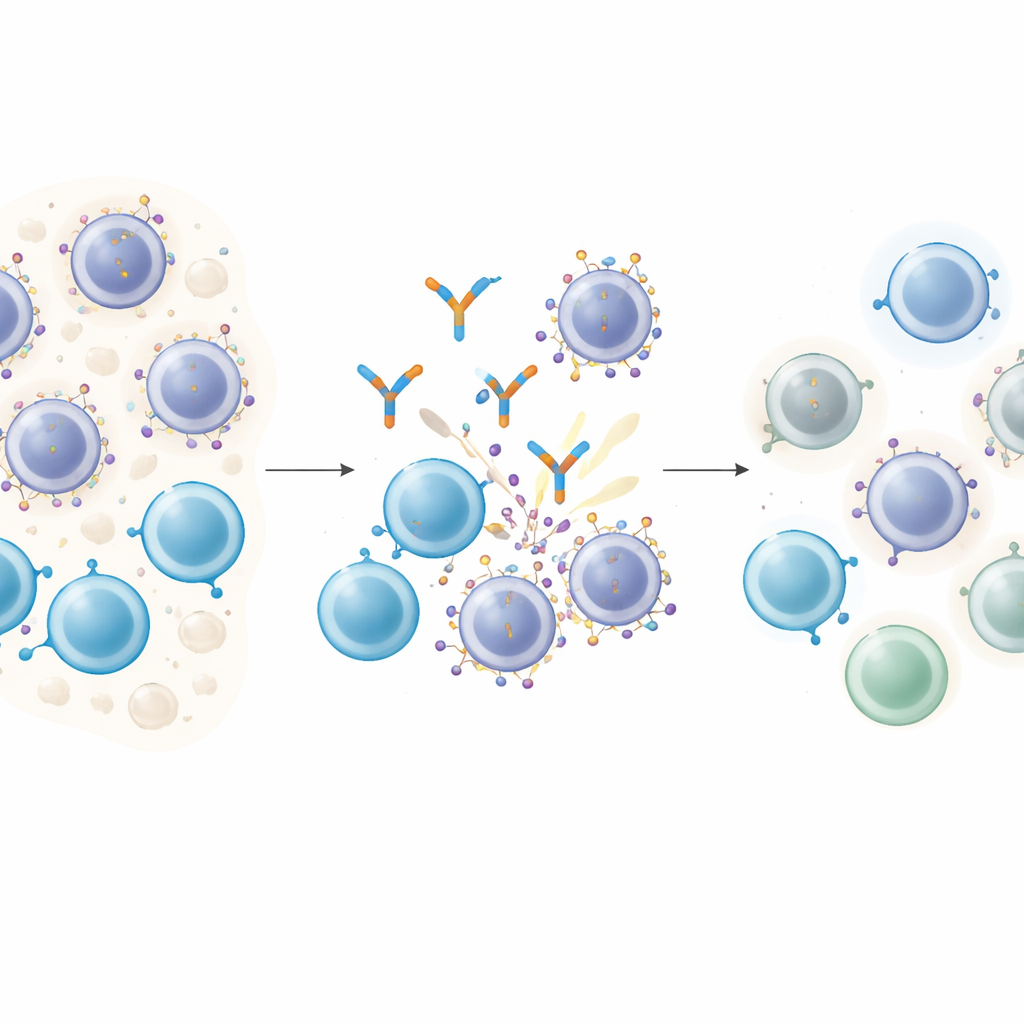
Come i farmaci intelligenti si agganciano alle cellule tumorali
Gli anticorpi che coinvolgono le cellule T funzionano come abbinatori molecolari: un’estremità afferra una cellula T, l’altra si ancora a una molecola bersaglio sulla cellula tumorale, avvicinando le due in modo che la cellula T possa uccidere la sua preda. Nel mieloma multiplo, GPRC5D è un bersaglio attraente perché è abbondante sulle plasmacellule maligne ma raro nella maggior parte dei tessuti normali. I pazienti trattati con un farmaco diretto contro GPRC5D chiamato talquetamab spesso sperimentano remissioni profonde. Tuttavia, quasi tutti ricadono col tempo, sollevando una domanda cruciale: le cellule tumorali stanno cambiando proprio il bersaglio su cui questi farmaci fanno affidamento?
Monitorare l’evoluzione tumorale in tempo reale
I ricercatori hanno seguito 21 persone con mieloma difficile da trattare che hanno ricevuto talquetamab. Hanno raccolto campioni di midollo osseo prima del trattamento in alcuni pazienti e di nuovo alla ricaduta, quindi hanno usato più livelli di analisi di DNA, RNA e cromatina per esaminare le cellule tumorali. Questa vista ultra‑dettagliata ha rivelato che, in circa due terzi dei pazienti in recidiva, il cancro aveva alterato GPRC5D in modi che avrebbero attenuato o bloccato l’effetto del farmaco. In modo sorprendente, diversi sottoclonI resistenti — rami geneticamente distinti del tumore — spesso coesistevano nella stessa persona, mostrando che l’evoluzione verso l’evasione può seguire più percorsi contemporaneamente.
Tre modalità principali con cui i tumori nascondono il bersaglio
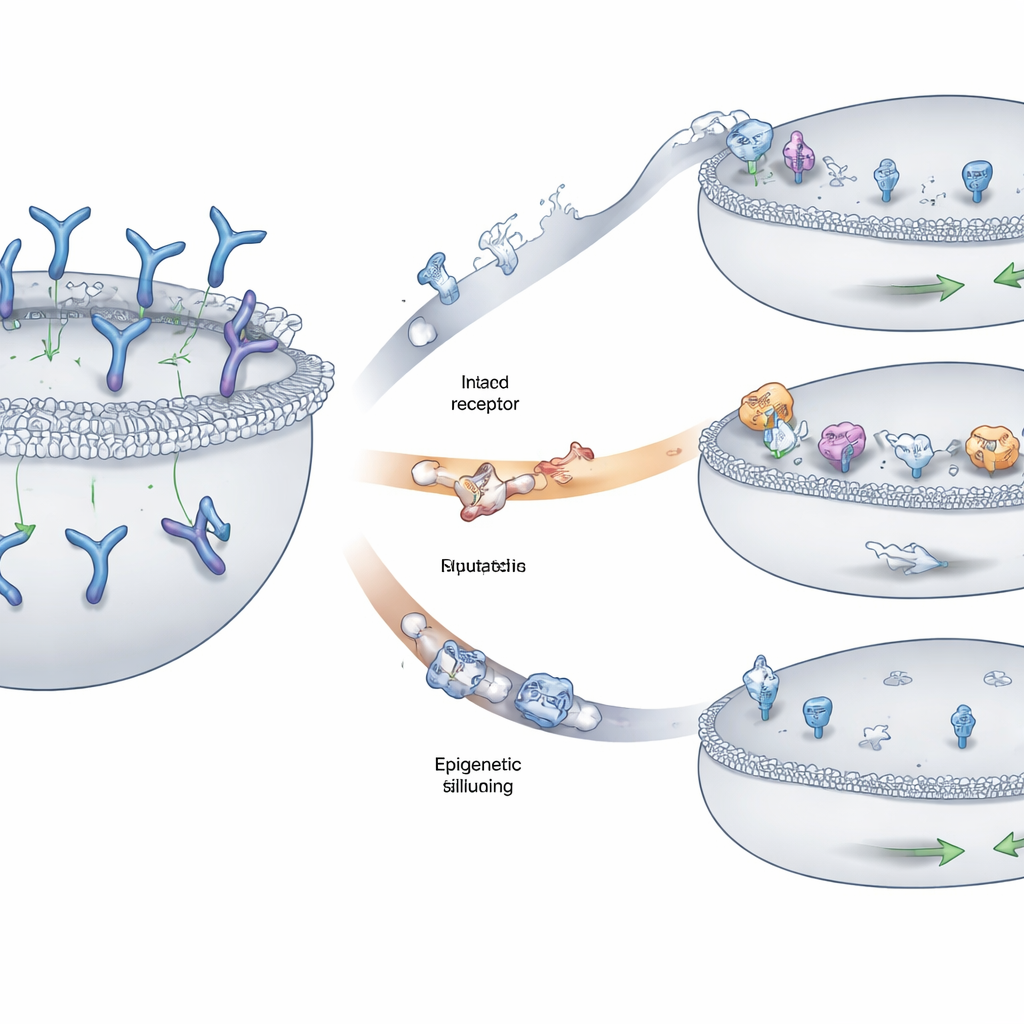
Il team ha individuato tre schemi ricorrenti con cui le cellule del mieloma sfuggivano al riconoscimento. In alcuni pazienti, sono state eliminate parti del cromosoma che portano il gene GPRC5D su entrambe le copie, cancellando completamente il segnale dalla superficie cellulare. In altri, cambiamenti più piccoli — sostituzioni di singole basi o piccole inserzioni e delezioni — alteravano regioni chiave della proteina GPRC5D. Molte di queste variazioni interrompevano parti della proteina necessarie per transitare correttamente dall’interno della cellula alla membrana esterna, causando il blocco di GPRC5D in compartimenti interni anziché la sua esposizione dove il farmaco potesse vederla. Una terza via riguardava il silenziamento epigenetico: il DNA intorno a GPRC5D veniva compattato e chimicamente modificato in modo che il gene fosse scarsamente trascritto, anche se la sequenza sottostante rimaneva in gran parte intatta. Le cellule tumorali che adottavano questa strategia producevano pochissimo o nessun GPRC5D.
Quando il segnale è presente ma la chiave non combacia più
Non tutte le vie di fuga rimuovevano GPRC5D dalla superficie cellulare. In alcuni casi la proteina appariva normale ai test di laboratorio standard ma non si adattava più al farmaco come una chiave nella serratura. Il team ha ricreato mutazioni specifiche derivate da pazienti in linee cellulari di laboratorio e ha testato quanto bene diversi anticorpi diretti contro GPRC5D riuscissero a legarsi e uccidere queste cellule. Una mutazione ha alterato sottilmente il punto esatto in cui talquetamab aggrappa il recettore, riducendo fortemente la capacità del farmaco di legarsi e di innescare la morte cellulare, anche se il recettore risultava ancora visibile con la colorazione di routine. È interessante che un diverso farmaco diretto contro GPRC5D che si ancora al recettore in due siti sia rimasto efficace contro diversi di questi mutanti, evidenziando come il design del farmaco — ad esempio l’uso di legami multivalenti o multi‑epitopo — possa influenzare se i cloni resistenti sopravvivono.
Oltre il bersaglio: altri limiti all’attacco immunitario
Sebbene la maggior parte delle recidive mostrasse qualche forma di perdita o alterazione di GPRC5D, una minoranza di pazienti recidivò senza cambiamenti evidenti nel bersaglio stesso. In questi casi, il problema sembrava risiedere nelle cellule T: erano meno efficienti e meno capaci di uccidere le cellule tumorali nei test di laboratorio, suggerendo che l’esposizione continua a lungo termine alla terapia engager possa esaurire il sistema immunitario. Lo studio ha inoltre scoperto che un sottotipo genetico particolare di mieloma (che coinvolge uno scambio cromosomico chiamato t(11;14)) mantiene naturalmente il gene GPRC5D in uno stato cromatinico più “chiuso”, con espressione basale inferiore. Ciò solleva la possibilità che alcuni pazienti possano essere predisposti a risposte scarse perché i loro tumori partono già con livelli attenuati del segnale bersaglio.
Cosa significa per i pazienti e per i trattamenti futuri
Per pazienti e clinici, questo lavoro spiega perché anche terapie mirate su GPRC5D altamente potenti non sono ancora cure: le cellule del mieloma possono cancellare, rimescolare, deviare o spegnere il segnale su cui questi farmaci fanno affidamento, e spesso lo fanno in più modi contemporaneamente. I risultati suggeriscono che monitorare il DNA tumorale, piuttosto che misurare solo i livelli proteici, sarà importante per rilevare mutazioni di fuga emergenti che i test di laboratorio standard possono mancare. Indicano inoltre strategie di prossima generazione — come farmaci che si legano a GPRC5D con maggiore avidità in più siti, combinazioni che colpiscono più bersagli contemporaneamente, o agenti che riaprono geni silenziati — per restare avanti rispetto all’evoluzione tumorale. In sostanza, questo studio mappa le vie di fuga utilizzate dal mieloma affinché terapie future possano essere progettate per bloccarle, mantenendo i trattamenti basati sulle cellule T efficaci più a lungo.
Citazione: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Parole chiave: mieloma multiplo, engager delle cellule T, GPRC5D, fuga antigenica, immunoterapia oncologica