Clear Sky Science · it
Linavonkibart e pembrolizumab nei tumori solidi avanzati resistenti al blocco degli immune checkpoint: uno studio di fase 1
Perché i tumori ostinati ci riguardano tutti
I farmaci immunoterapici che «rimuovono i freni» al sistema immunitario hanno cambiato il trattamento di molti tumori, ma la maggior parte dei pazienti o non trae mai beneficio oppure vede alla fine la ricomparsa della crescita tumorale. Questo studio testa un nuovo anticorpo terapeutico, linavonkibart, progettato per disattivare un potente scudo che i tumori usano per nascondersi dall’attacco immunitario, combinandolo con un’immunoterapia già approvata, il pembrolizumab. I risultati offrono un primo segnale che, anche in pazienti i cui tumori avevano già smesso di rispondere ai farmaci checkpoint, potrebbe essere possibile ristabilire il controllo immunitario mantenendo sotto controllo gli effetti collaterali.
Uno scudo nascosto attorno ai tumori
Molti farmaci immunoterapici moderni agiscono bloccando le cosiddette molecole checkpoint, come PD‑1, che normalmente limitano l’attività delle cellule T. Quando questi freni vengono rilasciati, le cellule immunitarie possono attaccare il cancro in modo più intenso. Tuttavia i tumori spesso si adattano costruendo un microambiente ostile che tiene lontane le cellule T citotossiche o le indebolisce una volta arrivate. Un architetto chiave di questa bolla protettiva è una proteina di segnalazione chiamata TGFβ1, prodotta sia dalle cellule tumorali sia dalle cellule di supporto circostanti. Tentativi precedenti di bloccare l’intera famiglia del TGFβ avevano mostrato potenziale ma avevano incontrato gravi problemi cardiaci e emorragici, perché altri membri della famiglia sono importanti per i tessuti sani. Linavonkibart è stato ingegnerizzato per centrare questo obiettivo neutralizzando selettivamente solo la forma latente e inattiva di TGFβ1 prima che venga attivata, lasciando intatte le molecole strettamente correlate di cui il corpo ha bisogno.
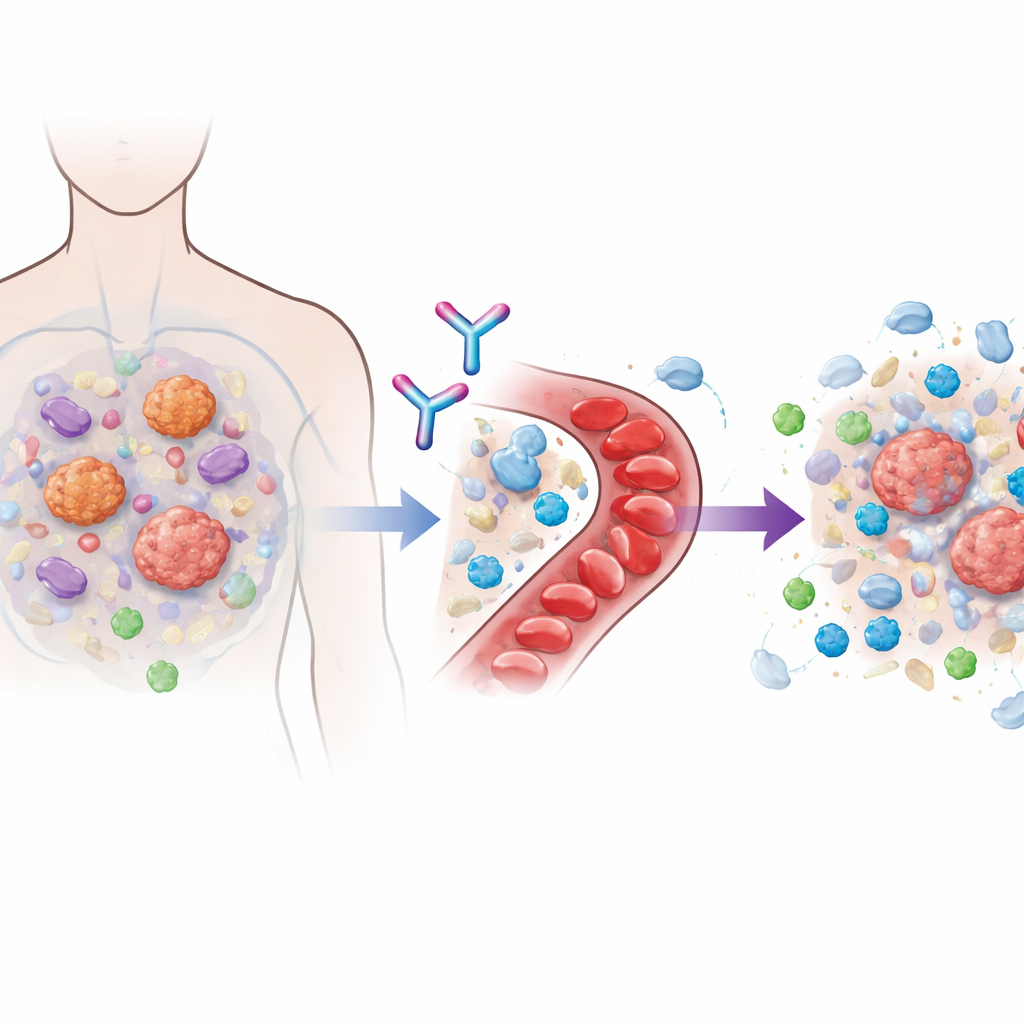
Progettare un primo test umano con cautela
Lo studio DRAGON è stato uno studio multicentrico di fase 1 condotto in 22 ospedali negli Stati Uniti e in Corea del Sud. Ha arruolato 112 adulti con tumori solidi avanzati, tutti con opzioni terapeutiche limitate. Nella prima parte dello studio, linavonkibart è stato somministrato da solo a dosi gradualmente crescenti a piccoli gruppi di pazienti, oppure in combinazione con il loro precedente farmaco a base di PD‑1. Questo approccio graduale è servito a mappare la sicurezza, la farmacocinetica e la farmacodinamica del farmaco e a scegliere una dose per i test più ampi. Nella seconda parte, 78 pazienti i cui tumori avevano già resistito ad almeno un ciclo di immunoterapia anti‑PD‑1 hanno ricevuto una dose fissa di linavonkibart insieme a pembrolizumab. Questi pazienti avevano tumori difficili da trattare, inclusi carcinoma renale a cellule chiare, melanoma, tumori della testa e del collo, carcinoma uroteliale (vescicale) e tumori polmonari, e la maggior parte aveva già ricevuto diversi trattamenti precedenti.
Sicurezza prima di tutto: cosa è successo ai pazienti
L’obiettivo principale di questo studio in fase iniziale era la sicurezza, e linavonkibart ha dato segnali incoraggianti su questo fronte. A tutti i livelli di dose non è stata raggiunta una dose massima tollerata, e non sono stati osservati eventi avversi dose‑limitanti o fatali attribuibili al farmaco. Quando linavonkibart è stato combinato con pembrolizumab alla dose di fase 2, circa tre quarti dei pazienti ha sperimentato qualche effetto collaterale correlato al trattamento, simile a quanto spesso si osserva con l’immunoterapia da sola. Eruzioni cutanee e prurito sono stati i problemi aggiuntivi più frequenti, e un piccolo numero di pazienti ha sviluppato infiammazione cutanea o polmonare più grave. È importante notare che la pericolosa reazione immunitaria nota come sindrome da rilascio di citochine, che può verificarsi con alcuni anticorpi terapeutici, non è stata osservata, e il profilo complessivo di sicurezza somigliava in larga misura a quello del solo pembrolizumab.
Indizi che il sistema immunitario può essere ri‑risvegliato
Sebbene non si trattasse di uno studio di efficacia ampio e definitivo, diversi segnali suggeriscono che bloccare TGFβ1 potrebbe aiutare a riaccendere le risposte al blocco di PD‑1. Nella fase di espansione, la combinazione linavonkibart–pembrolizumab ha ridotto tumori misurabili in una quota rilevante di pazienti che in precedenza avevano smesso di beneficiare dei farmaci anti‑PD‑1. I tassi di risposta confermata sono stati del 20% nel carcinoma renale a cellule chiare, 18,2% nel melanoma e poco oltre il 9% nei tumori della testa e del collo e nei carcinomi uroteliali, con un paziente affetto da carcinoma renale che ha ottenuto una scomparsa completa della malattia visibile. Molte di queste risposte sono durate per mesi, e i pazienti che hanno risposto sono rimasti generalmente in trattamento con la combinazione molto più a lungo rispetto alla loro precedente terapia anti‑PD‑1. Le biopsie prelevate prima e dopo il trattamento offrono una spiegazione biologica: i tumori mostravano una maggiore infiltrazione di cellule CD8 «killer», livelli più alti di cellule T attivate, meno cellule regolatorie immunosoppressive e cellule mieloidi, e uno spostamento complessivo verso un microambiente più infiammato e pronto all’attacco.
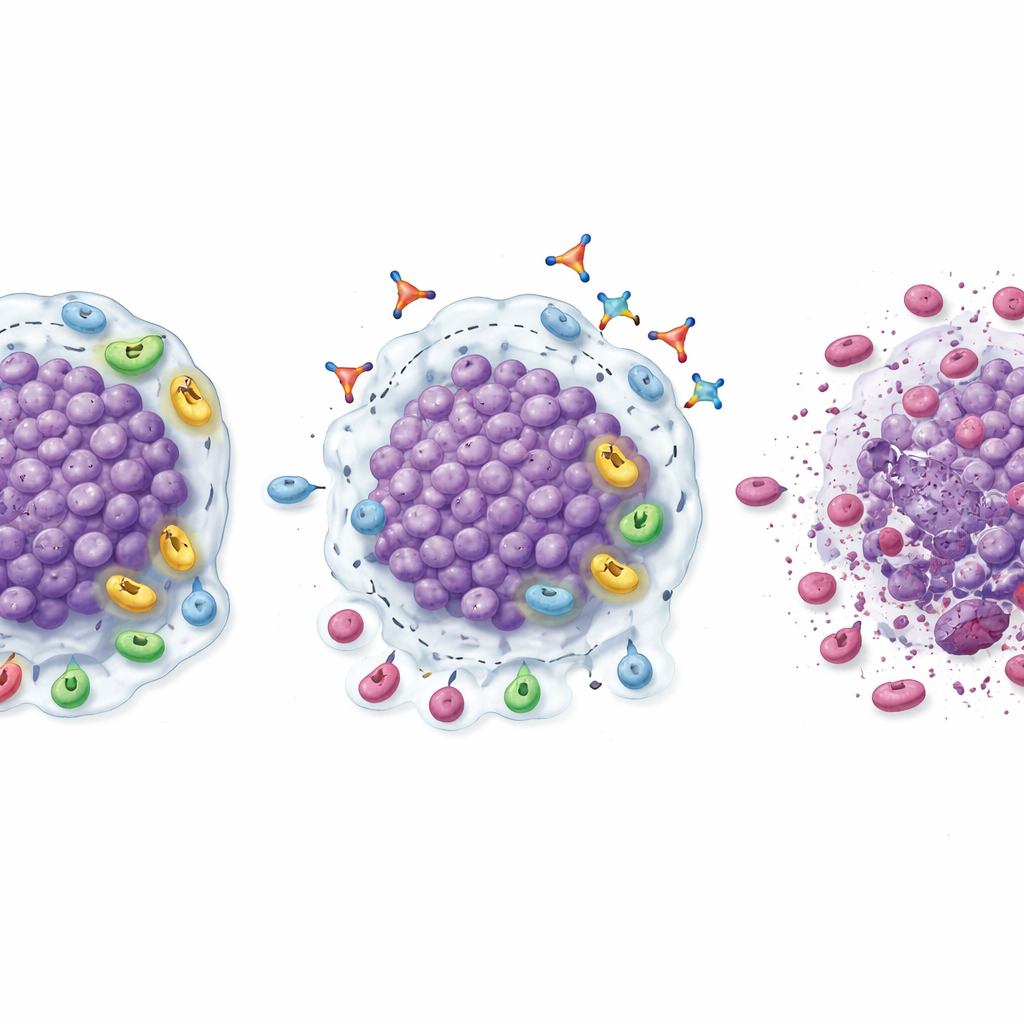
Individuare chi potrebbe beneficiare di più
I ricercatori hanno anche esplorato quali pazienti potrebbero essere particolarmente predisposti a rispondere. Nel carcinoma renale a cellule chiare, i tumori che già contenevano numerose cellule CD8 al basale—ma erano anche ricchi di cellule T regolatorie ed esprimevano alti livelli di TGFβ1—avevano maggiori probabilità di ridursi con la terapia combinata. In questi pazienti, i tassi di risposta e la sopravvivenza libera da progressione sono stati significativamente più elevati rispetto al gruppo renale più ampio. Questo schema suggerisce un «punto ideale»: i tumori che hanno molti soldati immunitari presenti ma sono tenuti sotto controllo dalla soppressione mediata da TGFβ1 potrebbero essere candidati ideali per linavonkibart più blocco di PD‑1. Se validato in studi più ampi, test tissutali semplici per questi marcatori potrebbero aiutare i medici a selezionare i pazienti con maggior probabilità di trarre beneficio.
Cosa significa questo lavoro per il futuro
Per le persone con tumori avanzati che hanno già resistito all’immunoterapia, la prospettiva di rimettere in moto il proprio sistema immunitario senza aggiungere una tossicità severa è allettante. Questo primo studio in umano fornisce prove iniziali che disabilitare selettivamente lo scudo TGFβ1 con linavonkibart può essere fatto in sicurezza e può ripristinare un controllo tumorale significativo se abbinato a un inibitore di PD‑1, in particolare in alcuni tumori renali. Sebbene lo studio fosse di piccole dimensioni e non randomizzato, il profilo di sicurezza, i riscontri biologici e le risposte durature insieme costituiscono un forte argomento a favore di studi di fase 2 più ampi. Se studi futuri confermeranno questi risultati, questo approccio potrebbe ampliare il numero di pazienti che possono beneficiare dell’immunoterapia, trasformando alcuni tumori oggi ostinati in tumori nuovamente vulnerabili alle difese dell’organismo.
Citazione: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Parole chiave: immunoterapia oncologica, inibizione del TGFβ1, resistenza agli immune checkpoint, carcinoma renale a cellule chiare, microambiente tumorale