Clear Sky Science · it
Abemaciclib nei meningiomi con alterazioni somatiche di NF2 o della via CDK: lo studio di fase 2 Alliance A071401
Perché questo studio sui tumori cerebrali è importante
I meningiomi sono i tumori cerebrali primari più comuni. Molte persone ottengono buoni risultati dopo chirurgia e radioterapia, ma per chi ha tumori che continuano a recidivare o a crescere, i farmaci efficaci sono pochi. Questo studio ha verificato se un farmaco già usato in oncologia, l’abemaciclib, potesse rallentare la crescita di meningiomi aggressivi che presentano specifiche alterazioni genetiche, offrendo nuova speranza dove le opzioni sono scarse.
Uno sguardo più attento ai tumori cerebrali ostinati
La maggior parte dei meningiomi cresce lentamente e può spesso essere controllata con intervento chirurgico e, se necessario, radioterapia. Tuttavia, i tumori di grado più elevato (grado 2 e 3) sono più aggressivi e più propensi a recidivare. Storicamente, i trattamenti farmacologici per questi tumori recidivanti hanno avuto successo limitato. Nell’ultimo decennio gli scienziati hanno mappato le alterazioni del DNA che guidano i meningiomi e hanno scoperto che alcuni tumori presentano modifiche in geni come NF2 e in quelli che regolano il ciclo cellulare, il meccanismo che indica alle cellule quando dividersi. Queste scoperte hanno aperto la strada a testare farmaci che prendono di mira specificamente queste vie alterate.
Progettare uno studio farmacologico guidato dal genotipo
I ricercatori hanno avviato uno studio nazionale di medicina di precisione chiamato Alliance A071401 per assegnare i pazienti con meningiomi recidivanti o progressivi a farmaci mirati in base al profilo genetico dei loro tumori. Un braccio di questo studio si è concentrato sull’abemaciclib, un farmaco orale che inibisce due proteine chiave del ciclo cellulare chiamate CDK4 e CDK6. I pazienti potevano partecipare a questo braccio se avevano meningiomi di grado 2 o 3 con mutazioni di NF2 o alterazioni della via CDK. Tutti i partecipanti avevano già subito interventi chirurgici, quasi tutti avevano ricevuto radioterapia e molti avevano provato altre terapie sistemiche. L’abemaciclib è stato assunto due volte al giorno in cicli di 28 giorni e continuato fino a chiara progressione del tumore o fino a quando gli effetti collaterali non diventavano inaccettabili.
Quanto è efficace il trattamento?
Il principale parametro di successo era la quota di pazienti vivi e liberi da progressione della malattia sei mesi dopo l’inizio dell’abemaciclib. Tra i primi 24 pazienti eligibili analizzati, 14 (58%) hanno raggiunto questo traguardo, superando con comodità la soglia predefinita di otto pazienti che avrebbe indicato un’attività promettente. La migliore risposta complessiva è stata “malattia stabile” in due terzi di questi pazienti; nessuno ha mostrato una riduzione evidente dei tumori, ma impedire la crescita di tumori aggressivi è clinicamente rilevante in un contesto in cui tendono a peggiorare nonostante il trattamento. Quando sono stati considerati tutti i 35 pazienti valutabili, il tempo mediano alla progressione variava da 7,6 a 10,1 mesi, a seconda dell’analisi, e la sopravvivenza globale mediana era di circa 29 mesi. Le analisi genetiche hanno suggerito che i pazienti con tumori portatori di mutazioni NF2 tendevano a rimanere liberi da progressione più a lungo rispetto a quelli con sole alterazioni della via CDK, sebbene lo studio fosse troppo piccolo per trarre conclusioni definitive.
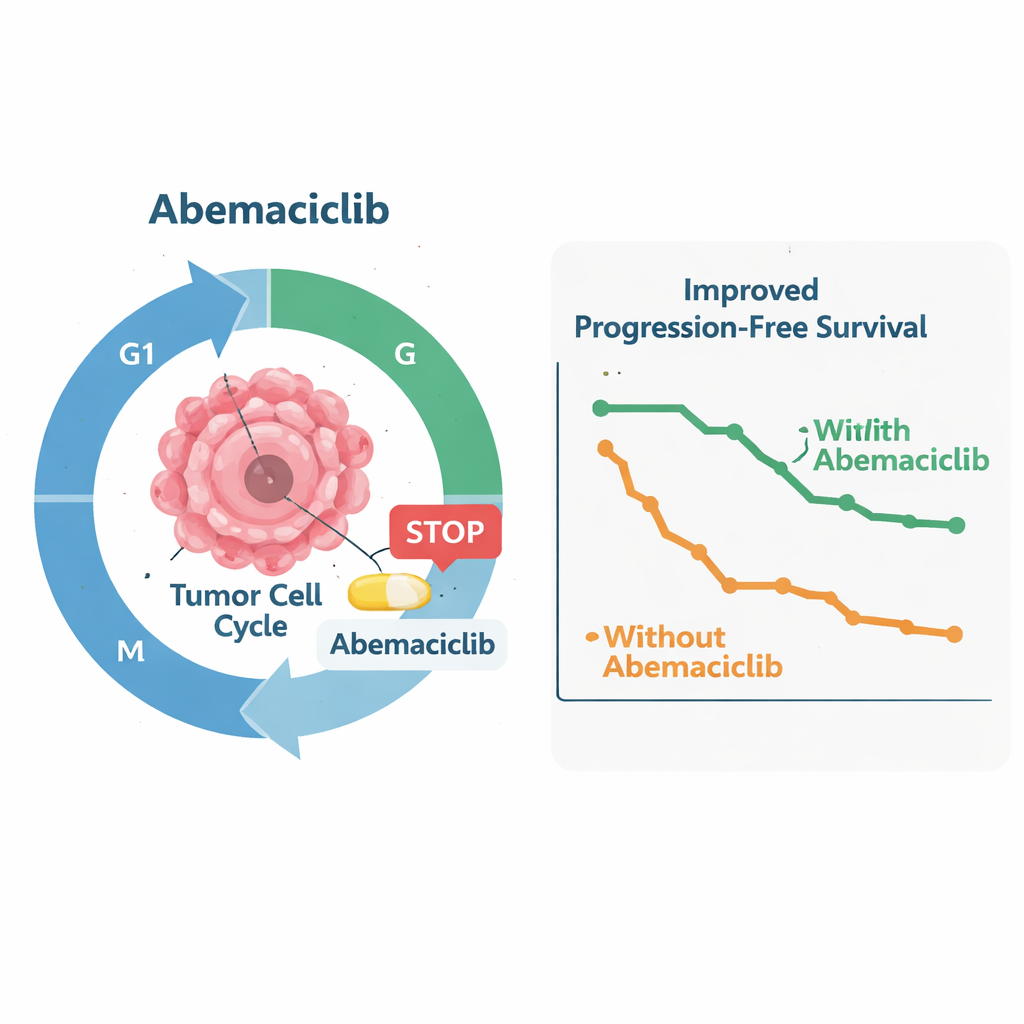
Effetti collaterali e sicurezza
Tutti i 36 pazienti che hanno iniziato l’abemaciclib sono stati monitorati per gli effetti collaterali. In media hanno ricevuto nove cicli di trattamento. Circa un terzo ha avuto ritardi in almeno un ciclo e sette hanno interrotto la terapia a causa di effetti avversi o complicazioni. Undici pazienti hanno presentato eventi severi (grado 3 o 4) probabilmente correlati al farmaco, tra cui riduzione delle cellule ematiche, diarrea, affaticamento, aumento delle transaminasi epatiche e, in un caso, vomito severo. Questi effetti collaterali sono stati simili a quelli osservati quando l’abemaciclib è impiegato per altri tumori, come il cancro al seno, e sono generalmente risultati gestibili con aggiustamenti di dose e cure di supporto.
Cosa significa per i pazienti
Questo trial non includeva un gruppo di confronto che ricevesse un altro farmaco standard, in parte perché non esiste un trattamento standard concordato una volta che chirurgia e radioterapia falliscono. I ricercatori hanno quindi confrontato i loro risultati con dati storici di studi precedenti su pazienti simili, che mostrano che solo circa un terzo rimane libero da progressione a sei mesi. In questo studio, il tasso di sopravvivenza libero da progressione a sei mesi del 58% risulta incoraggiante, soprattutto dato che molti tumori avevano già resistito a molteplici terapie. Sebbene l’abemaciclib raramente abbia ridotto le dimensioni dei tumori, la sua capacità di controllarne la crescita per molti mesi rappresenta un progresso significativo per pazienti con poche opzioni.
Un passo verso una cura più precisa dei tumori cerebrali
Per le persone con meningiomi aggressivi e resistenti ai trattamenti, questo studio offre un cauto motivo di ottimismo. Dimostra che associare i pazienti a farmaci in base alla genetica dei loro tumori è fattibile su scala nazionale e che l’abemaciclib può rallentare la progressione della malattia con un profilo di sicurezza gestibile in molti casi. Sebbene siano necessari studi più ampi e controllati, questi risultati supportano ulteriori sperimentazioni dell’abemaciclib—possibilmente in combinazione con altri trattamenti—e avvicinano il campo a una cura veramente personalizzata per i pazienti con meningiomi di alto grado.
Citazione: Brastianos, P.K., Dooley, K., Geyer, S. et al. Abemaciclib in meningiomas with somatic NF2 or CDK pathway alterations: the phase 2 Alliance A071401 trial. Nat Med 32, 717–724 (2026). https://doi.org/10.1038/s41591-025-04141-4
Parole chiave: meningioma, abemaciclib, tumore cerebrale, terapia mirata, studio clinico