Clear Sky Science · it
Paesaggio interpretabile dell'infiammazione nelle cellule immunitarie circolanti
Perché l'infiammazione nel sangue è importante per te
L'infiammazione è al centro di molte malattie, dall'artrite e l'asma fino a COVID-19 e cancro. Eppure i medici faticano ancora a interpretare i segnali infiammatori del corpo in modo da spiegare chiaramente cosa non va e quale trattamento funzionerà meglio. Questo studio costruisce una enorme “mappa” delle cellule immunitarie circolanti nel sangue e mostra come queste cellule possano funzionare da biomarcatori viventi e facilmente campionabili per classificare un'ampia gamma di malattie infiammatorie.
Costruire una mappa gigante delle cellule immunitarie
Per tracciare questo paesaggio, i ricercatori hanno analizzato più di 6,5 milioni di cellule immunitarie prelevate dal sangue di 1.047 persone. I volontari rappresentavano 19 condizioni, incluse malattie autoimmuni come lupus e artrite reumatoide, malattie polmonari croniche come asma e BPCO, infezioni quali COVID-19 e HIV, e diversi tumori, insieme a donatori sani. Utilizzando il sequenziamento dell'RNA a singola cellula, hanno misurato quali geni fossero attivati in ciascuna cellula, quindi hanno impiegato metodi statistici avanzati per correggere le differenze tecniche tra gli studi e raggruppare le cellule in 64 distinti stati immunitari. Questa “Atlante dell'Infiammazione” cattura sia protagonisti noti — come cellule T, cellule B e monociti — sia sottotipi più specializzati che cambiano con la malattia.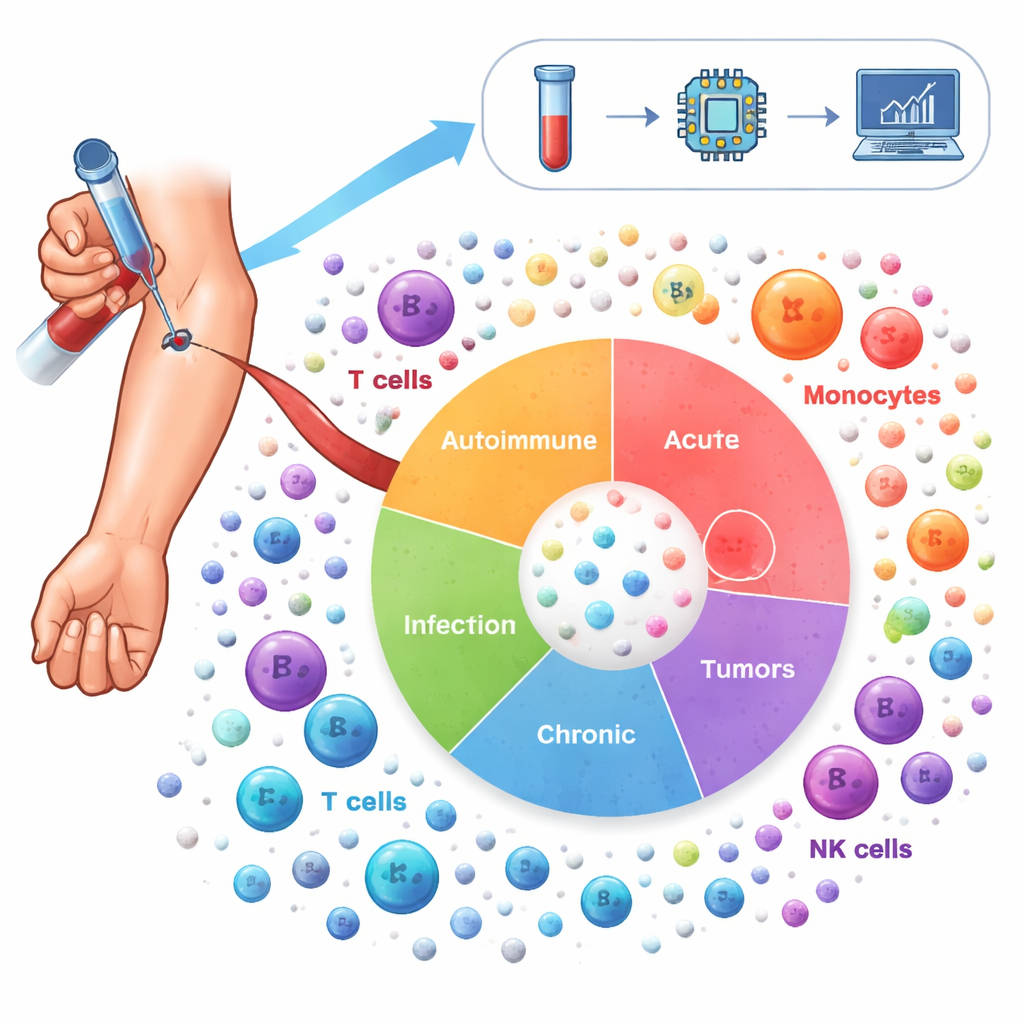
Leggere le firme infiammatorie del corpo
Il team si è poi concentrato sui geni che controllano come le cellule immunitarie si attivano, si muovono nell'organismo, presentano antigeni e rispondono a molecole di segnalazione come interferoni e fattore di necrosi tumorale. Hanno raggruppato questi geni in 21 “firme” biologiche e le hanno affinate per ciascun principale tipo cellulare. Confrontando i pazienti con i donatori sani, hanno potuto vedere quali firme erano aumentate o diminuite nelle diverse malattie. Per esempio, molte malattie infiammatorie a mediazione immunitaria mostravano maggiore attività di molecole di adesione e del macchinario di presentazione antigenica, mentre le risposte a interferone risultavano depresse nella maggior parte dei tipi cellulari ma intensificate in certi linfociti T CD8. Infezioni virali come l'influenza e COVID-19 potenziavano i programmi indotti da interferone, mentre infezioni croniche come HIV ed epatite B li indebolivano.
Approfondire geni chiave e interruttori di controllo
Poiché le firme ampie nascondono ancora dettagli importanti, i ricercatori hanno analizzato i singoli geni e i loro regolatori. Nei linfociti T CD8 non-naive hanno rilevato che due geni, FGFBP2 e GZMB, erano particolarmente attivi in specifici sottotipi di memoria effettrice, in particolare nella colite ulcerosa. Questi geni sono stati collegati a danni alle superfici epiteliali, e il loro forte segnale nel sangue suggerisce che queste cellule aggressive siano già predisposte prima di entrare nei tessuti. Un'analisi separata delle reti di regolazione genica ha evidenziato due fattori di trascrizione, STAT1 e SP1, come controllori centrali dei programmi indotti da interferone. I loro modelli di attività differivano tra malattie e tipi cellulari — per esempio, comportamento opposto in monociti rispetto ai linfociti T CD8 nel lupus, e cambiamenti tra fasi di riacutizzazione e fasi non attive — suggerendo come le stesse vie possano essere protettive in un contesto e dannose in un altro.
Addestrare macchine a riconoscere la malattia dalle cellule del sangue
Per trasformare questo atlante in uno strumento pratico, il team ha applicato apprendimento automatico interpretabile. Hanno addestrato modelli a gradient-boosted decision tree separatamente per ciascun tipo cellulare principale, chiedendo agli algoritmi di etichettare le singole cellule con la corretta malattia sulla base della loro espressione genica. Questi modelli hanno raggiunto elevata accuratezza quando testati su campioni tenuti da parte, soprattutto dopo la correzione delle differenze tecniche. Usando SHAP, un metodo che spiega quali geni guidano ogni decisione, i ricercatori hanno potuto identificare potenziali biomarcatori. Un esempio è CYBA nei monociti, i cui livelli aiutavano a distinguere malattie cutanee come la psoriasi dall'infiammazione intestinale nella malattia di Crohn e nella colite ulcerosa. Un altro è IFITM1 in certi linfociti T e cellule linfoidi innate, che separava l'asma dalla BPCO e suggeriva diversi schemi di difesa antivirale cronica.
Verso una bussola diagnostica basata sul sangue
Infine, gli autori hanno verificato se interi pazienti — non solo singole cellule — potessero essere classificati a partire dai loro profili immunitari circolanti. Hanno proiettato i dati di ogni cellula in uno spazio compresso di “embedding”, mediato questi embedding per tipo cellulare per paziente e addestrato classificatori per predire la malattia. Quando i nuovi pazienti somigliavano a quelli nei dati di addestramento, le prestazioni erano eccellenti. Ma quando i campioni provenivano da studi completamente indipendenti che usavano metodi di laboratorio diversi, l'accuratezza scendeva bruscamente, rivelando quanto questi strumenti siano sensibili alla variabilità tecnica. Un dataset più controllato e “centralizzato”, generato in un unico centro con una singola chimica di sequenziamento, ha ripristinato gran parte delle prestazioni, indicando la necessità di protocolli standardizzati o di set di addestramento molto grandi e diversificati.
Cosa significa per la diagnosi e il trattamento futuri
Per un lettore non specialista, il messaggio chiave è che le tue cellule immunitarie circolanti portano un ricco codice di come il tuo corpo è infiammato. Leggendo questi codici cellula per cellula, questo lavoro dimostra che è possibile distinguere molte malattie, scoprire geni che possono guidare sintomi specifici e iniziare a costruire test ematici universali per classificare le malattie infiammatorie. Lo studio non è ancora un test clinico pronto all'uso — le differenze tecniche tra gli studi limitano ancora l'affidabilità — ma pone le basi per futuri strumenti di “biopsia liquida” che potrebbero aiutare i medici a identificare prima la diagnosi e il trattamento giusti, usando un semplice prelievo di sangue.
Citazione: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Parole chiave: infiammazione, cellule immunitarie, sequenziamento dell'RNA a singola cellula, biomarcatori, apprendimento automatico