Clear Sky Science · it
Utilità clinica reale del sequenziamento genomico completo nei tumori solidi avanzati
Perché leggere i test del DNA può cambiare la cura del cancro
I medici utilizzano sempre più spesso potenti test del DNA per analizzare i tumori alla ricerca di centinaia di alterazioni genetiche contemporaneamente, con l’obiettivo di associare ogni paziente a un farmaco che miri in modo preciso al suo tumore. Ma al di fuori degli studi clinici non era chiaro quanto spesso questa strategia effettivamente prolungasse la vita delle persone. Questo studio esamina più di 54.000 persone con tumori avanzati in tutta la Giappone per porre una domanda semplice ma importante: quando si profila in modo completo il patrimonio genetico di un tumore, quale beneficio reale ottengono concretamente i pazienti?
Uno sguardo sotto il cofano di migliaia di tumori
I ricercatori hanno utilizzato un database nazionale che registra informazioni genetiche e cliniche dei pazienti che hanno effettuato la profilazione genomica completa (CGP) come parte della cura di routine. Tutti i pazienti avevano tumori solidi avanzati e avevano in gran parte completato i trattamenti standard. Attraverso un unico test che analizza 324 geni correlati al cancro, il gruppo ha catalogato quali mutazioni erano presenti e quanto solida fosse l’evidenza che ciascuna mutazione potesse essere bersagliata da una terapia esistente o supportata da dati convincenti. Hanno raggruppato i riscontri dal livello di evidenza più consolidato (livello A) fino a quelli supportati solo da studi preclinici iniziali (livello E) o privi di un collegamento terapeutico attuale.
Corrispondenze genetiche e sopravvivenza: chi sta meglio?
Nel complesso, quasi tre quarti dei pazienti presentavano almeno una alterazione genetica che gli esperti considerano potenzialmente “azionabile”, cioè in grado di orientare la terapia. Coloro i cui tumori portavano marcatori con le evidenze più solide (livello A) tendevano, in media, a vivere più a lungo rispetto ai pazienti i cui tumori presentavano solo marcatori più deboli o assenti. Per esempio, le persone con riscontri di livello A associati a farmaci già approvati avevano una sopravvivenza mediana di circa 16 mesi dopo il test, rispetto a circa 12 mesi per i pazienti con riscontri meno informativi. Questo schema è stato osservato in diversi tumori, inclusi polmone, vie biliari e endometrio, suggerendo che individuare un target ad alta confidenza può tradursi in risultati migliori, anche nella pratica clinica reale. 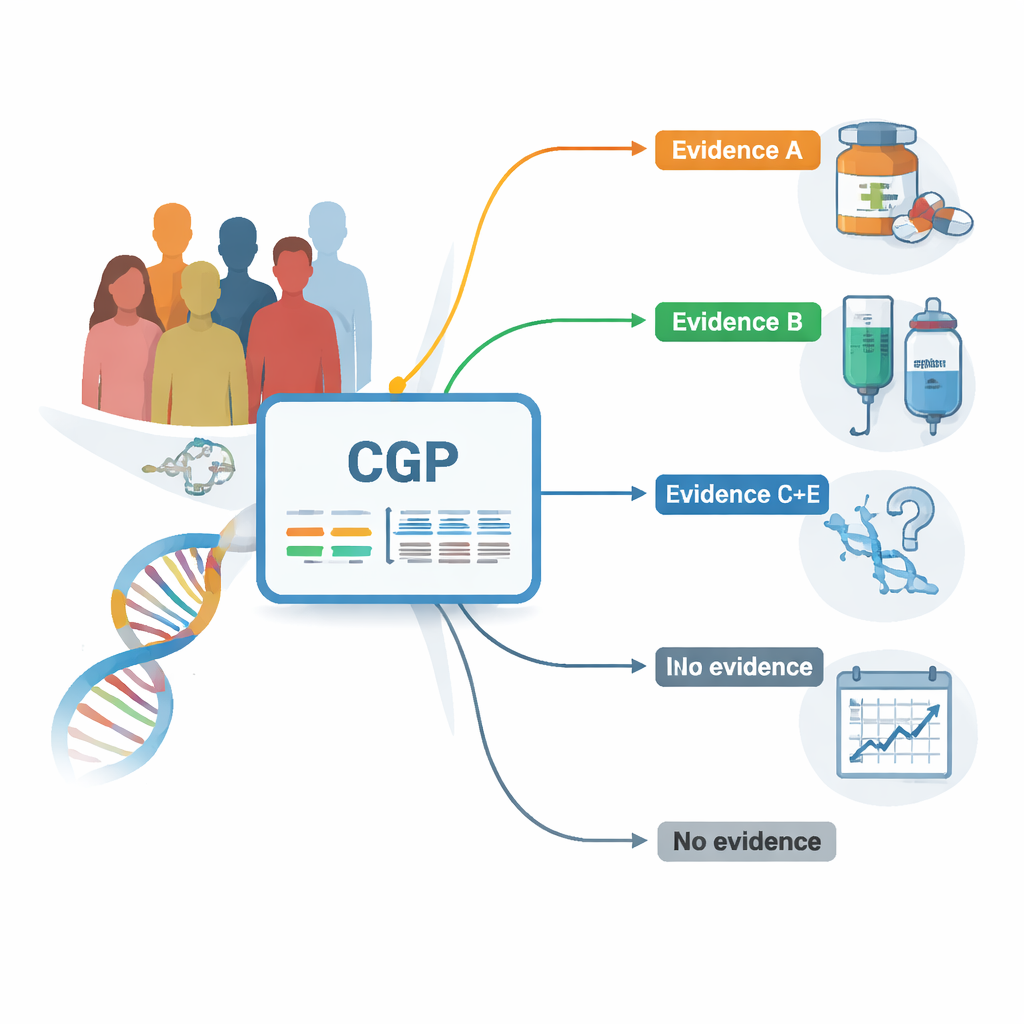
Dalla mutazione promettente al farmaco effettivo
Tuttavia avere un buon bersaglio nel tumore e ricevere effettivamente un farmaco corrispondente si sono rivelate due cose molto diverse. Solo circa l’8% di tutti i pazienti ha poi ricevuto un trattamento chiaramente guidato dai risultati della CGP—sia un farmaco di precisione approvato sia una terapia sperimentale in uno studio clinico o in uso off-label. Le barriere includevano età avanzata, condizioni generali di salute peggiori e il fatto semplice che trial clinici o farmaci adatti non erano sempre disponibili per ogni mutazione. La frazione di pazienti che ha effettivamente beneficiato è aumentata nel tempo con l’approvazione di più farmaci di precisione, ma sono emerse grandi differenze tra tipi di tumore: più di uno su cinque dei pazienti con tumori della tiroide o del polmone ha ricevuto trattamenti guidati dalla CGP, mentre la quota è rimasta sotto il 2% nei tumori del pancreas e del fegato.
Quando una soluzione unica non va bene per tutti
Lo studio si è anche concentrato sui cosiddetti marcatori “tumor-agnostici”, che dovrebbero funzionare trasversalmente in molti tumori. Un esempio chiave è il carico mutazionale tumorale (TMB), una conta delle variazioni del DNA presenti in un tumore. I pazienti con TMB molto elevato—in particolare 20 o più mutazioni per milione di basi—tendevano a rispondere meglio e a vivere più a lungo dopo il trattamento con l’immunoterapia pembrolizumab, indipendentemente da un altro marcatore chiamato instabilità dei microsatelliti. Tuttavia sono emerse eccezioni sorprendenti. In un raro tumore cutaneo noto come malattia di Paget extramammaria, anche i tumori con TMB elevato hanno resistito a pembrolizumab e i pazienti hanno avuto esiti peggiori, avvertendo che un marcatore “universale” può fallire in contesti specifici. Il gruppo ha anche mostrato che non tutte le fusioni genetiche che coinvolgono i geni NTRK rispondono allo stesso modo ai farmaci anti-TRK, e che alcuni pazienti i cui test più vecchi e mirati avevano mancato mutazioni chiave hanno comunque tratto beneficio quando la CGP le ha rilevate in seguito. 
Cosa significa per pazienti e medici
Per le persone con cancro avanzato, questo studio offre sia speranza che realismo. La CGP aiuta chiaramente a stratificare i pazienti in gruppi con prospettive migliori o peggiori e può far emergere opzioni terapeutiche potenti, in particolare in alcuni tumori e nei pazienti con tumori molto ricchi di mutazioni. Allo stesso tempo, la maggior parte dei pazienti con riscontri “azionabili” non riceve comunque un farmaco corrispondente, a causa dei limiti nelle approvazioni dei farmaci, nell’accesso ai trial e nello stato di salute. Il messaggio è che il test genetico esteso è uno strumento prezioso—ma il suo beneficio reale dipende dall’esistenza dei farmaci giusti, dei trial e dei sistemi di cura in grado di tradurre i risultati del test in azione.
Citazione: Saito, Y., Horie, S., Kogure, Y. et al. Real-world clinical utility of comprehensive genomic profiling in advanced solid tumors. Nat Med 32, 690–701 (2026). https://doi.org/10.1038/s41591-025-04086-8
Parole chiave: oncologia di precisione, profilazione genomica, carico mutazionale tumorale, terapia mirata, immunoterapia