Clear Sky Science · it
Espansione delle cDC1 tumorali mediata da Flt3L migliora l’immunoterapia primando cellule T CD8 “stem‑like” nei linfonodi
Aiutare il sistema immunitario a ricordare come combattere il cancro
Perché i tumori di alcune persone regrediscono con le immunoterapie moderne mentre altri ne traggono poco beneficio? Questo studio esplora i meccanismi del sistema immunitario per rispondere a quella domanda. I ricercatori mostrano che potenziando un particolare gruppo di cellule sentinella nei tumori è possibile creare una riserva di cellule T citotossiche a lunga vita, “stem‑like”, nei linfonodi vicini. Queste cellule, a loro volta, rendono i farmaci di blocco dei checkpoint, in particolare la terapia anti‑CTLA‑4, più efficaci e duraturi.
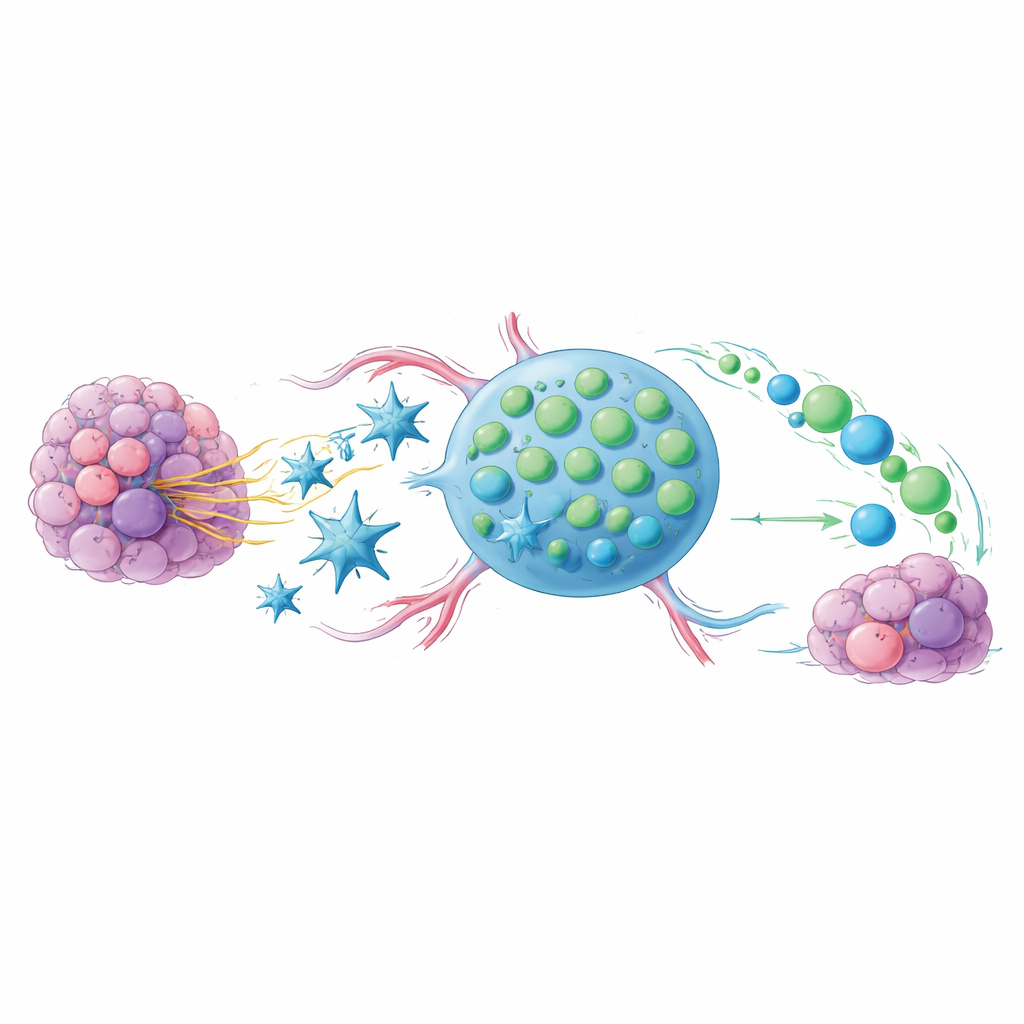
Il problema delle cellule antitumorali esauste
I farmaci che bloccano i checkpoint come anti‑PD‑1 e anti‑CTLA‑4 liberano le cellule immunitarie contro il cancro, ma funzionano bene solo in una frazione dei pazienti. Un indizio risiede nello stato delle cellule T CD8, i principali esecutori contro cellule infette o tumorali. Quando queste cellule T sono sollecitate troppo a lungo, entrano in uno stato di affaticamento («exhaustion») e smettono di proliferare efficacemente. Un sottoinsieme più piccolo, però, conserva caratteristiche più giovanili e “stem‑like”: si dividono facilmente, generano nuovi effettori e sono fortemente associati a risposte favorevoli nei pazienti trattati con inibitori dei checkpoint. La domanda centrale di questo lavoro è come indurre i tumori e il loro microambiente a favorire queste cellule stem‑like rispetto alle loro controparti esauste.
Potenziare le cellule sentinella del tumore
Il gruppo si è concentrato sulle cellule dendritiche convenzionali di tipo 1, una classe rara ma potente di sentinelle immunitarie che eccelle nel presentare frammenti tumorali alle cellule T. Hanno usato un segnale di crescita chiamato ligando Flt3 (Flt3L) per espandere queste cellule all’interno di tumori murini, sia ingegnerizzando le cellule tumorali per secernere il ligando sia somministrandolo come farmaco. Il sequenziamento dell’RNA a singola cellula ha rivelato che i tumori ricchi di Flt3L contenevano molti più dendriti e linfociti e meno cellule tumorali. Nel compartimento dendritico si sono ampliate tre popolazioni distinte, inclusa una altamente matura e predisposta a migrare verso i linfonodi, dove le cellule T vengono inizialmente educate. Allo stesso tempo, le cellule T CD8 all’interno di questi tumori si sono spostate da un profilo terminalmente esausto verso uno stato più stem‑like o simile alla memoria.
Costruire una riserva di cellule T stem‑like nei linfonodi
Tracciando le cellule T specifiche per il tumore e usando strumenti genetici, i ricercatori hanno dimostrato che il trattamento con Flt3L aumenta una popolazione di CD8 che esprime marcatori di superficie associati al potenziale stem‑like e a divisione attiva. Queste cellule dipendevano dalle cellule dendritiche XCR1‑positive e dal movimento guidato da CCR7 delle dendritiche dal tumore al linfonodo drenante. Quando le dendritiche venivano deplete o la loro migrazione disabilitata, la riserva di cellule T stem‑like si riduceva. Bloccare l’uscita dei linfociti dai linfonodi produceva un effetto simile, interrompendo l’afflusso di nuove cellule T al tumore. Il profilo molecolare ha rivelato che questo processo dipendeva dal fattore di trascrizione Myb e favoriva cellule T con un riconoscimento dei bersagli tumorali di forza relativamente bassa, un tipo sempre più riconosciuto come importante per un controllo duraturo del cancro.
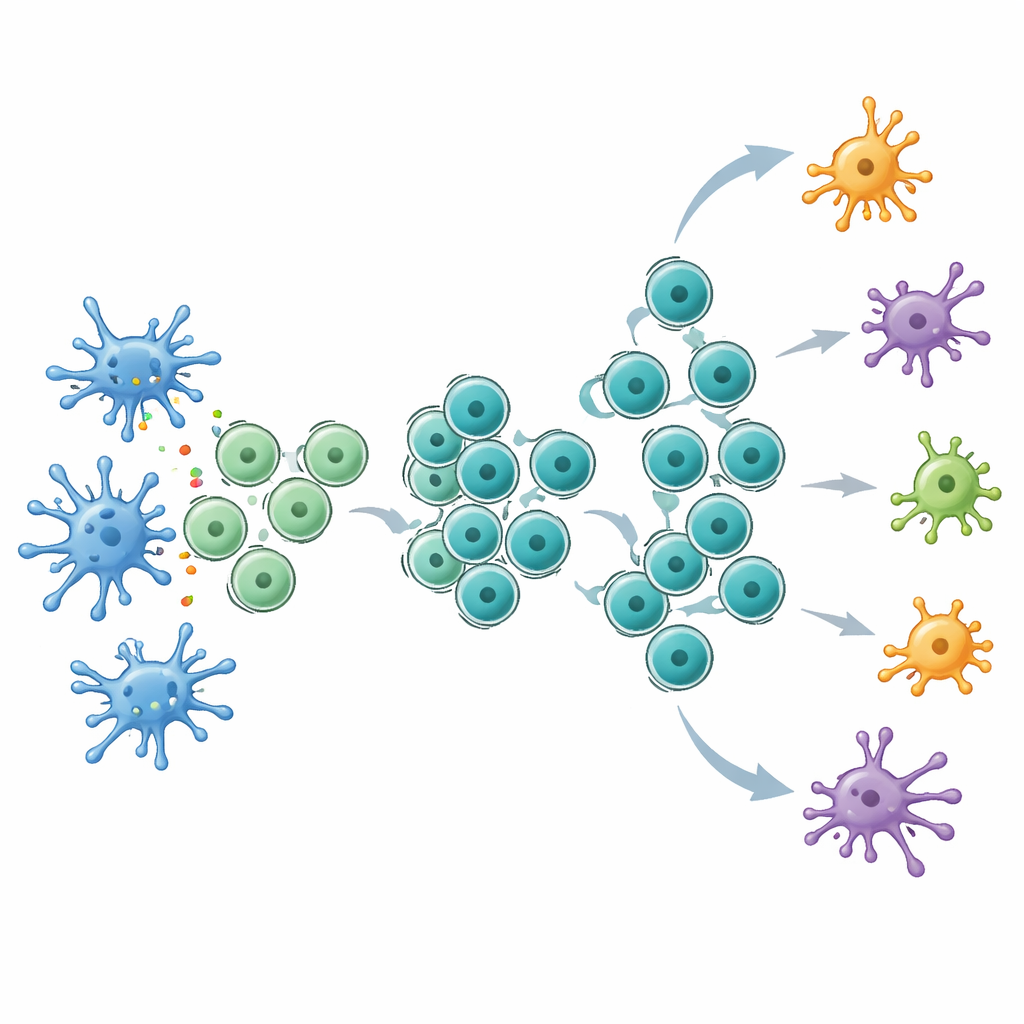
Rendere la terapia di checkpoint più efficace
Con questa riserva ampliata di cellule T stem‑like, i topi hanno risposto molto meglio al blocco dei checkpoint, in particolare al trattamento anti‑CTLA‑4. I tumori negli animali trattati con Flt3L si sono ridotti di più, la sopravvivenza è migliorata e nel sangue e nei linfonodi si sono trovate più cellule T specifiche per il tumore. Nei tumori, Flt3L ha aumentato le cellule CD8 stem‑like, mentre il successivo blocco di CTLA‑4 sembrava spingere queste cellule a maturare in effettori potenti che producevano alti livelli di molecole antitumorali chiave. Il sequenziamento dei recettori delle cellule T ha mostrato che la terapia combinata ha esteso la gamma di cloni T che si espandevano, includendo molti cloni subdominanti, suggerendo un attacco più diversificato contro il tumore. Analisi dettagliate a singola cellula hanno individuato un cluster unico di cellule T CD8, caratterizzato dall’espressione del recettore per la citochina IL‑21, che si collocava a metà strada tra stati stem‑like ed esausti e condivideva recettori T sia con popolazioni precoci sia tardive. Bloccare la segnalazione di IL‑21 indeboliva i benefici della combinazione Flt3L più anti‑CTLA‑4.
Cosa significa per i trattamenti anticancro futuri
Il messaggio per un lettore non specialistico è che il successo dell’immunoterapia non dipende solo dall’attivare con forza il sistema immunitario, ma dall’avere il tipo giusto di cellule da attivare. Questo lavoro mostra che nutrire e guidare le cellule dendritiche con Flt3L può rifornire i linfonodi vicini con un serbatoio rinnovabile di cellule T citotossiche stem‑like. Quando vengono poi somministrati inibitori dei checkpoint come l’anti‑CTLA‑4, questi possono attingere a tale riserva per generare ondate di nuovi combattenti più numerosi, più diversi e più efficaci nel controllare i tumori. Analisi di dataset tumorali umani suggeriscono che le firme geniche collegate a questa via predicono anch’esse esiti migliori nei pazienti. Nel loro insieme, questi risultati indicano verso trattamenti combinati che prima costruiscono il “stock” cellulare immunitario con agenti come Flt3L e poi lo liberano con farmaci checkpoint per un controllo tumorale più forte e duraturo.
Citazione: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Parole chiave: immunoterapia del cancro, cellule dendritiche, cellule T CD8 stem‑like, inibizione dei checkpoint, ligando Flt3