Clear Sky Science · it
CD38 dota le cellule Treg antigeno-specifiche locali di resilienza allo stress per il controllo dell’infiammazione compartimentalizzata del SNC
Perché le cellule immunitarie che proteggono il cervello sono importanti
Molte malattie autoimmuni cerebrali, come la sclerosi multipla, si comportano come incendi che covano: un’intensa fase infiammatoria iniziale si attenua, ma il danno può riesplodere anni dopo. Questo studio pone una domanda apparentemente semplice ma di grande portata: dopo un attacco nel sistema nervoso centrale (SNC), che mantiene la pace — e cosa invece riporta l’equilibrio verso la malattia? Gli autori si concentrano su una piccola popolazione di cellule immunitarie chiamate cellule T regolatorie che si insediano in cervello e midollo spinale dopo l’infiammazione, e svelano come una singola molecola di superficie le renda capaci di sopravvivere in un ambiente ostile e prevenire le ricadute.
Peacekeeper immunitari che restano sul posto
Usando un modello murino che imita aspetti della sclerosi multipla, i ricercatori hanno seguito diversi tipi di cellule T mentre la malattia saliva fino al picco e poi entrava in fase di recupero. Mentre le normali cellule T helper che promuovono l’infiammazione diminuivano di numero con il miglioramento dei sintomi, le cellule T regolatorie — cellule specializzate che normalmente attenuano le risposte immunitarie — rimanevano nel SNC. La loro quota relativa all’interno del pool locale di cellule T aumentava in realtà, e si raggruppavano in nicchie distinte attorno agli spazi del fluido cerebrale e alle membrane protettive che rivestono il cervello. Etichettando da dove provenivano le cellule T in arrivo, il gruppo ha mostrato che, dopo il recupero, pochissime nuove cellule T regolatorie giungevano dai linfonodi. Invece, la popolazione del SNC si manteneva in gran parte localmente, suggerendo una forza «peacekeeping» residente a lungo termine. 
Guardiani tolleranti allo stress di una nicchia ostile
Il SNC postinfiammatorio è tutt’altro che confortevole per questi guardiani. Dopo l’ondata principale della malattia, i livelli del segnale di crescita interleuchina‑2 (IL‑2) — dal quale le cellule T regolatorie dipendono fortemente — calano perché la maggior parte delle cellule T convenzionali si è ritirata. Allo stesso tempo, il tessuto è ricco della molecola metabolica NAD+, che può innescare la morte cellulare o compromettere recettori di superficie chiave quando viene modificata da un enzima specifico. Marcando geneticamente e seguendo singole cellule T regolatorie, gli autori hanno distinto cellule «stabili» che mantennero la loro identità da quelle «instabili» che persero il programma caratteristico Foxp3. Le cellule stabili mostravano un’impronta molto più marcata di segnalazione IL‑2 e livelli più elevati di recettori per l’IL‑2, suggerendo che la capacità di percepire quantità scarse di IL‑2 è centrale per sopravvivere in questo ambiente stressato.
Controllo locale delle ricadute dall’interno del cervello
Per verificare se queste cellule T regolatorie residenti fossero davvero importanti per il controllo a lungo termine della malattia, i ricercatori le rimossero selettivamente dal SNC usando una tossina somministrata direttamente nel fluido cerebrale, preservando invece la maggior parte delle cellule T regolatorie sistemiche nel resto del corpo. Nel giro di pochi giorni, i topi in fase di recupero svilupparono gravi ricadute con rinnovata paralisi. Al contrario, depletare le cellule T regolatorie solo nell’organismo, risparmiando quelle nel SNC, non scatenò focolai. La ricaduta coinvolse la riattivazione rapida e l’espansione di cellule T effettrici già insediate nel SNC, anche quando il loro reclutamento dal sangue era bloccato. Questo dimostra che le cellule T regolatorie locali, piuttosto che quelle circolanti, sono essenziali per contenere cellule aggressive residue che permangono dopo il passaggio acuto.
Come un enzima protegge le cellule regolatorie
Approfondendo, gli autori cercarono molecole che distinguessero le cellule T regolatorie del SNC tolleranti allo stress. Emersi come attore chiave è CD38, un enzima di superficie che degrada il NAD+ extracellulare. Nel SNC infiammato, le cellule T regolatorie aumentarono fortemente l’espressione di CD38, mentre le cellule T convenzionali non mostrarono un cambiamento così marcato. Quando il team trasferì cellule T regolatorie reattive alla mielina prive di CD38 in topi, queste cellule raggiunsero il SNC ma non riuscirono a controllare la malattia, a differenza delle controparti normali. In animali chimerici misti, dove solo le cellule T regolatorie residenti erano carenti di CD38, rimuovere la frazione CD38‑sufficiente fu sufficiente a provocare ricadute, mostrando che CD38 agisce in modo cellula‑intrinseco per abilitare un controllo efficace.
Proteggere il segnale vitale
Esperimenti meccanicistici rivelarono come CD38 conferisca questa resilienza. Alti livelli di NAD+ nel SNC possono alimentare la modifica chimica delle proteine di superficie ad opera dell’enzima ARTC2.2. Un bersaglio sensibile è la subunità ad alta affinità del recettore per l’IL‑2, che le cellule T regolatorie esprimono a livelli molto elevati, specialmente quando riconoscono antigeni cerebrali. Nelle cellule T regolatorie prive di CD38 esposte al NAD+, la maggior parte dei recettori per l’IL‑2 risultò modificata, portando a una minore attivazione del messaggero a valle STAT5 e a una ridotta risposta all’IL‑2. Al contrario, le cellule che esprimevano CD38 abbassarono localmente il NAD+ attorno a sé, limitando questa modifica dannosa e preservando una forte segnalazione IL‑2. In topi vivi, iniettare NAD+ nel cervello uccise selettivamente la maggior parte delle cellule T regolatorie tramite questa via, risparmiando le cellule T convenzionali, sottolineando quanto la nicchia sia precaria senza questo enzima protettivo. 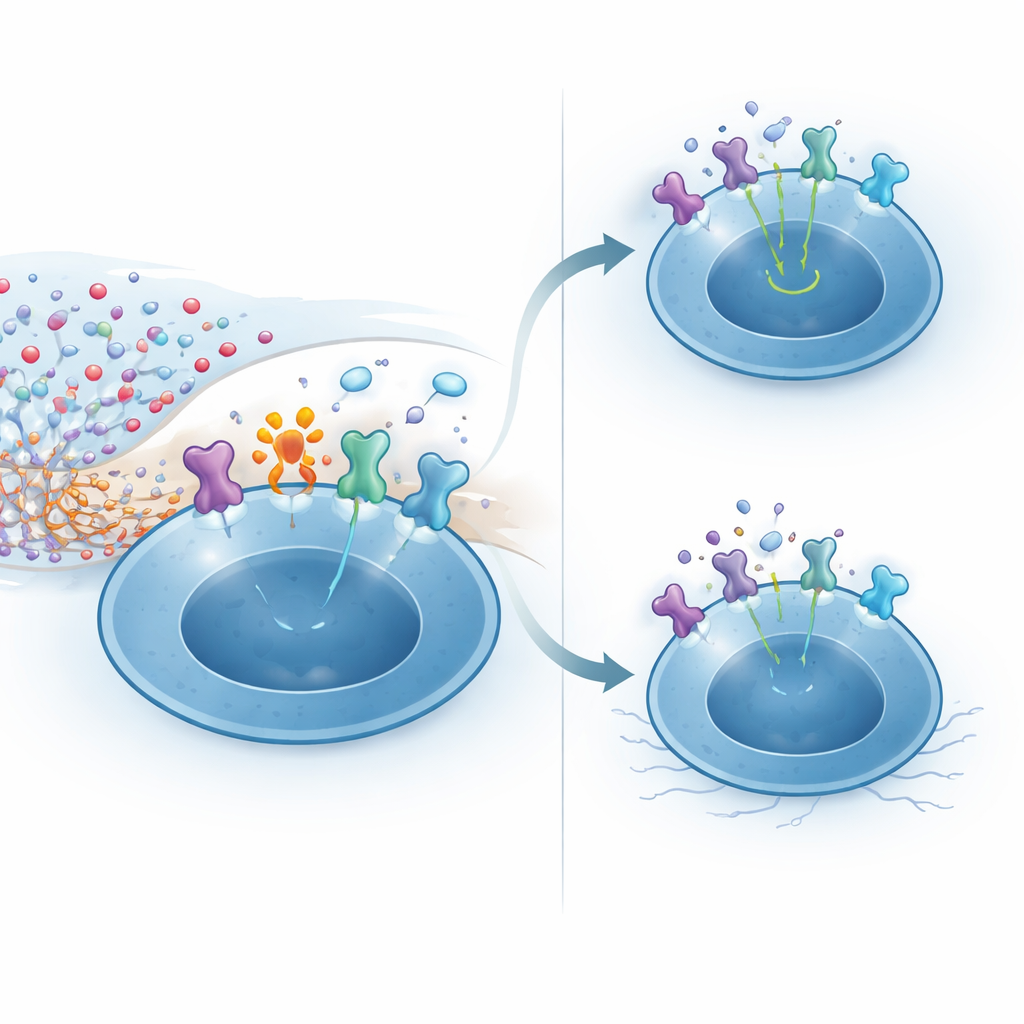
Cosa significa per l’autoimmunità cerebrale cronica
Questo lavoro dipinge il quadro dell’autoimmunità cronica del SNC come una battaglia compartimentalizzata: piccoli ammassi di cellule T aggressive residue risiedono in cervello e midollo spinale, tenuti sotto controllo da cellule T regolatorie locali altrettanto specializzate. Questi guardiani sono «tolleranti allo stress» perché CD38 consente loro di sopravvivere a elevati livelli di NAD+ e di continuare a percepire quantità minute di IL‑2, preservando la loro identità e funzione soppressiva. Per il lettore non specialistico, il punto chiave è che il controllo a lungo termine di malattie come la sclerosi multipla potrebbe dipendere meno dal sistema immunitario circolante e più dal nutrire e proteggere questi peacekeeper residenti all’interno del cervello stesso — potenzialmente intervenendo su vie che potenziano la funzione di CD38 o la sensibilità all’IL‑2 nelle cellule T regolatorie.
Citazione: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Parole chiave: cellule T regolatorie, sclerosi multipla, infiammazione del sistema nervoso centrale, enzima CD38, tolleranza immunitaria