Clear Sky Science · it
Patterning spaziale della segnalazione TGFβ nei fibroblasti alla base della resistenza al trattamento nell'artrite reumatoide
Perché il dolore articolare ostinato conta
Molte persone con artrite reumatoide assumono farmaci moderni che placano il sistema immunitario, eppure le loro articolazioni restano dolorose e rigide. Questo studio si chiede perché alcuni pazienti non migliorano nemmeno quando l'infiammazione articolare sembra attenuarsi. Esaminando con precisione dove e come certe cellule di supporto nell'articolazione attivano programmi di cicatrizzazione, i ricercatori scoprono una forma nascosta di danno che potrebbe spiegare il dolore persistente e indicare nuove strategie terapeutiche.
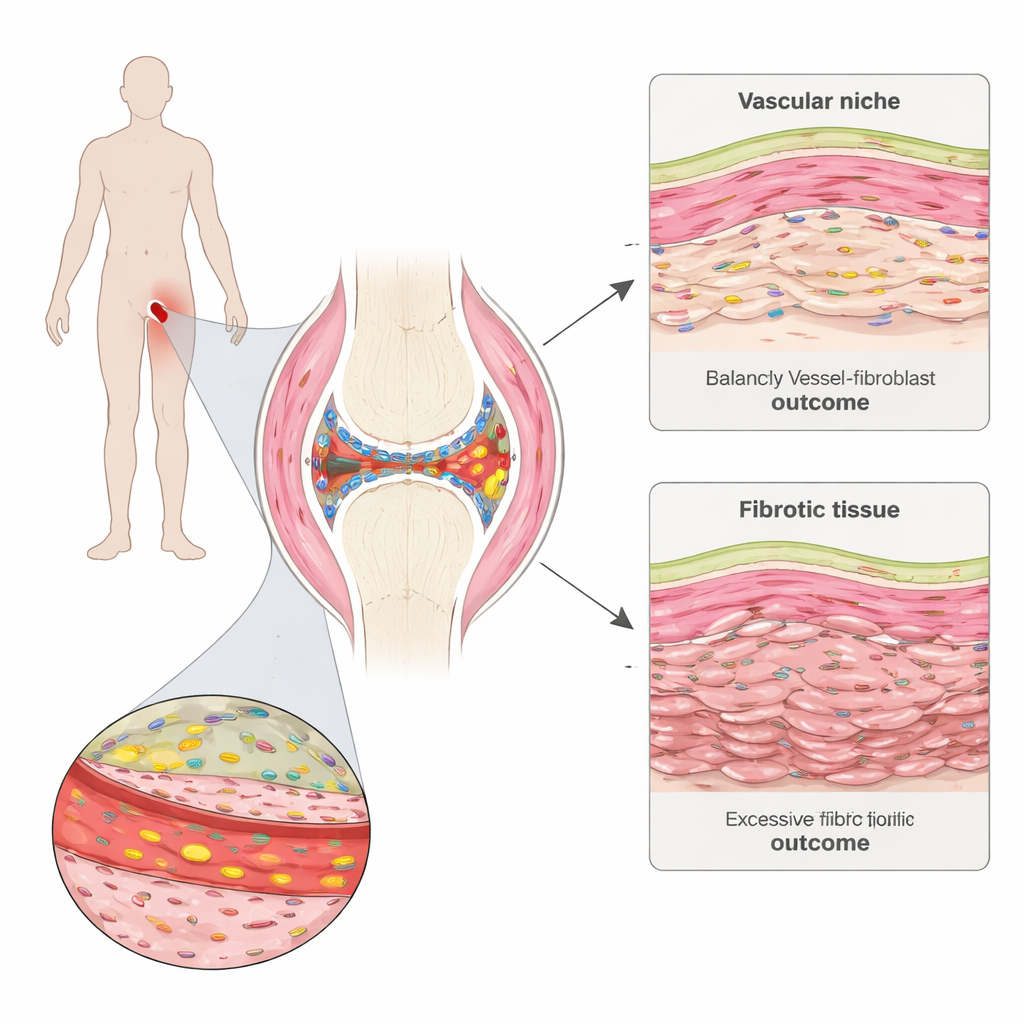
Uno sguardo ravvicinato nell'articolazione dolorante
L'artrite reumatoide colpisce la sinovia, un sottile tessuto che riveste e lubrifica le articolazioni. Il gruppo ha raccolto piccole biopsie sinoviali da persone con malattia in fase precoce prima di iniziare la terapia e di nuovo sei mesi dopo. Usando avanzate tecniche di mappatura spaziale dell'espressione genica, hanno potuto vedere quali geni erano attivi in migliaia di singole cellule preservando la loro posizione nel tessuto. Hanno identificato “quartieri” distinti nella sinovia, inclusi ammassi di cellule immunitarie, aree ricche di grasso, il sottile rivestimento interno e regioni ricche di vasi sanguigni e cellule strutturali chiamate fibroblasti.
Cellule che formano cicatrici e resistenza al trattamento
Confrontando i pazienti che poi raggiunsero la remissione con quelli che non ci riuscirono, i ricercatori hanno trovato uno schema netto: prima del trattamento, i pazienti non in remissione mostravano già segnali più forti di cicatrizzazione tissutale, o fibrosi. Un particolare programma dei fibroblasti, caratterizzato dall'alta produzione di una proteina della matrice extracellulare chiamata COMP, era espanso in questi pazienti. Questi fibroblasti ricchi di COMP condividevano tratti con le cellule che formano cicatrici osservate nella fibrosi polmonare e cutanea e risultavano maggiormente associati a una risposta terapeutica scarsa. Col tempo, le regioni dominate da queste cellule tendevano a diventare densamente impregnate di tessuto connettivo ma relativamente povere di cellule, suggerendo che depositano una matrice rigida che può persistere anche dopo l'attenuazione dell'infiammazione.
I vasi sanguigni come conduttori nascosti
I fibroblasti fibrogenici non erano distribuiti a caso. Si raggruppavano intorno ai vasi sanguigni, formando zone perivascolari stratificate. Lo strato più interno, a contatto con la parete del vaso, esprimeva geni diversi rispetto allo strato esterno. Il gruppo ha mostrato che le cellule che rivestono i vasi inviano segnali Notch ai fibroblasti vicini, che a loro volta modulano come questi fibroblasti rispondono a una famiglia di segnali pro‑cicatriziali nota come TGF‑beta. Vicino al vaso, la segnalazione Notch spinge i fibroblasti a produrre TGF‑beta ma contemporaneamente riduce il numero di recettori per TGF‑beta sulla loro superficie, contenendone la sensibilità. Più lontano, dove l'influenza Notch svanisce, i fibroblasti presentano più recettori e diventano altamente reattivi, trasformandosi in cellule ricche di COMP che guidano la fibrosi.
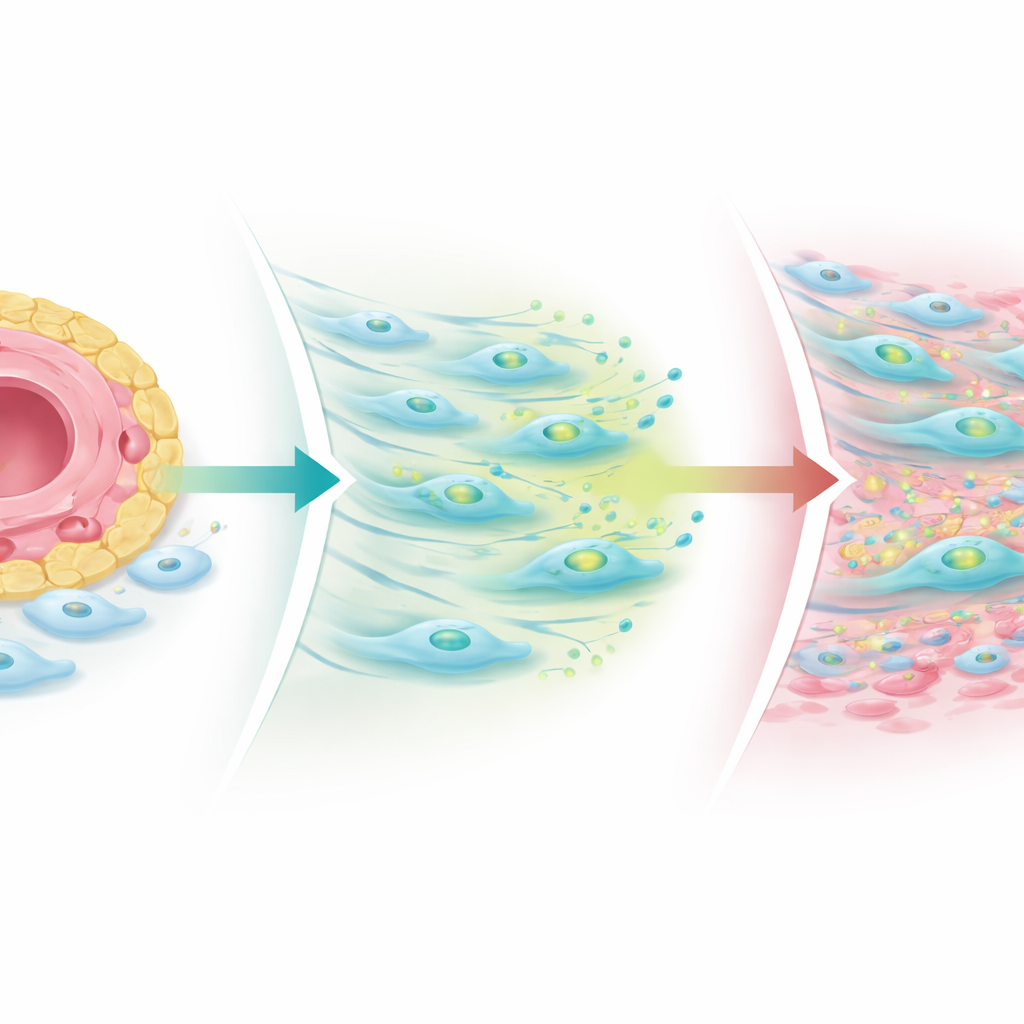
Cosa succede quando l'equilibrio si rompe
I ricercatori hanno costruito modelli articolari semplificati in colture e organoidi tridimensionali derivati da tessuto di pazienti per sondare questo meccanismo. Quando hanno rafforzato i segnali Notch dalle cellule endoteliali, i fibroblasti aumentarono la produzione di TGF‑beta ma ridussero i livelli di recettori, limitando la cicatrizzazione. Quando hanno bloccato Notch o disturbato il suo schema regolare, i fibroblasti recuperarono i recettori per TGF‑beta—in particolare un co‑recettore chiamato recettore TGF‑beta III—and le cellule fibrogeniche positive per COMP si espansero lontano dai vasi. Nelle biopsie dei pazienti prelevate dopo il trattamento, gli ammassi di cellule immunitarie si ridussero in quasi tutti i casi, ma le nicchie fibrogeniche, in particolare le regioni ricche di COMP, spesso crebbero, soprattutto in chi continuava a soffrire di dolore articolare. Ciò suggerisce che i farmaci antinfiammatori standard possono spegnere il “fuoco” immunitario lasciando però intatto o addirittura svelando un processo di cicatrizzazione che mantiene le articolazioni rigide e dolorose.
Nuove vie per calmare le articolazioni ostinate
Infine, il gruppo ha testato se interrompere questo circuito fibrogenico potesse essere utile terapeuticamente. Negli organoidi derivati da pazienti, farmaci che inibiscono Notch o bloccano la segnalazione TGF‑beta ridussero la produzione di COMP, di altre proteine correlate alla cicatrice e di collagene chiave, e rimodellarono l'attività genica nelle zone perivascolari. Per un osservatore non specialistico, il messaggio è che non tutto il danno nell'artrite reumatoide deriva dall'infiammazione visibile: una parte è "cablaggio" del tessuto di supporto dell'articolazione e dei suoi vasi. Mirando alla conversazione Notch–TGF‑beta che controlla come i fibroblasti depositano tessuto cicatriziale, i trattamenti futuri potrebbero prevenire o invertire una forma fibrotica ostinata della malattia che resiste agli attuali farmaci focalizzati sul sistema immunitario.
Citazione: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Parole chiave: artrite reumatoide, fibrosi, fibroblasti, segnalazione TGF-beta, via Notch