Clear Sky Science · it
Ingegneria della xilosiltransferasi per manipolare i proteoglicani nelle cellule dei mammiferi
Perché la «pellicola» cellulare è importante
Ogni cellula del nostro corpo porta una sorta di «mantello» molecolare che la aiuta a comunicare con le vicine e a percepire l’ambiente circostante. Una parte importante di questo rivestimento è costituita dai proteoglicani: proteine decorate con lunghe catene di zuccheri che funzionano come minuscole antenne per fattori di crescita, segnali immunitari e segnali strutturali. Quando questa decorazione zuccherina è alterata, lo sviluppo può risultare compromesso e tessuti come ossa e muscoli possono essere gravemente colpiti. Tuttavia, i ricercatori hanno faticato a mappare con precisione quali proteine portano queste catene e come i singoli componenti del «mantello» influenzino il comportamento cellulare. Questo studio introduce una strategia chimica precisa per marcare e ricostruire queste catene zuccherine su cellule di mammifero vive, aprendo la strada per leggere e riscrivere l’informazione codificata sulle loro superfici. 
Rimodulare il primo passo dell’attacco degli zuccheri
La costruzione dei proteoglicani inizia quando una famiglia enzimatica speciale, le xilosiltransferasi XT1 e XT2, installa il primo zucchero su una proteina, segnando il punto in cui crescerà una lunga catena. Poiché entrambi gli enzimi possono compiere questo stesso primo passo, è stato difficile capire su quali proteine ciascuno lavori all’interno delle cellule. Gli autori hanno usato un design «bump‑and‑hole» — comune nella biologia chimica moderna — per risolvere il problema. Hanno leggermente ridefinito il sito attivo di XT1, creando uno spazio aggiuntivo (il «buco»), e introdotto un blocco di costruzione zuccherino corrispondente, leggermente più ingombrante, 6AzGlc (il «rigonfiamento»). La XT1 ingegnerizzata può ora usare questo zucchero modificato, mentre l’enzima naturale non può farlo, permettendo ai ricercatori di marcare soltanto le proteine toccate dall’enzima riprogettato.
Introdurre di nascosto uno zucchero su misura nelle cellule
Per far funzionare questo approccio in cellule vive, il team ha dovuto fornire lo zucchero «con il bump» in una forma riconoscibile dal metabolismo cellulare. Invece di affidarsi alle normali vie di assorbimento degli zuccheri — che non gestiscono bene gli analoghi della xiloso — hanno costruito una versione protetta di 6AzGlc che porta un gruppo fosfato nascosto. Una volta nel citosol, gli enzimi cellulari liberano questo gruppo e convertono la molecola in UDP‑6AzGlc, la forma attivata richiesta dalle xilosiltransferasi ingegnerizzate. Cromatografie accurate hanno confermato che le cellule trattate con il composto incapsulato configurato correttamente producevano quantità sostanziali dello zucchero attivato su misura, mentre un controllo immagine speculare ne produceva quasi nessuna. 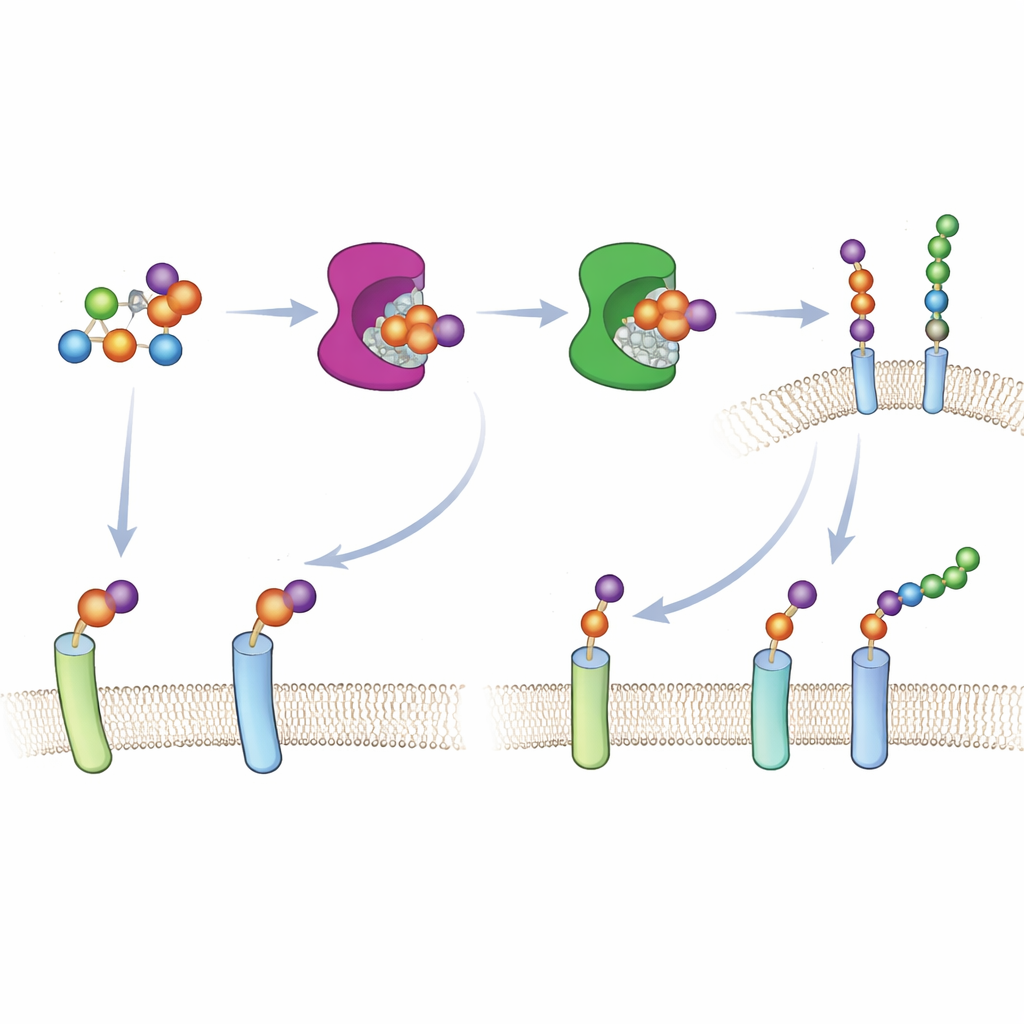
Marcare e identificare gli attori nascosti
Con l’enzima modificato e lo zucchero attivato al loro posto, i ricercatori hanno dimostrato che solo le cellule che esprimevano la XT1 o la XT2 ingegnerizzata incorporavano il marcatore 6AzGlc nei loro proteoglicani di superficie. Il gruppo azido sul 6AzGlc funge da minuscolo manico chimico che può essere «clikkato» a coloranti fluorescenti o a biotina, permettendo la visualizzazione e l’arricchimento delle proteine marcate. La spettrometria di massa dei campioni arricchiti ha rivelato una ricca collezione di proteoglicani noti — tra cui decorina, diversi glicopican, sindecano‑4, CD44 e versicana — confermando che il sistema marca proteine che portano genuinamente zuccheri. È importante che gli enzimi ingegnerizzati abbiano mantenuto le stesse preferenze di sequenza dei loro omologhi naturali, il che significa che il marcatore chimico viene installato in siti di attacco autentici e non in posizioni nuove o artificiali.
Costruire proteoglicani su misura
Un vantaggio inaspettato del marcatore 6AzGlc è che, diversamente dallo zucchero di partenza naturale, non può essere esteso in una catena completa dagli enzimi a valle. Questo limita di fatto la crescita della catena e semplifica la struttura molecolare da analizzare mediante spettrometria di massa. Gli autori hanno trasformato questa caratteristica in uno strumento: dopo che XT1 installa il 6AzGlc in un sito di attacco naturale, usano la chimica click per agganciare frammenti di eparina sintetici, creando «proteoglicani su misura» con catene zuccherine definite con precisione. In cellule di carcinoma mammario prive del proprio sindecano‑1, la reintroduzione di tali versioni progettate ha ripristinato l’estensione cellulare normale su una superficie rivestita di proteine, dimostrando che il proteoglicano ricostruito chimicamente può sostituire funzionalmente quello naturale.
Cosa significa per la biologia e la medicina
Questo lavoro fornisce un potente insieme di strumenti per marcare selettivamente e manipolare le catene zuccherine che controllano come le cellule comunicano. Separando i ruoli di XT1 e XT2 e marcando solo i loro bersagli diretti, i ricercatori possono ora mappare quali proteoglicani operano in tessuti e stati patologici specifici. La capacità di bloccare la crescita naturale delle catene e sostituirla con zuccheri costruiti su misura permette inoltre di scomporre quanto della funzione di un proteoglicano dipenda dal suo impianto proteico rispetto al suo «mantello» zuccherino. A lungo termine, tale ingegneria di precisione potrebbe aiutare a decodificare la segnalazione complessa alla superficie cellulare e ispirare terapie che riparino o riprogrammarno cappotti cellulari difettosi in disordini dello sviluppo, cancro e altre malattie.
Citazione: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Parole chiave: proteoglicani, glicosaminoglicani, xilosiltransferasi, biologia chimica, segnalazione sulla superficie cellulare