Clear Sky Science · it
Un unico sito allosterico fonde attivazione, modulazione e inibizione in TRPM5
Come un piccolo guardiano regola gusto e metabolismo
I cibi che apprezziamo e il modo in cui il nostro organismo gestisce lo zucchero dipendono da microscopiche proteine “guardiane” nelle cellule. Una di queste, un canale chiamato TRPM5, ci aiuta a percepire sapori dolci, amari e umami e contribuisce al rilascio di insulina dal pancreas. Questo studio rivela come una singola piccola tasca su TRPM5 possa comportarsi come una manopola di controllo principale, accendendo il canale, regolandone la sensibilità e persino spegnendolo — intuizioni che potrebbero orientare futuri trattamenti per diabete, obesità e disturbi gastrointestinali.
Un canale all’incrocio tra gusto e glicemia
TRPM5 si trova nelle membrane delle cellule gustative della lingua, nelle cellule endocrine dell’intestino e nelle cellule che secernono insulina nel pancreas. Quando il calcio intracellulare aumenta, TRPM5 si apre e lascia passare ioni carichi positivamente, modificando brevemente il voltaggio della cellula. Nei gusti, questo segnale elettrico comunica al cervello la presenza di qualcosa di dolce, amaro o umami sulla lingua. Nel pancreas, contribuisce a perfezionare i picchi di insulina dopo un pasto. Persone e animali con funzione TRPM5 compromessa mostrano problemi nel rilascio di insulina e nel controllo della glicemia, suggerendo che farmaci mirati a TRPM5 potrebbero un giorno aiutare a trattare malattie metaboliche. Tuttavia, fino a poco tempo fa i ricercatori non disponevano di strumenti precisi per accendere o spegnere questo canale.
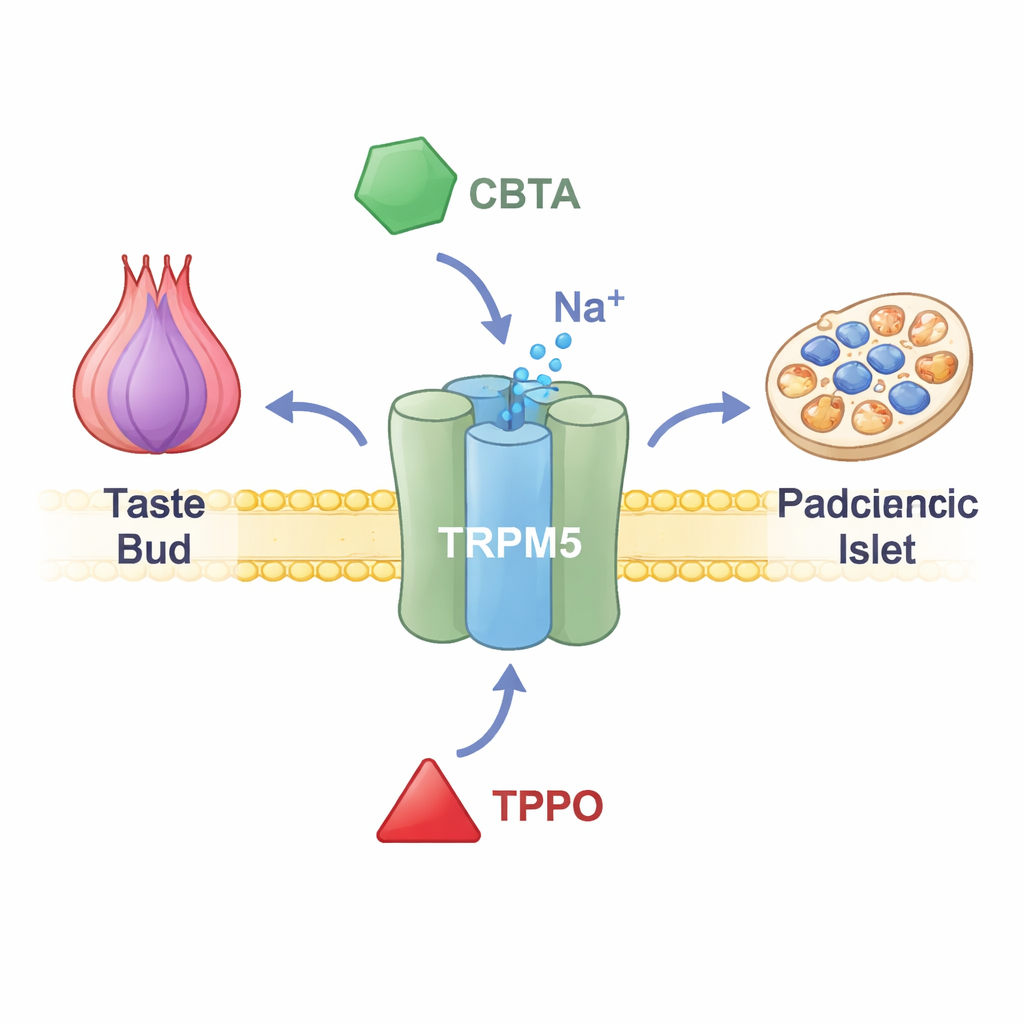
Un nuovo interruttore chimico che potenzia il canale
I ricercatori si sono concentrati su un composto sintetico chiamato CBTA, noto in precedenza per stimolare TRPM5 ma non ancora compreso a fondo. Utilizzando registrazioni elettriche da cellule ingegnerizzate per esprimere TRPM5, hanno mostrato che CBTA può aprire il canale anche quando il calcio è quasi assente, dimostrando che agisce come un vero attivatore e non si limita a potenziare gli effetti del calcio. Quando sono presenti tracce di calcio — livelli che normalmente lascerebbero TRPM5 inattivo — CBTA e calcio agiscono insieme, generando correnti molto più ampie di quelle indotte da ciascuno separatamente. Ciò significa che CBTA rende TRPM5 straordinariamente sensibile, così che livelli di calcio vicino al riposo diventano improvvisamente sufficienti per aprire completamente il canale.
Una tasca di controllo nascosta rivelata dalla crio-EM
Per vedere come funziona a livello atomico, il team ha usato la criomicroscopia elettronica per catturare istantanee tridimensionali di TRPM5 in diverse condizioni. Hanno scoperto che CBTA si inserisce in una cavità precedentemente non osservata nella parte superiore di una regione sensibile alla tensione del canale, appena sopra il sito dove il calcio si lega di solito. Questa cavità, formata da un cluster di amminoacidi, funge da sito di ancoraggio preciso. Quando gli scienziati hanno mutato i componenti chiave che rivestono questa tasca, CBTA non è più stato in grado di attivare TRPM5, mentre il calcio continuava a funzionare, confermando che questa nicchia è essenziale per l’azione del composto. Colpisce che il legame di CBTA riorganizzi sottilmente parti vicine della proteina in modo da rendere molto più facile per il calcio occupare il suo sito abituale, spiegando la drammatica sinergia osservata nelle misure elettriche.
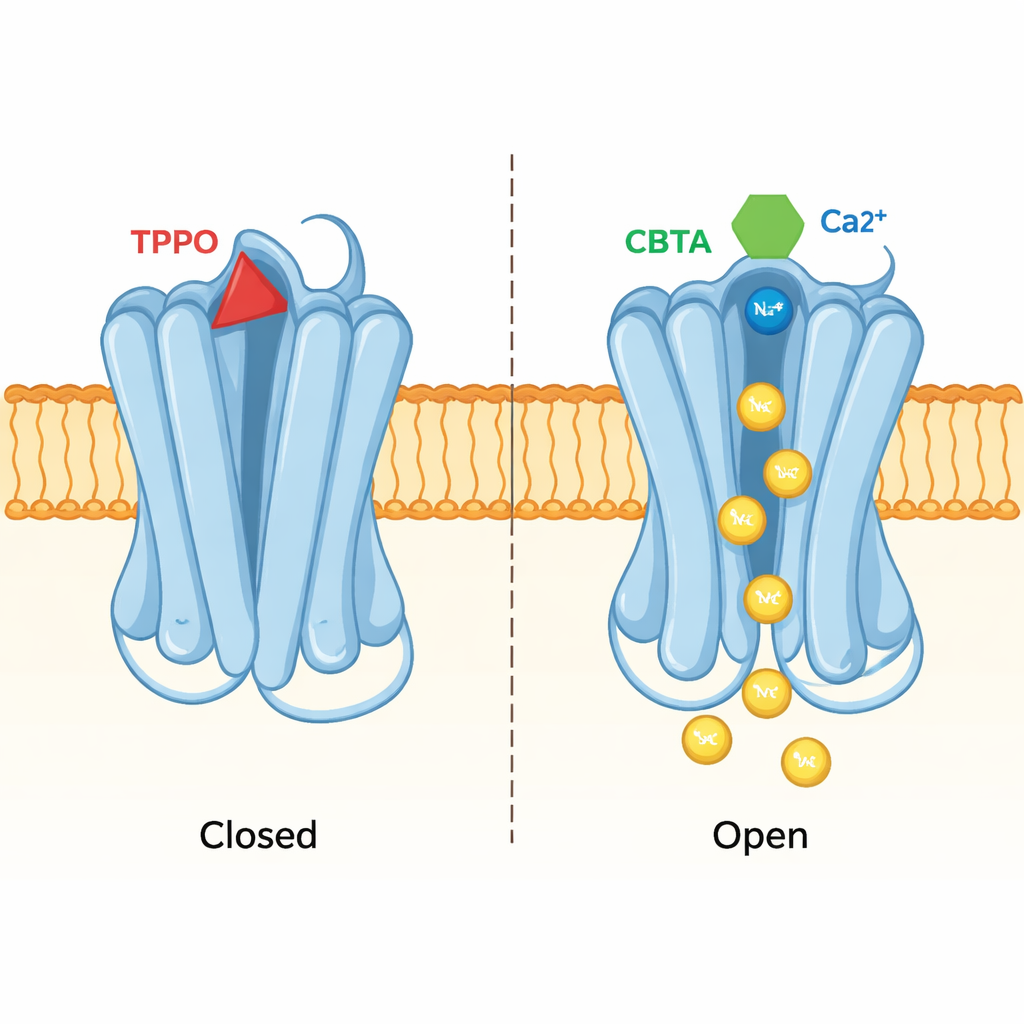
Una tasca, due risultati opposti
Lo stesso approccio strutturale ha rivelato come un inibitore chiamato TPPO utilizzi esattamente la stessa tasca per produrre l’effetto opposto. Quando TPPO si lega, entrambi i siti del calcio su TRPM5 restano occupati, ma il poro centrale del canale rimane contratto e non passa alcun ione. Il confronto tra le strutture legate a TPPO e a CBTA ha mostrato che le diverse forme dei due composti spingono segmenti proteici vicini in direzioni opposte. CBTA favorisce movimenti che si propagano fino al poro aprendolo; TPPO invece interrompe la comunicazione tra la tasca e il poro, mantenendo la porta chiusa. In sostanza, questa singola tasca può comportarsi sia da acceleratore sia da freno, a seconda della molecola che la occupa.
Rindirizzare i cablaggi interni del canale
Lo studio mostra inoltre che questa tasca di controllo può assumere funzioni normalmente svolte da una regione separata di legame del calcio sul lato interno della cellula. In canali mutanti in cui il solito sito interno per il calcio è disabilitato, il calcio da solo non riusciva ad aprire TRPM5. Eppure CBTA riusciva ancora ad attivare questi mutanti e a rimodellare un elemento strutturale chiave che collega le parti interne ed esterne del canale. In altri mutanti che interrompono la connessione tra il legame del calcio e l’apertura del poro, l’aggiunta di CBTA ha ristabilito un comportamento normale. Questi risultati rivelano che il sito appena identificato può riorientare o riparare la comunicazione tra domini diversi del canale, funzionando come un hub flessibile per la segnalazione a lungo raggio all’interno della proteina.
Perché questo è importante per i farmaci futuri
Per i non specialisti, il messaggio centrale è che i ricercatori hanno trovato una singola tasca sensibile ai farmaci su TRPM5 che può integrare attivazione, modulazione fine e spegnimento. Un piccolo attivatore come CBTA può sia imitare il calcio sia aumentare considerevolmente la sensibilità del canale, mentre un altro composto, TPPO, può bloccare lo stesso canale chiudendolo, tutto ancorandosi nello stesso punto. Questo quadro unificato del controllo di TRPM5 apre la strada alla progettazione di molecole su misura che ne aumentino o ne riducano l’attività in tessuti specifici, con potenziali applicazioni che vanno dal miglioramento di terapie basate sul gusto e farmaci per la motilità intestinale fino allo sviluppo di nuove strategie per gestire la glicemia e le malattie metaboliche.
Citazione: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Parole chiave: canale TRPM5, percezione del gusto, secrezione di insulina, apertura dei canali ionici, modulazione allosterica