Clear Sky Science · it
Analisi di associazione genome-wide dell’ipotiroidismo autoimmune rivelano contributi autoimmune e specifici per la tiroide e una relazione inversa con il rischio di cancro
Perché questo è importante per la salute quotidiana
Molte persone si sentono stanche, fredde o mentalmente annebbiati senza rendersi conto che la loro ghiandola tiroidea potrebbe essere la causa. L’ipotiroidismo autoimmune, in cui le difese dell’organismo attaccano lentamente la tiroide, colpisce più di una persona su venti. Questo studio utilizza dati genetici provenienti da centinaia di migliaia di volontari per rispondere a due grandi domande: quali variazioni ereditarie del nostro DNA rendono più probabile questa condizione e come sono collegate queste stesse variazioni al rischio di sviluppare il cancro? Le risposte rivelano un sorprendente compromesso tra un sistema immunitario che a volte danneggia la tiroide ma che può anche offrire una protezione aggiuntiva contro i tumori.
Uno sguardo sull’intero genoma
I ricercatori hanno combinato cartelle cliniche e informazioni genetiche provenienti da due grandi progetti di popolazione, FinnGen in Finlandia e UK Biobank nel Regno Unito. Si sono concentrati su persone che necessitavano di terapia sostitutiva a lungo termine con ormoni tiroidei ed hanno escluso con cura coloro le cui problematiche tiroidee erano dovute a interventi chirurgici, cancro o altre cause non autoimmuni. Questo ha prodotto oltre 81.000 casi di ipotiroidismo autoimmune e più di 700.000 controlli, rendendo lo studio il più ampio finora su questa condizione. Scandagliando milioni di marcatori del DNA in tutto il genoma, hanno individuato 418 segnali genetici indipendenti al di fuori del principale complesso genico immunitario, distribuiti in almeno 280 regioni del genoma. Molti di questi segnali riguardavano variazioni del DNA rare o a bassa frequenza che alterano la struttura delle proteine, offrendo indizi diretti sulla biologia sottostante.
Separare gli effetti immunitari generali da quelli specifici della tiroide
L’ipotiroidismo autoimmune si colloca all’incrocio tra l’autoimmunità generale e la biologia specifica della tiroide. Per distinguere questi componenti, il team ha confrontato i propri risultati con studi genetici di altre malattie autoimmuni e con i livelli ematici dell’ormone stimolante la tiroide (TSH), il marcatore clinico chiave usato per rilevare una tiroide ipoattiva. Utilizzando un metodo di classificazione bayesiano, hanno raggruppato i segnali genetici in quelli condivisi con ampie malattie autoimmuni e quelli più specifici della regolazione degli ormoni tiroidei. Hanno stimato che approssimativamente il 38% dei segnali agisce attraverso vie immunitarie generali che influenzano molte condizioni autoimmuni, mentre circa il 20% agisce principalmente tramite la funzione tiroidea. Le varianti focalizzate sulla tiroide tendevano a influenzare i livelli ormonali e geni attivi nel tessuto tiroideo, mentre le varianti dell’immunità generale risultavano più attive nelle cellule T, i globuli bianchi che orchestrano le risposte immunitarie.
Un focus su un interruttore immunitario chiave
Una scoperta particolarmente rilevante ha riguardato una rara variante del DNA nel gene ZAP70, che codifica una proteina di segnalazione chiave nelle cellule T. Difetti gravi in questa proteina sono noti per causare profonde immunodeficienze, ma la variante identificata qui produce solo una perdita parziale di funzione. Esperimenti di laboratorio su cellule T ingegnerizzate hanno mostrato che questo ZAP70 alterato indebolisce, ma non blocca completamente, la cascata di segnali che normalmente segue il riconoscimento di un bersaglio. Le cellule portatrici della variante erano meno capaci di attivare marcatori di attivazione e passaggi di segnalazione a valle. Questa risposta attenuata sembra alterare l’equilibrio delicato che normalmente elimina le cellule T autoreattive, predisponendo così i portatori a malattie autoimmuni e aumentando modestamente il loro rischio di alcune immunodeficienze.
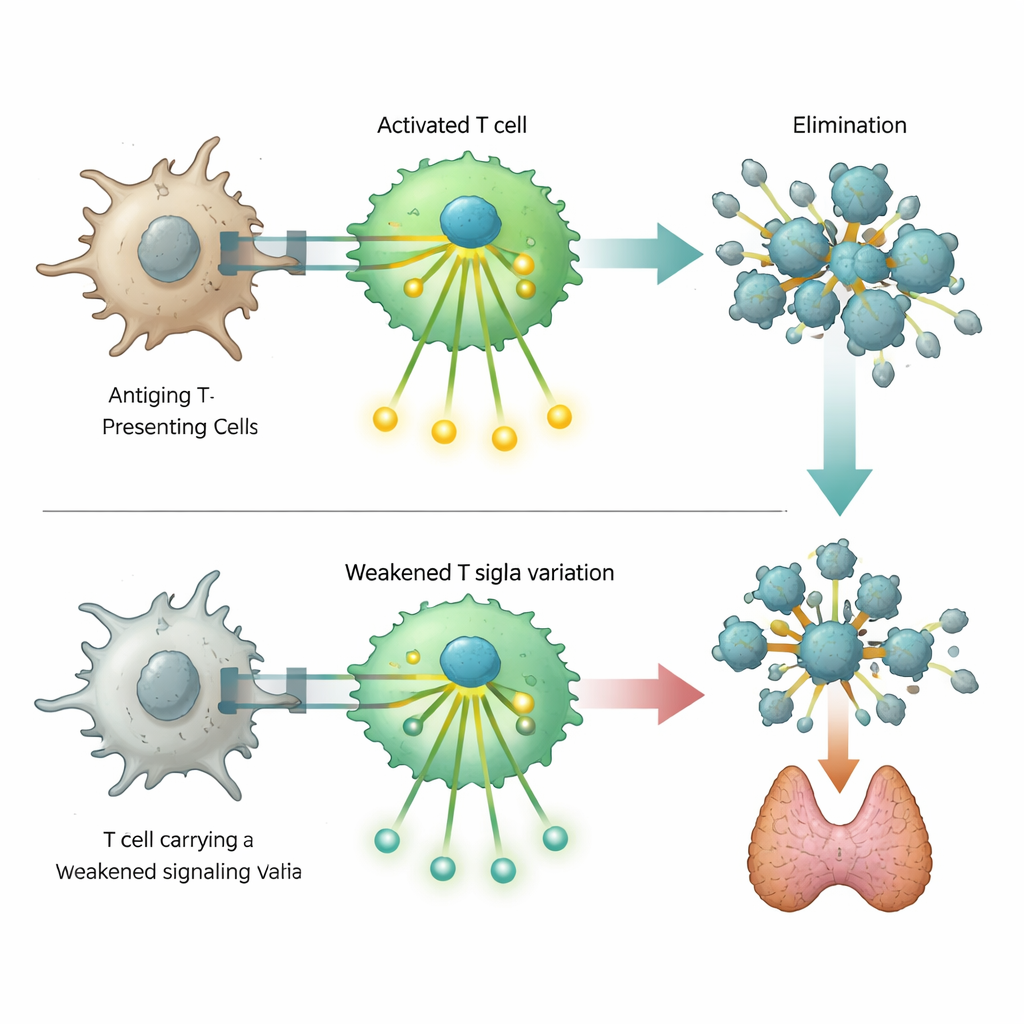
Un legame inatteso con la protezione dal cancro
Poiché le stesse vie immunitarie che guidano l’autoimmunità possono anche attaccare i tumori, gli autori hanno poi indagato come la genetica dell’ipotiroidismo autoimmune si relazioni al rischio di cancro. Hanno calcolato un punteggio di rischio poligenico che riassume la tendenza ereditaria di ciascuna persona all’ipotiroidismo e ne hanno testato l’associazione con molte malattie nei dati finlandesi. Come previsto, un punteggio più alto si associava a un rischio maggiore di varie condizioni autoimmuni. Più sorprendente è stato un andamento coerente di rischio inferiore per diversi tumori, in particolare carcinoma basocellulare e altri tumori della pelle, ma anche cancro al seno e alla prostata e un raggruppamento complessivo “tutti i tumori”. Quando il team ha esaminato direttamente gli studi genome-wide sul cancro, circa il 10% dei siti legati all’ipotiroidismo influenzava anche il cancro della pelle, con la stessa variante genetica che generalmente aumentava l’autoimmunità tiroidea diminuendo al contempo il rischio di cancro cutaneo. Queste varianti condivise erano concentrate in geni legati al sistema immunitario, inclusi noti target farmacologici usati nell’immunoterapia di checkpoint.
Cosa significa per i pazienti e la medicina
Visto in termini semplici, questo lavoro mostra che alcune persone nascono con sistemi immunitari leggermente più "attivi", che le rendono più suscettibili a danni lenti e spesso silenti alla ghiandola tiroidea ma allo stesso tempo meglio attrezzate per individuare ed eliminare tumori emergenti. Lo studio distingue quali cambiamenti genetici agiscono tramite un’eccessiva attività immunitaria generale e quali influenzano specificamente la produzione di ormoni tiroidei, spiegando perché condizioni come la malattia di Hashimoto e la malattia di Graves possono condividere alcuni geni di rischio pur spingendo la funzione tiroidea in direzioni opposte. Aiuta anche a spiegare perché i pazienti che sviluppano problemi tiroidei durante trattamenti oncologici che potenziano il sistema immunitario spesso rispondono meglio a quei trattamenti. Nel complesso, i risultati suggeriscono che variazioni comuni e naturali in geni di checkpoint e di segnalazione immunitaria modellano sia la malattia autoimmune tiroidea sia il rischio di cancro nel corso della vita, offrendo nuovi spunti per la prevenzione e un uso più personalizzato delle immunoterapie.
Citazione: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Parole chiave: ipotiroidismo autoimmune, malattie della tiroide, rischio genetico, sistema immunitario, protezione dal cancro