Clear Sky Science · it
Analisi di associazione genome-wide evidenziano il ruolo dell’ambiente molecolare intestinale nella variazione del microbiota umano
Perché il tuo DNA e i batteri intestinali fanno parte della stessa storia
Trilioni di microbi vivono nel nostro intestino e influenzano tutto, dalla digestione al metabolismo e persino il sistema immunitario. Ma perché alcune persone ospitano naturalmente composizioni diverse di batteri intestinali rispetto ad altre, anche quando vivono nello stesso posto e mangiano cibi simili? Questo studio, basato su dati genetici dettagliati e sul microbiota di quasi 30.000 adulti in Svezia e Norvegia, mostra che il nostro DNA contribuisce in modo discreto a scrivere la comunità microbica che vive dentro di noi.
Uno sguardo massiccio negli intestini nordici
Per scoprire come i geni umani modellino il microbioma, i ricercatori hanno combinato i dati di quattro grandi studi di popolazione svedesi, comprendenti 16.017 adulti, e hanno verificato i risultati in 12.652 norvegesi. Tutti i partecipanti hanno fornito sangue per l’analisi del DNA umano e campioni di feci per il sequenziamento profondo del DNA microbico. Invece di concentrarsi solo su ampi gruppi batterici, il gruppo ha usato metodi ad alta risoluzione in grado di distinguere centinaia di specie individuali. Hanno quindi scandagliato il genoma umano, variante dopo variante, per vedere quali tratti di DNA si associavano alla ricchezza microbica complessiva (quante specie diverse sono presenti) e alla presenza o abbondanza di specie batteriche specifiche.
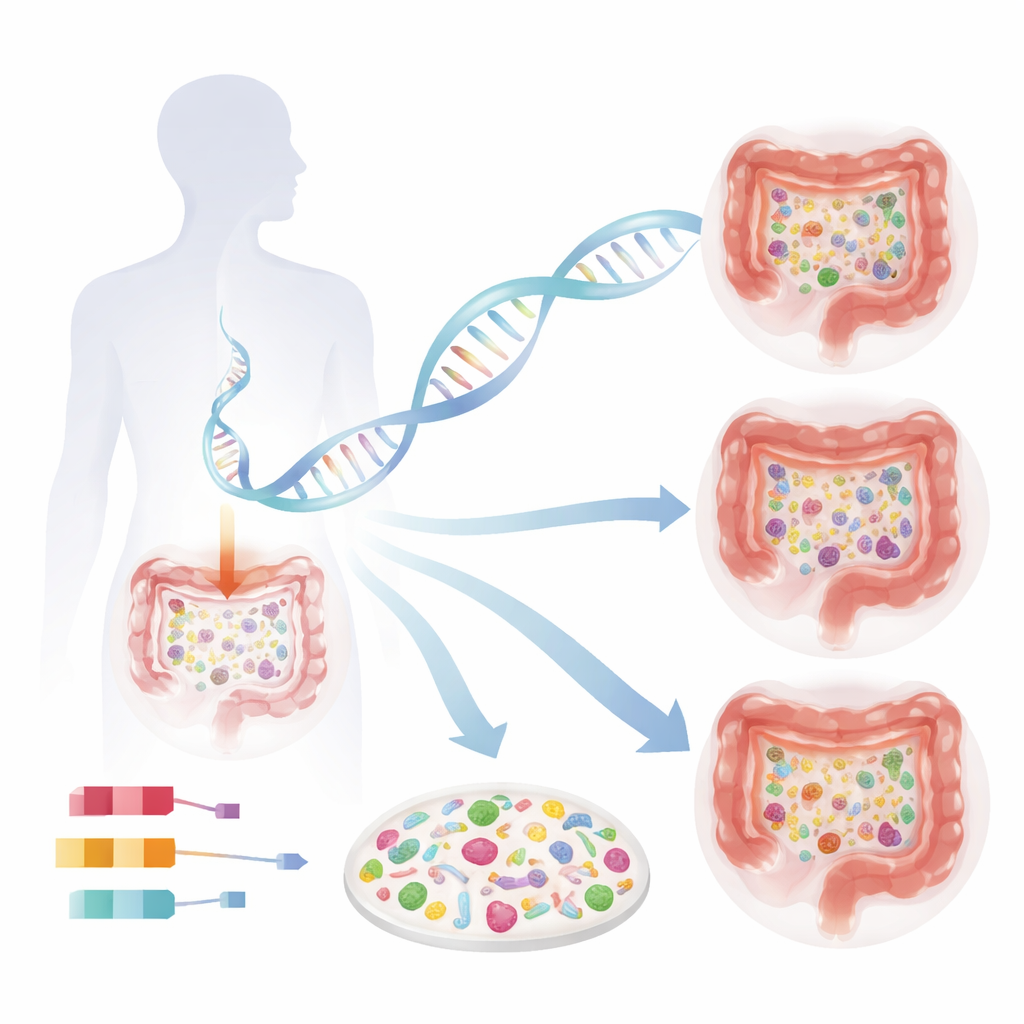
Interruttori genetici che modulano la ricchezza microbica
Una delle scoperte più sorprendenti è stata una regione del genoma umano contenente due geni, OR51E1 e OR51E2, noti in precedenza come recettori degli odori. Questi recettori si trovano anche su cellule speciali produttrici di ormoni nel rivestimento intestinale e rilevano acidi grassi prodotti dai microbi. Le persone portatrici di una particolare versione di questa regione di DNA tendevano ad avere meno specie batteriche nell’intestino, e questo schema è stato confermato in modo indipendente nel gruppo norvegese. La scoperta suggerisce che il modo in cui le cellule intestinali percepiscono gli acidi grassi microbici ricade sulla diversità del microbioma stesso, forse modificando ormoni intestinali che regolano la motilità, l’appetito o le risposte immunitarie locali.
Zuccheri di superficie, muco e il quartiere microbico
Lo studio ha anche individuato diverse regioni genetiche che regolano l’ambiente zuccherino e mucoso sulla superficie intestinale — spazi privilegiati per i batteri. Varianti nel noto gene della lattasi (LCT), che determina se gli adulti possono digerire lo zucchero del latte, erano legate a cambiamenti in più specie, incluso Bifidobacterium che prospera con il lattosio. Geni che definiscono i gruppi sanguigni e lo stato di “secretore” correlato — ABO, FUT2 e FUT3–FUT6 — modificano gli zuccheri contenenti fucosio esposti sul muco intestinale e nelle secrezioni. Diverse combinazioni genetiche qui erano collegate a insiemi distinti di batteri che possono aderire a questi zuccheri o nutrirsene. Un’altra regione chiave ricadeva all’interno di un gene delle mucine, MUC12, parte dell’impalcatura del rivestimento mucoso stesso. Variazioni in questa regione si associavano all’abbondanza di una specie chiamata Coprobacillus cateniformis e condividevano persino un segnale genetico con la frequenza di evacuazione intestinale, suggerendo effetti intrecciati su funzione intestinale e composizione microbica.
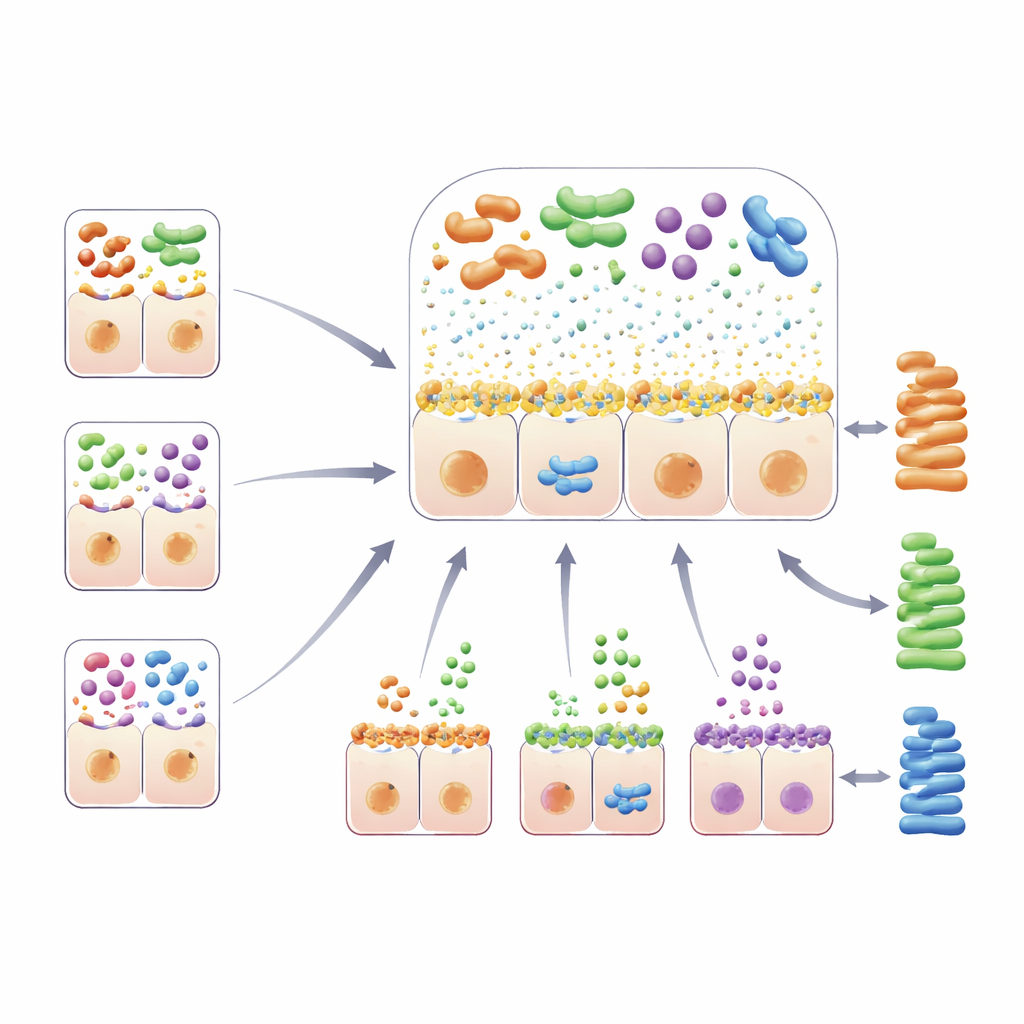
Dai microbi al metabolismo e alla forma corporea
Oltre a mappare “chi vive lì”, il team ha chiesto se le regioni del DNA legate a certi batteri si sovrapponessero anche a tratti umani come colesterolo nel sangue, acidi biliari e distribuzione del grasso corporeo. In diversi casi gli stessi segmenti del genoma erano coinvolti. Varianti vicino ai geni CORO7–HMOX2 e FOXP1 influenzavano un gruppo di batteri includendo Turicibacter e Clostridium saudiense, e si allineavano anche con differenze nel rapporto vita-fianchi, negli acidi biliari e nel colesterolo LDL (a bassa densità). Usando strumenti genetici progettati per suggerire relazioni causali, gli autori hanno trovato indizi che un microbo, una specie di Intestinibacter, possa aumentare il colesterolo LDL, e che Turicibacter potrebbe influenzare dove il grasso corporeo viene immagazzinato. Un’altra regione, SLC5A11, era legata a un batterio produttore di butirrato, Agathobaculum butyriciproducens, che ha mostrato effetti protettivi in modelli animali di malattie cerebrali. Qui, la variante del DNA umano sembrava abbassare i livelli ematici di una piccola molecola chiamata mio-inositolo favorendo al contempo la crescita di questo microbo potenzialmente utile.
Cosa significa per la salute e per terapie future
Nel complesso, questi risultati mostrano che geni umani coinvolti nella sensazione intestinale, nella composizione del muco e negli zuccheri di superficie aiutano a determinare quali specie microbiche possano insediarsi con successo nel nostro intestino. Gli effetti sono modesti per ogni singolo gene, e il quadro finora è più chiaro per batteri relativamente comuni in persone di ascendenza europea. Tuttavia, il lavoro amplia l’elenco delle regioni del DNA umano collegate in modo affidabile a specifici microbi intestinali da poche a almeno otto, e collega diverse di esse a tratti metabolici come il colesterolo e la distribuzione del grasso corporeo. Per il lettore non specialistico, il messaggio chiave è che il microbioma intestinale non è plasmato solo dalla dieta e dall’ambiente: il nostro progetto genetico costruisce l’habitat che i microbi incontrano, spingendo la comunità verso alcuni residenti e lontano da altri. Con studi più ampi e diversificati, comprendere questa relazione bidirezionale tra geni e microbi potrebbe aiutare a personalizzare consigli dietetici, prevedere rischi di malattia e forse guidare terapie che combinano farmaci, alimentazione e manipolazione mirata del microbioma.
Citazione: Dekkers, K.F., Pertiwi, K., Baldanzi, G. et al. Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation. Nat Genet 58, 540–549 (2026). https://doi.org/10.1038/s41588-026-02512-2
Parole chiave: microbioma intestinale, genetica umana, muco intestinale, acidi biliari, metabolismo