Clear Sky Science · it
GlycoRNA complessi con eparan solfato regolano la segnalazione di VEGF-A
Come le cellule modulano con precisione i segnali per i vasi sanguigni
I vasi sanguigni non spuntano semplicemente dove compaiono segnali di crescita: devono essere controllati con precisione per nutrire i tessuti senza alimentare tumori o causare cecità. Questo studio scopre un inaspettato “freno” su un importante segnale che promuove la formazione dei vasi, chiamato VEGF-A. Gli autori mostrano che piccoli frammenti di RNA, esposti sulla superficie delle cellule in associazione con zuccheri e proteine, possono attenuare il messaggio di VEGF-A, rimodellando il modo in cui pensiamo al linguaggio che le cellule usano alla loro superficie.
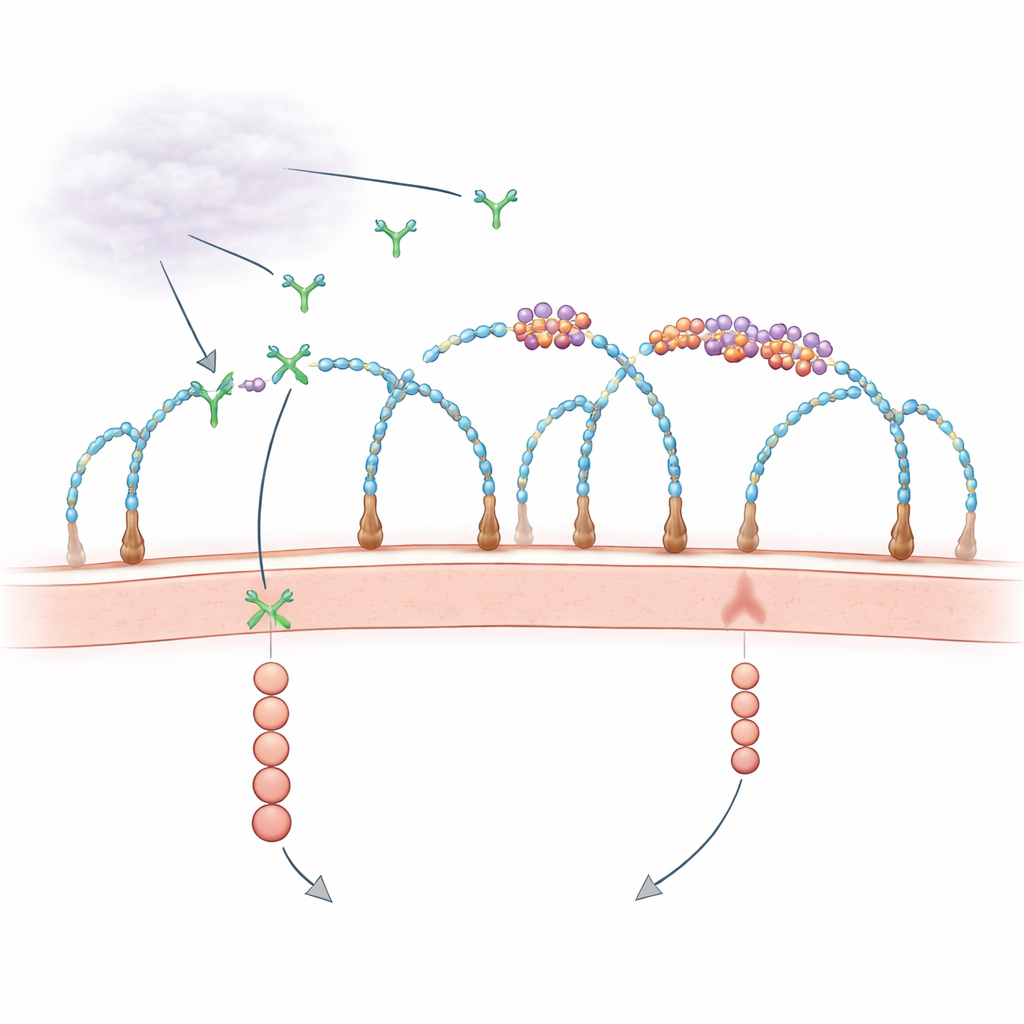
Un ruolo sorprendente per l’RNA sulla superficie cellulare
Per decenni, i biologi hanno saputo che il rivestimento esterno della cellula, ricco di proteine decorate da zuccheri chiamate proteoglicani dell’eparan solfato, aiuta a catturare i fattori di crescita e a presentarli ai loro recettori. Allo stesso tempo, osservazioni sporadiche suggerivano che frammenti di RNA al di fuori delle cellule potessero influenzare la crescita dei vasi sanguigni, ma i protagonisti e i meccanismi erano poco chiari. Lavori recenti hanno rivelato che alcuni piccoli RNA sono legati chimicamente a zuccheri complessi formando i “glycoRNA”, e che certe proteine leganti l’RNA compaiono anch’esse sulla superficie cellulare, raggruppandosi con questi RNA. Il nuovo studio pone una domanda precisa: questi minuscoli isolotti di RNA–proteina sulla membrana controllano davvero il modo in cui segnali di crescita come VEGF-A vengono ricevuti?
Costruire isolotti di RNA–proteina con catene zuccherine
Usando schermate di knockout CRISPR sull’intero genoma e microscopia ad alta risoluzione, i ricercatori hanno scoperto che specifiche catene zuccherine—eparan solfato con particolari decorazioni di solfato—sono impalcature essenziali per assemblare questi ammassi di RNA–proteina, che chiamano ribonucleoproteine sulla superficie cellulare (csRNP). Quando enzimi chiave che sintetizzano o solfatano l’eparan solfato venivano rimossi, gli ammassi di glycoRNA e delle loro proteine partner sparivano dalla superficie cellulare, pur essendo ancora presenti all’interno delle cellule. Enzimi che recidono le catene di eparan solfato dalla superficie o agenti chimici che bloccano la solfatazione avevano lo stesso effetto. Questi risultati mostrano che catene di eparan solfato integre e correttamente solfatate organizzano le csRNP in isolotti nanoscopici sulla membrana.
Gli ammassi di RNA agiscono come freni su un potente segnale pro-vascolare
Il gruppo si è poi concentrato su cellule endoteliali umane, che rivestono i vasi e rispondono a VEGF-A. Hanno scoperto che anche queste cellule espongono ammassi csRNP ancorati all’eparan solfato. Trattare cellule vive con RNasi, enzimi che degradano l’RNA, rimosse la componente RNA senza disturbare le catene zuccherine sottostanti. In tali condizioni, la forma più comune di VEGF-A che si lega all’eparan (VEGF-A165) provocò un’attivazione molto più intensa della via di segnalazione ERK a valle, mentre una forma più corta priva della coda che lega l’eparan (VEGF-A121) rimase inalterata. Dopo la rimozione dell’RNA, più molecole di VEGF-A165 si legarono alla superficie cellulare, anche se i livelli di recettore rimasero gli stessi. In dispositivi microfluidici 3D, le cellule endoteliali esposte a RNasi crescevano più avanti nei gel di collagene e formavano strutture tubolari in modo più robusto, indicando che la distruzione dell’RNA di superficie libera un comportamento pro-angiogenico.
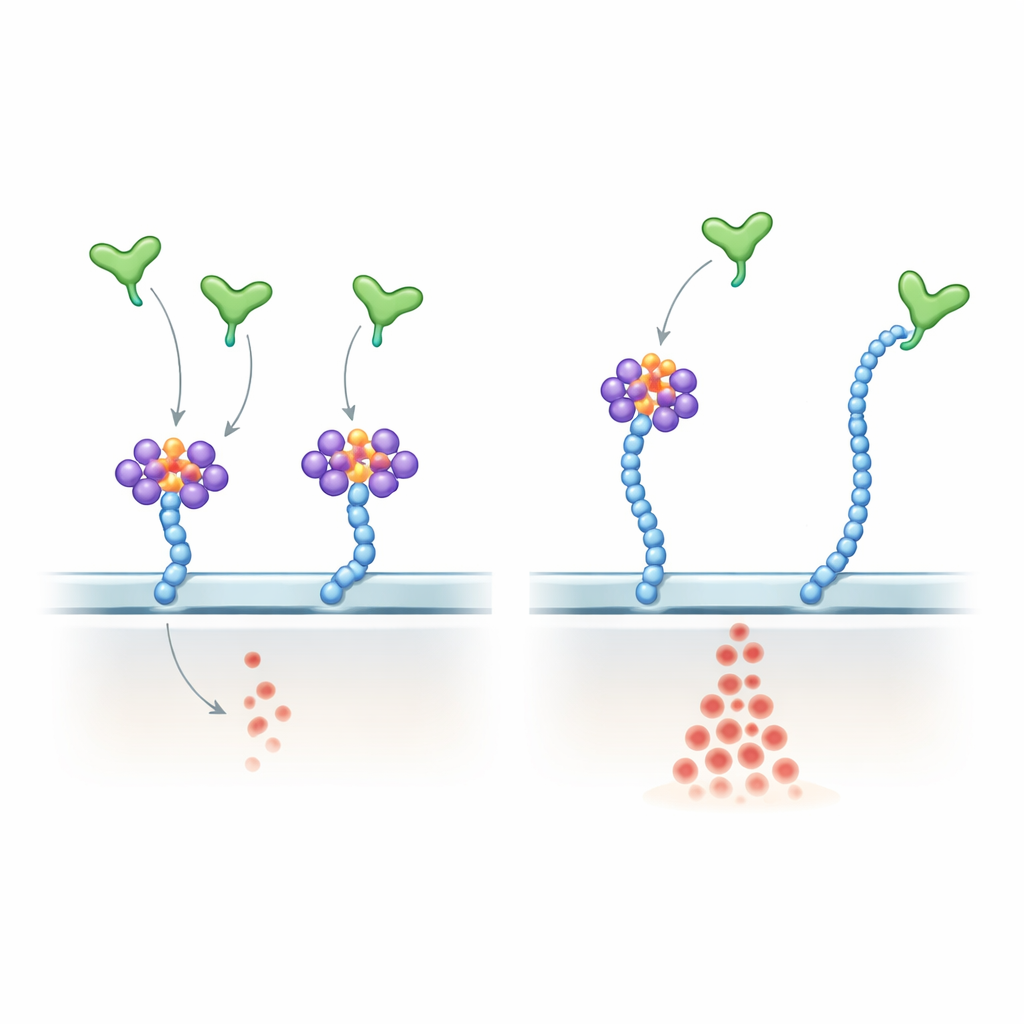
Dissezionare come VEGF-A percepisce RNA e zuccheri
Per sondare il meccanismo, gli autori mostrarono che VEGF-A165 si lega direttamente a specifici piccoli RNA, inclusi molti glycoRNA noti, attraverso la sua regione C-terminale carica positivamente—la stessa regione che lega l’eparan solfato. Hanno ingegnerizzato una versione sottile di VEGF-A165 in cui residui chiave di arginina in questa coda sono stati sostituiti con lisine. Questo mutante mantenne la carica positiva complessiva e continuò ad agganciare le catene di eparan solfato, ma legava male i glycoRNA e divenne in gran parte insensibile al trattamento con RNasi. Nelle cellule endoteliali, il mutante provocò un’attivazione di ERK più forte e più resistente alle RNasi rispetto al VEGF-A165 normale, rispecchiando da vicino l’effetto della rimozione dell’RNA dalla superficie cellulare. In topi vivi, l’iniezione del mutante nell’occhio causò una crescita vascolare retinica più esuberante rispetto alla proteina normale. In embrioni di zebrafish, la sovraespressione della versione mutante di Vegfa disturbò il normale pattern vascolare e aumentò il numero di cellule endoteliali.
Dal meccanismo di base alle implicazioni più ampie
Infine, gli autori mostrarono che fondere la coda di VEGF-A che lega l’eparan a una proteina segnale non correlata, Wnt3a, poteva reindirizzare l’attività di Wnt: attaccare la coda normale riduceva i cambiamenti di sviluppo indotti da Wnt, mentre attaccare la coda insensibile all’RNA li aumentava. Insieme, questi esperimenti supportano un modello per cui gli ammassi csRNP, ancorati da eparan solfato specificamente solfatato, legano VEGF-A e fattori correlati per temperarne l’attività. Quando la componente RNA viene rimossa o quando i fattori di crescita perdono la capacità di percepire l’RNA, l’equilibrio si sposta verso una segnalazione più intensa e uno sviluppo vascolare alterato in più specie.
Perché questo è importante per la salute e le terapie future
Per un non specialista, il messaggio chiave è che le cellule usano non solo proteine e zuccheri, ma anche piccoli RNA esposti sulla loro superficie per modulare con finezza potenti segnali di crescita come VEGF-A. Questi ammassi di RNA–proteina ancorati agli zuccheri agiscono come freni regolabili sulla formazione dei vasi, aiutando a garantire che i nuovi vasi germoglino dove e quando necessario. Disgregare questo equilibrio—degradando l’RNA di superficie o alterando le proprietà di legame dell’RNA dei fattori di crescita—può esagerare o deviare la crescita vascolare. Comprendere questo livello di controllo appena rivelato potrebbe aprire la strada a terapie che modulano con maggiore precisione l’angiogenesi in senso aumentativo o riduttivo nel cancro, nelle malattie oculari, nella guarigione delle ferite e nella medicina rigenerativa, mirando agli RNA di superficie, alle loro impalcature zuccherine o alle regioni di riconoscimento dell’RNA dei fattori di crescita.
Citazione: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Parole chiave: angiogenesi, fattore di crescita endoteliale vascolare, eparan solfato, RNA sulla superficie cellulare, glycoRNA