Clear Sky Science · it
Analisi sistematiche della mobilizzazione dei lipidi da parte delle proteine di trasferimento lipidico umane
Come le cellule tengono in ordine i loro grassi
Ogni cellula del tuo corpo è avvolta da membrane ricche di lipidi, e migliaia di diversi grassi aiutano queste membrane a svolgere funzioni che vanno dall’invio di segnali alla gestione dell’energia. Ma questi lipidi non sono distribuiti a caso: ogni compartimento interno della cellula ha la sua miscela caratteristica. Questo studio pone una domanda semplice ma di vasta portata: come fanno le cellule a portare i grassi giusti nel posto giusto al momento giusto, e cosa succede quando questo sistema si guasta?
Proteine che trasportano i grassi
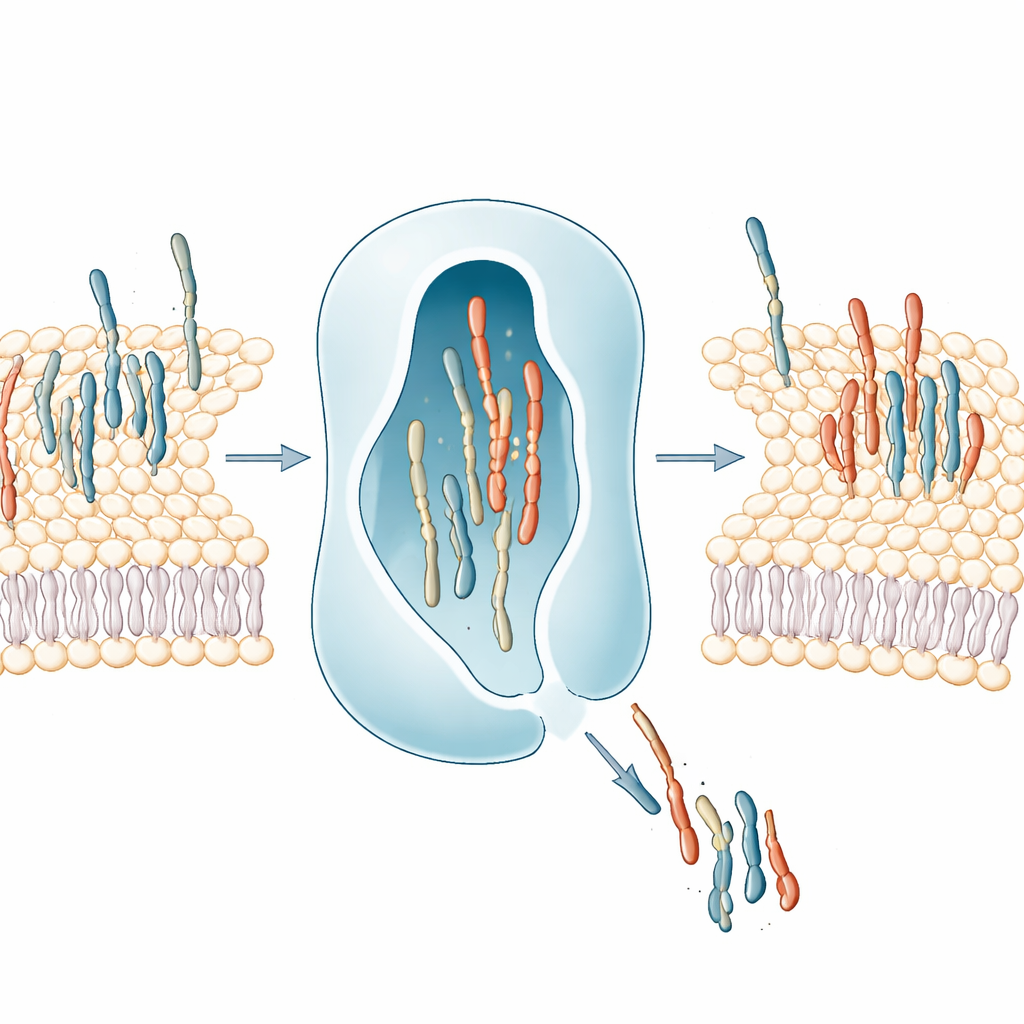
Le cellule si affidano a una grande famiglia di molecole chiamate proteine di trasferimento lipidico, o LTP, che possono staccare una molecola lipidica da una membrana, proteggere il suo corpo oleoso all’interno di una tasca e consegnarla a un’altra membrana. Molte LTP umane sono collegate a malattie come il cancro e disturbi neurologici, eppure per la maggior parte di esse non sapevamo quali lipidi effettivamente trasportino. Gli autori si sono proposti di costruire una mappa sistematica di quali LTP umane legano quali lipidi e di come l’aumento dell’attività di queste LTP rimodelli l’insieme dei lipidi all’interno di una cellula.
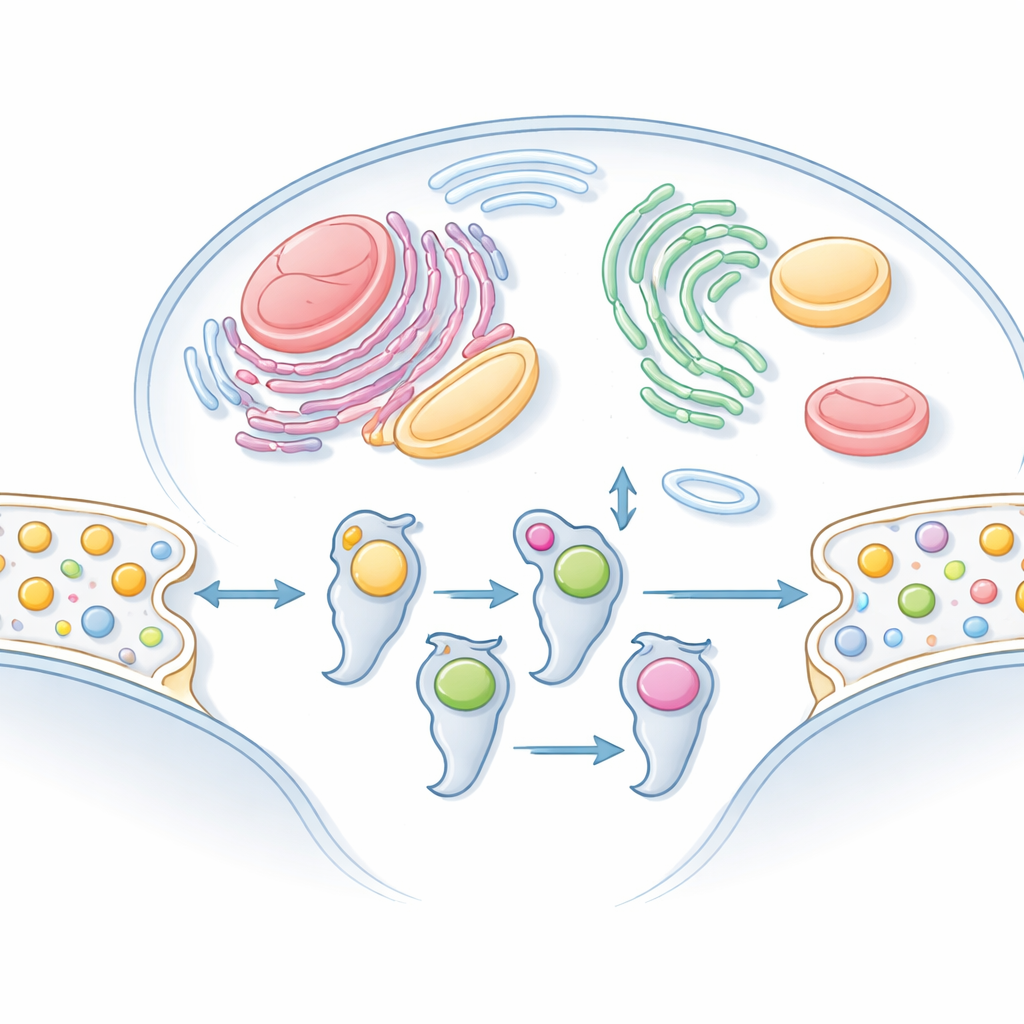
Costruire una mappa su larga scala dello scambio di lipidi
Per farlo, il team ha clonato 101 LTP umane e le ha espresse in due contesti diversi. In cellule di origine umana hanno permesso a ciascuna LTP di assemblarsi con i lipidi naturalmente presenti. In condizioni in vitro hanno miscelato LTP purificate con membrane artificiali ricavate da estratti tissutali animali. Hanno quindi purificato più di 100 complessi LTP–lipide e identificato i lipidi legati mediante spettrometria di massa sensibile. Abbinando segnali proteici e lipidici attraverso molteplici fasi di separazione, hanno filtrato i trasporti accidentali e mantenuto solo i lipidi che viaggiavano con affidabilità con ciascuna LTP. Il risultato è stato un catalogo di partner lipidici che copre nove grandi famiglie di LTP.
Nuovi carichi e nuove regole
Questa mappa ha confermato partner noti — come la vitamina A per le sue proteine vettore — ma ha anche rivelato carichi nuovi e talvolta sorprendenti. Un LTP chiamato HSDL2, collegato a disturbi dello stoccaggio dei grassi, è stato trovato a mobilitare triacilgliceroli, gli stessi lipidi neutri che riempiono le cellule adipose. Altri LTP legavano lipidi segnalatori come il diacilglicerolo, o un gruppo speciale di lipidi “eteri” prodotti da una via biosintetica distinta. Molte LTP si sono rivelate capaci di gestire più di una classe di lipidi, suggerendo che svolgono doppi ruoli: possono muovere il loro carico principale mentre gestiscono anche lipidi ausiliari che guidano il processo di scambio o modulano il metabolismo. Quando i ricercatori hanno costretto le cellule a sovraprodurre singole LTP, i livelli sia dei partner lipidici noti sia di quelli appena scoperti sono cambiati in modi prevedibili, dimostrando che i carichi mappati non sono artefatti di laboratorio ma funzionano nelle cellule vive.
Perché solo alcuni grassi sono mobili
Analizzando l’intero set di dati, gli autori hanno notato che le LTP non trattano tutte le versioni di un dato lipide allo stesso modo. Hanno mostrato chiare preferenze per lipidi con code più corte e con una o due doppi legami chimici in quelle code. Questi grassi creano piccole imperfezioni nelle membrane che ne facilitano l’estrazione, mentre code molto rigide o fortemente piegate sono più difficili da rimuovere. Alcune LTP sono andate oltre e hanno favorito pattern di code estremamente specifici. Per esempio, il trasportatore di ceramide CERT preferiva ceramidi con determinate lunghezze di catena, incluse specie molto lunghe e rare che contribuiscono a formare domini di membrana molto compatti. Un altro gruppo, le proteine di trasferimento della fosfatidilinositolo, preferiva una specie che porta una coda di acido arachidonico, un precursore di molti segnali simili ad ormoni. Simulazioni al computer delle strutture delle LTP hanno rivelato come ammassi di particolari amminoacidi all’interno delle tasche di legame creino incastri perfetti per queste code selezionate.
Lipidi collegati e comportamento cellulare coordinato
Lo studio ha anche indagato se i diversi lipidi trasportati dalla stessa LTP siano correlati nella vita della cellula. Confrontando la loro mappa con ampi dataset esistenti, gli autori hanno scoperto che i lipidi gestiti dalla stessa LTP tendono a salire e scendere insieme quando il metabolismo è perturbato e tendono ad apparire negli stessi luoghi all’interno di cellule e tessuti. Ciò suggerisce che le LTP aiutino a coordinare gruppi di lipidi che lavorano insieme, piuttosto che spostare molecole isolate. In altre parole, ogni LTP potrebbe definire una piccola “rete” di grassi che viaggiano e agiscono come un’unità.
Perché questo è importante per salute e malattia
Per i non specialisti, il messaggio chiave è che le cellule non si limitano a sintetizzare i grassi giusti; devono anche trasportare specie lipidiche accuratamente selezionate verso le membrane corrette, e lo fanno con un set di strumenti di trasferimento sorprendentemente versatile. Questo lavoro offre la prima mappa ampia e sperimentalmente fondata di quali LTP umane trasportano quali lipidi, e rivela regole semplici — come una preferenza per certe lunghezze di coda e gradi di insaturazione — che decidono quali membri dell’enorme pool lipidico sono effettivamente mobili. Poiché molte LTP e i loro partner lipidici sono legati al cancro, alle risposte immunitarie e alla funzione cerebrale, questa risorsa offre un punto di partenza per comprendere come cambiamenti sottili nel traffico lipidico possano riverberare nella malattia e per progettare terapie future che indirizzino questi trasportatori microscopici verso rotte più salutari.
Citazione: Titeca, K., Chiapparino, A., Hennrich, M.L. et al. Systematic analyses of lipid mobilization by human lipid transfer proteins. Nature 651, 511–520 (2026). https://doi.org/10.1038/s41586-025-10040-y
Parole chiave: proteine di trasferimento lipidico, membrane cellulari, lipidomica, metabolismo delle membrane, trasporto del ceramide