Clear Sky Science · it
Il sequenziamento su scala di popolazione chiarisce i determinanti della persistenza del DNA di EBV
Perché un virus comune è ancora importante
La maggior parte degli adulti porta con sé il virus di Epstein–Barr (EBV), spesso senza nemmeno saperlo. Per alcuni, però, questo passeggero silenzioso è collegato a malattie che vanno dalla mononucleosi a tumori e patologie autoimmuni. Questo studio pone una domanda semplice ma di ampio respiro: possiamo usare le enormi raccolte di dati genetici già disponibili per vedere chi ha più EBV nel sangue e se i loro geni aiutano a determinare chi mantiene il virus sotto controllo e chi no?
Leggere un’impronta virale nascosta nel nostro DNA
Le biobanche moderne, come la UK Biobank e il programma statunitense All of Us, hanno sequenziato il DNA completo di centinaia di migliaia di volontari. Questi progetti si sono concentrati sui geni umani, ma i dati grezzi contengono anche frammenti di DNA virale. I ricercatori hanno notato che il genoma umano di riferimento usato per l’allineamento include una “cromosoma” aggiuntiva per EBV. Riesaminando le letture che si mappavano su questo segmento EBV, hanno potuto stimare quante copie del genoma di EBV fossero presenti nel sangue di ciascuna persona al momento del prelievo. Dopo aver accuratamente mascherato alcune regioni ripetitive fuorvianti, hanno definito come aventi “DNAemia da EBV” le persone con livelli chiaramente rilevabili—una quantità misurabile di DNA di EBV circolante nel sangue.
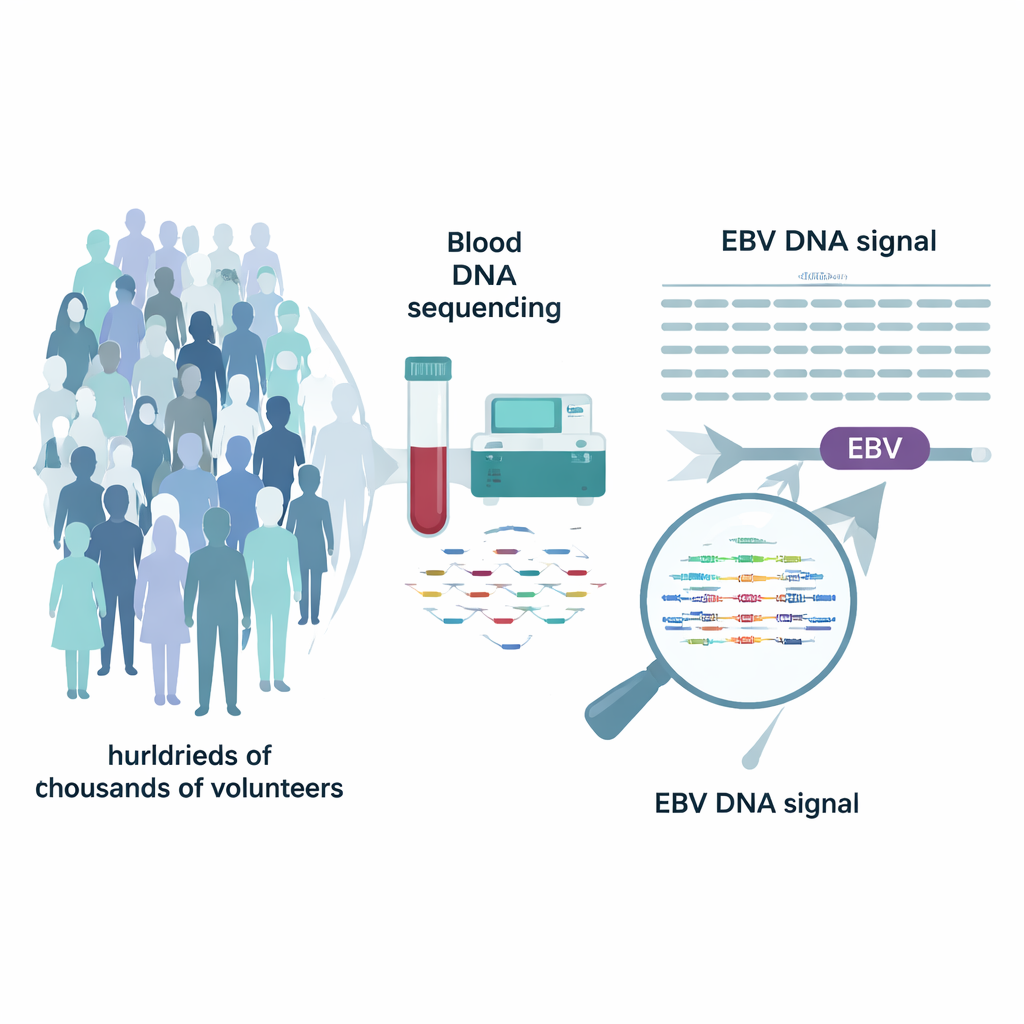
Una piccola minoranza porta un carico virale elevato
Analizzando quasi mezzo milione di persone nella UK Biobank e un quarto di milione in All of Us, il gruppo ha scoperto che la maggior parte degli adulti non aveva DNA di EBV rilevabile nel sangue, nonostante oltre il 90% mostrasse prove di infezione passata nei test degli anticorpi. Circa il 10% dei partecipanti, tuttavia, rientrava nella coda della distribuzione con livelli chiaramente elevati di DNA di EBV. Questi individui tendevano ad essere più anziani, più spesso di sesso maschile e leggermente più propensi a prendere farmaci immunosoppressori. Schemi simili sono apparsi in entrambe le coorti e, in un set separato di campioni di saliva, il virus era molto più comune, evidenziando che EBV risiede in diversi serbatoi nel corpo e che le misure nel sangue catturano solo uno di essi.
Collegamenti tra persistenza virale e malattia
Con questo nuovo biomarcatore a disposizione, gli autori hanno indagato come la persistenza del DNA di EBV nel sangue si relazioni alla salute. Hanno scandagliato migliaia di codici diagnostici e misurazioni di laboratorio per vedere quali fossero più comuni nelle persone con DNAemia da EBV. Sono emerse forti associazioni con condizioni già sospettate di essere legate a EBV, tra cui linfoma di Hodgkin, artrite reumatoide, lupus, broncopneumopatia cronica ostruttiva e alcuni tumori polmonari. Sono emersi anche segnali per problemi cardiovascolari, insufficienza renale, depressione e affaticamento, e collegamenti suggeriti a rari disturbi neurologici come la neuromielite ottica. Molti di questi pattern sono stati riprodotti nella coorte indipendente All of Us. Lo studio non può provare che EBV causi questi problemi, ma mostra che alti livelli di DNA di EBV nel sangue sono un marcatore di rischi sanitari più ampi e di alterazioni del sistema immunitario.
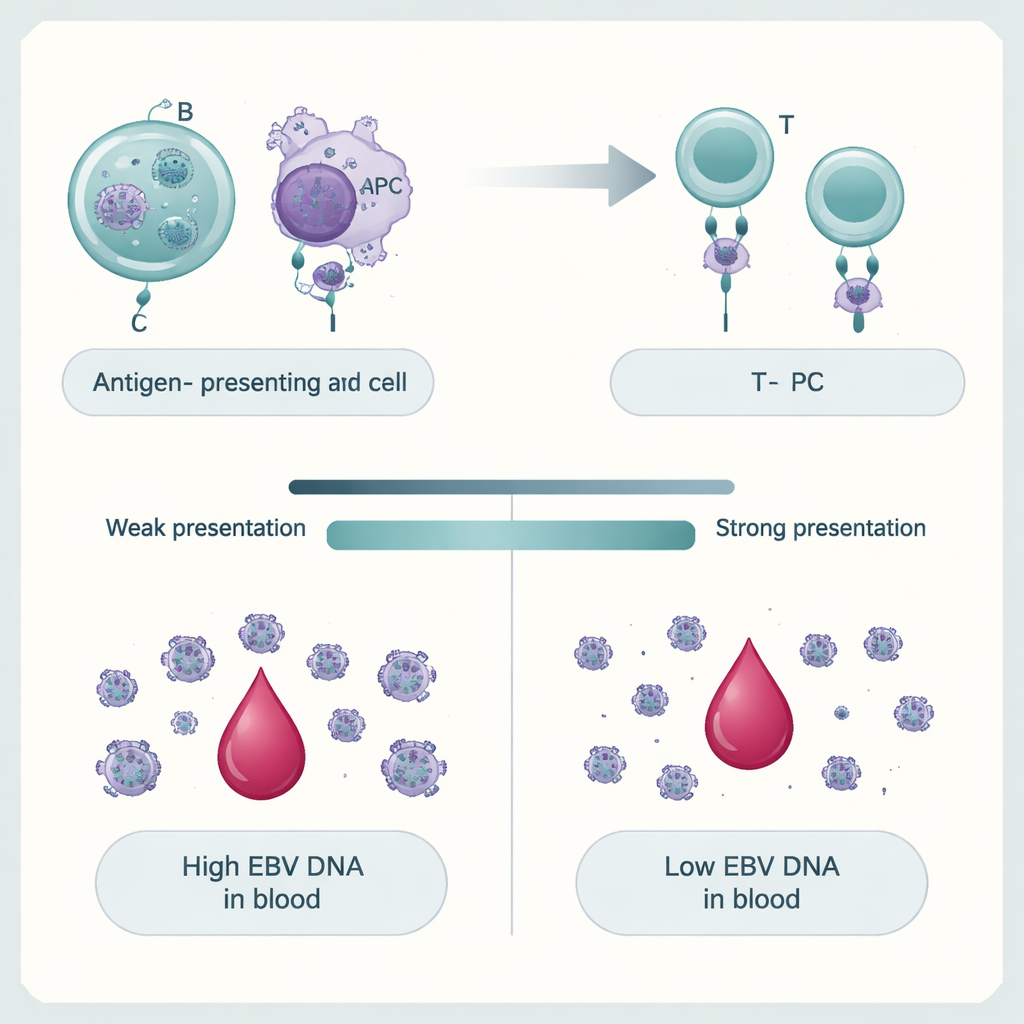
Come i nostri geni plasmano il controllo del virus
Il gruppo ha poi chiesto perché solo alcune persone presentino livelli elevati di DNA di EBV. Scansionando milioni di varianti genetiche nel genoma, hanno mostrato che la DNAemia da EBV è un tratto poligenico: molte piccole differenze del DNA insieme spostano i livelli virali verso l’alto o verso il basso. I segnali più forti si sono concentrati dentro e intorno ai geni del complesso maggiore di istocompatibilità (MHC), che aiutano le cellule immunitarie a mostrare frammenti virali alle cellule T. Varianti che alterano queste proteine, in particolare le molecole MHC di classe II, erano strettamente legate alla persistenza del DNA di EBV. I geni attivi nelle cellule B—il principale serbatoio a lungo termine di EBV—e in altre cellule presentanti antigene risultavano particolarmente arricchiti. Utilizzando modelli informatici di come diverse varianti MHC umane legano porzioni del proteoma di EBV, gli autori hanno trovato che le versioni previste come migliori presentatrici di frammenti EBV tendevano a proteggere da livelli elevati di DNA di EBV, mentre le presentatrici più deboli si associavano alla persistenza.
Cosa significa per la comprensione delle infezioni
Per i non specialisti, il messaggio centrale è che il nostro equilibrio a lungo termine con EBV non è casuale. Minando i dati di sequenziamento su scala di popolazione già esistenti, lo studio mostra che il makeup genetico di una persona—soprattutto nei geni immunitari che mostrano frammenti virali alle cellule T—contribuisce a determinare quanto EBV persista nel sangue. Livelli elevati segnalano un sottoinsieme di persone a rischio aumentato per una gamma di malattie immunitarie, respiratorie e possibili malattie neurologiche. Il lavoro offre una guida per trasformare vecchi dati di sequenziamento in nuove intuizioni su molti virus che condividono il nostro corpo e suggerisce che strategie mirate per potenziare o imitare una presentazione antigenica efficace potrebbero un giorno aiutare a mantenere infezioni lifelong come EBV meglio sotto controllo.
Citazione: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Parole chiave: Virus di Epstein–Barr, persistenza virale, genetica umana, malattie autoimmuni, sequenziamento di biobanche