Clear Sky Science · it
Vaccini mRNA personalizzati evocano un’immunità T cellulare duratura nel TNBC adiuvante
Una nuova speranza dopo il trattamento del tumore al seno
Per molte donne con una forma aggressiva di tumore al seno chiamata carcinoma mammario triple‑negativo, la paura non finisce con la chemioterapia e l’intervento chirurgico. Questo tumore ha un alto rischio di recidiva e di diffusione, spesso già nei primi anni successivi. Lo studio descritto qui testa un vaccino altamente personalizzato, costruito sulle mutazioni del tumore di ciascuna paziente, per verificare se può addestrare il sistema immunitario a mantenere la sorveglianza per anni e ridurre la probabilità di ricaduta dopo il completamento della terapia standard.
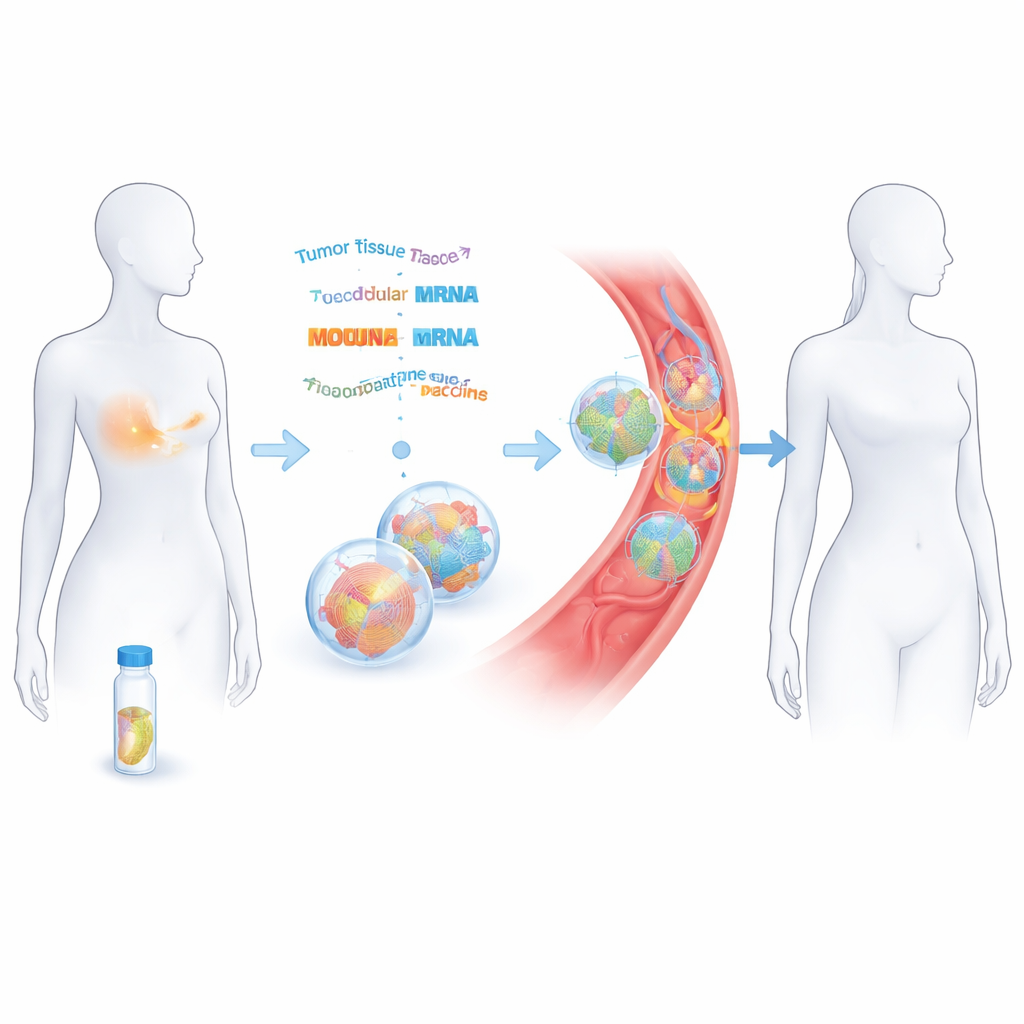
Trasformare un tumore rimosso in un vaccino su misura
I ricercatori hanno lavorato con 14 donne con carcinoma mammario triple‑negativo in stadio iniziale che avevano già ricevuto chirurgia e chemioterapia con intento curativo. Dal tessuto tumorale asportato hanno letto il DNA e l’RNA per catalogare le mutazioni uniche del cancro. Con strumenti informatici hanno previsto quali di questi cambiamenti potevano essere riconosciuti come estranei dalle cellule immunitarie. Fino a 20 di questi “neoantigeni” sono stati poi cuciti insieme e codificati in due filamenti di RNA messaggero (mRNA), simili nel principio ai vaccini contro il COVID‑19 ma adattati a ogni paziente. Questi filamenti di mRNA sono stati confezionati in piccole bolle lipidiche e somministrati per via endovenosa in otto dosi nell’arco di circa due mesi.
Come il vaccino risveglia i difensori immunitari
Una volta nel corpo, l’mRNA istruisce i sentinelli immunitari chiamati cellule dendritiche a produrre temporaneamente le proteine neoantigene e a esporne frammenti sulla loro superficie. Questo funziona come un manifesto “ricercato” per le cellule T, la forza principale del sistema immunitario nel distruggere il cancro. Il team ha prelevato sangue prima della vaccinazione e in diversi momenti successivi per testare se comparivano cellule T specifiche per i neoantigeni e quanto fossero potenti. Usando saggi di laboratorio sensibili, hanno trovato che ogni paziente sviluppò risposte T nuove o potenziate contro almeno una delle mutazioni selezionate, e la maggior parte rispose a diverse. In molti casi, ampie frazioni delle cellule T circolanti—livelli normalmente osservati solo con potenti terapie cellulari—erano ora orientate a riconoscere bersagli specifici del tumore.
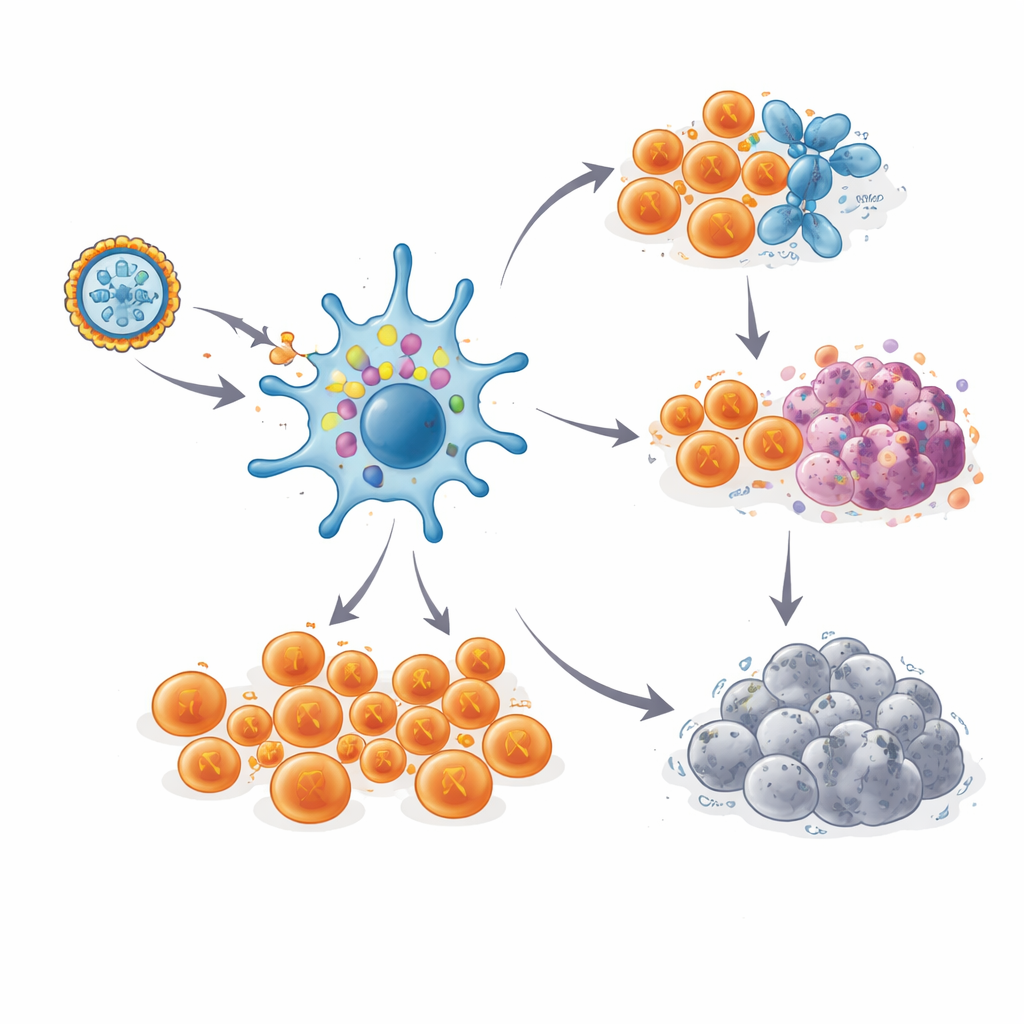
Memoria immunitaria di lunga durata
Importante, queste risposte delle cellule T non si sono affievolite rapidamente. Nella maggior parte delle pazienti le risposte più forti hanno raggiunto il picco durante il periodo di vaccinazione, sono calate leggermente e poi sono rimaste a livelli elevati per uno fino a tre anni e mezzo, anche senza richiami. Tracciando i “codici a barre” unici dei recettori di singoli cloni di cellule T, gli scienziati hanno potuto seguire specifiche cellule reattive ai neoantigeni per fino a sei anni in una paziente che è rimasta libera da cancro. Analisi dettagliate a singola cellula hanno mostrato due destini principali per queste cellule. Molte sono diventate cellule T citotossiche altamente armate, pronte a distruggere qualsiasi cellula che portasse il neoantigene giusto. Altre si sono sviluppate in un pool di memoria più raro, di tipo staminale, con marker di auto‑rinnovamento, suggerendo un serbatoio capace di rigenerare nuove ondate di combattenti se le cellule tumorali riapparissero.
Cosa è accaduto alle pazienti
Dopo un follow‑up mediano di poco più di cinque anni dalla prima dose di vaccino, undici delle quattordici donne non avevano avuto una recidiva; una di queste è deceduta per cause non correlate mentre era ancora in remissione. Tre donne hanno avuto una ricaduta, e i loro casi forniscono indizi sul perché un vaccino personalizzato a volte può fallire. Una paziente aveva montato solo una debole risposta T ed ha successivamente beneficiato di un diverso farmaco immunoterapico, un anticorpo anti‑PD‑1, prima di soccombere infine a una malattia disseminata. Una seconda paziente aveva un rischio ereditario e tumori in entrambe le mammelle; solo un tumore è stato usato per progettare il vaccino, e prove successive hanno mostrato che la recidiva proveniva dal tumore geneticamente distinto non vaccinato. La terza paziente aveva forti cellule T indotte dal vaccino che avevano infiltrato il tumore recidivante, ma le cellule tumorali avevano in gran parte perso molecole chiave necessarie per esporre i neoantigeni sulla loro superficie, nascondendosi così efficacemente dall’attacco immunitario.
Perché questo lavoro è importante per il futuro
Questo studio di fase iniziale era di piccole dimensioni e senza un gruppo di controllo, quindi non può dimostrare che il vaccino da solo abbia prevenuto le recidive. Ciononostante, dimostra che costruire un vaccino mRNA complesso e su misura dal tumore di una paziente è fattibile nelle routine ospedaliere, è generalmente ben tollerato e può innescare armate di cellule T potenti e durature contro molteplici bersagli specifici del cancro. I risultati evidenziano anche vie di fuga che i tumori possono usare, come la perdita del macchinario di presentazione degli antigeni o l’origine da lesioni non prese di mira, indicando la possibilità di combinazioni con altre terapie immunitarie e una caratterizzazione genomica tumorale più ampia. Per le pazienti affette da carcinoma mammario triple‑negativo, questo lavoro suggerisce che un vaccino su misura, somministrato dopo il trattamento standard, potrebbe un giorno aiutare a impedire il ritorno della malattia trasformando il loro sistema immunitario in una linea di difesa durevole e altamente specifica.
Citazione: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Parole chiave: carcinoma mammario triple‑negativo, vaccini mRNA per il cancro, immunoterapia con neoantigeni, immunità delle cellule T, recidiva tumorale