Clear Sky Science · it
L’invecchiamento favorisce l’accumulo microgliale di proteine sinaptiche a degradazione lenta
Perché la pulizia proteica del nostro cervello conta con l’avanzare dell’età
La maggior parte di noi spera di mantenere la mente lucida con l’età, eppure l’età è il principale fattore di rischio per l’Alzheimer e altre demenze. Questo studio pone una domanda apparentemente semplice: cosa succede alle attività quotidiane di “manutenzione” delle proteine all’interno delle cellule cerebrali con l’invecchiamento? Sviluppando nuovi strumenti molecolari nei topi per seguire nel tempo le proteine neuronali appena sintetizzate, i ricercatori tracciano come le proteine vengono rinnovate, come si aggregano e come le cellule immunitarie del cervello, le microglia, contribuiscono a rimuovere il disordine. I risultati mostrano un rallentamento generalizzato della pulizia proteica che si concentra sulle sinapsi — le giunzioni dove i neuroni comunicano — e che potrebbe aiutare a spiegare la perdita di memoria legata all’età.
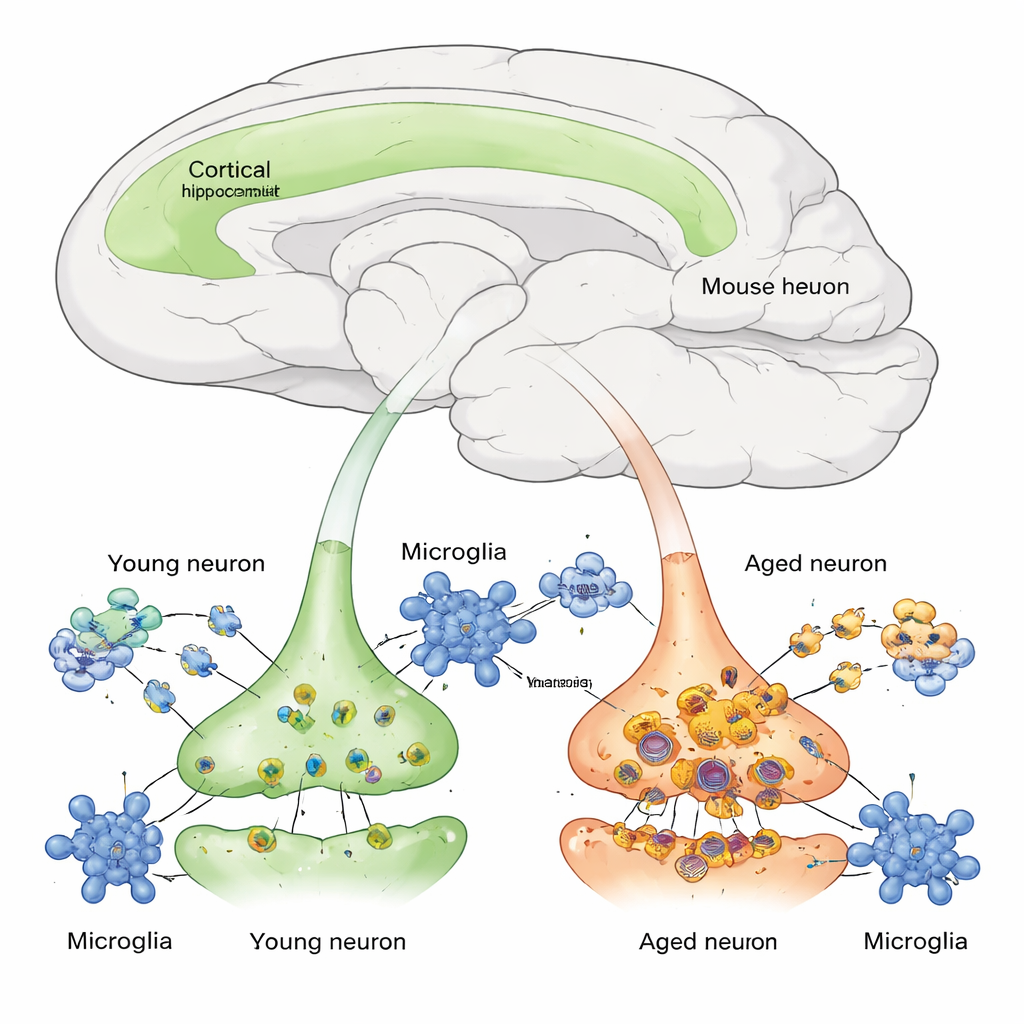
Seguire le nuove proteine nelle cellule cerebrali vive
Le proteine nelle nostre cellule vengono costantemente sintetizzate e degradate, un equilibrio noto come proteostasi. Finora è stato difficile misurare questo processo in tipi cellulari specifici all’interno di un cervello mammifero vivente. Gli autori hanno ingegnerizzato topi con un sistema genetico di “marcatura” chiamato BONCAT che induce solo certi neuroni — quelli che usano il promotore Camk2a, per lo più neuroni eccitatori corticali e ippocampali — a inserire un amminoacido speciale, cliccabile, nelle proteine appena fatte. Dopo aver somministrato questo amminoacido ai topi per un breve periodo, il gruppo è stato in grado di isolare e identificare tramite spettrometria di massa solo le proteine neuronali recentemente sintetizzate, e poi osservare come i loro livelli calassero nel tempo man mano che le proteine venivano degradate.
Come l’invecchiamento rallenta il turnover proteico
Utilizzando una versione virale dello strumento di marcatura, i ricercatori hanno etichettato i neuroni in topi giovani (4 mesi), di mezza età (12 mesi) e anziani (24 mesi). Hanno quindi seguito migliaia di proteine in diverse regioni cerebrali — corteccia sensoriale e visiva, ippocampo e ipotalamo — durante un periodo di “inseguimento” di due settimane dopo l’interruzione della marcatura. Modellando queste curve di decadimento, hanno stimato l’emivita di ciascuna proteina, ossia il tempo necessario perché ne venga rimossa metà. In media, le emivite delle proteine neuronali sono praticamente raddoppiate tra i topi giovani e quelli anziani, con la maggior parte del rallentamento che emerge dopo la mezza età. L’effetto variava per regione, e alcuni gruppi di proteine degradavano in modo strettamente coordinato, indicando che interi percorsi — come quelli che controllano la segnalazione sinaptica — condividono cinetiche simili e dipendenti dall’età.
Proteine che si aggregano e sinapsi vulnerabili
Un tasso di degradazione più lento aumenta il rischio che le proteine si malripieghino e si attacchino tra loro. Il gruppo ha isolato aggregati insolubili al detergente da cervelli di topi anziani e, utilizzando il loro marcatore neuronale, ha definito un “aggregoma” di 1.726 proteine neuronali che finiscono in questi ammassi. Quasi la metà delle proteine che mostravano una degradazione ridotta con l’età comparivano anche negli aggregati, e molte erano state collegate, da studi genetici precedenti, a disturbi dello sviluppo o neurodegenerativi. Le proteine sinaptiche si sono distinte: componenti delle macchine pre- e postsinaptiche, giunzioni cellulari ed elementi mitocondriali localizzati alle sinapsi risultavano fortemente arricchiti sia tra le proteine a degradazione lenta sia tra quelle che si aggregano. La microscopia ha confermato che proteine specifiche come RTN3 e SRSF3 formavano punti simili ad aggregati nell’ippocampo di topi anziani ma non in quelli giovani. Questo cedimento della proteostasi focalizzato sulle sinapsi si accorda con evidenze di lungo corso secondo cui la perdita sinaptica corre strettamente con il declino cognitivo.
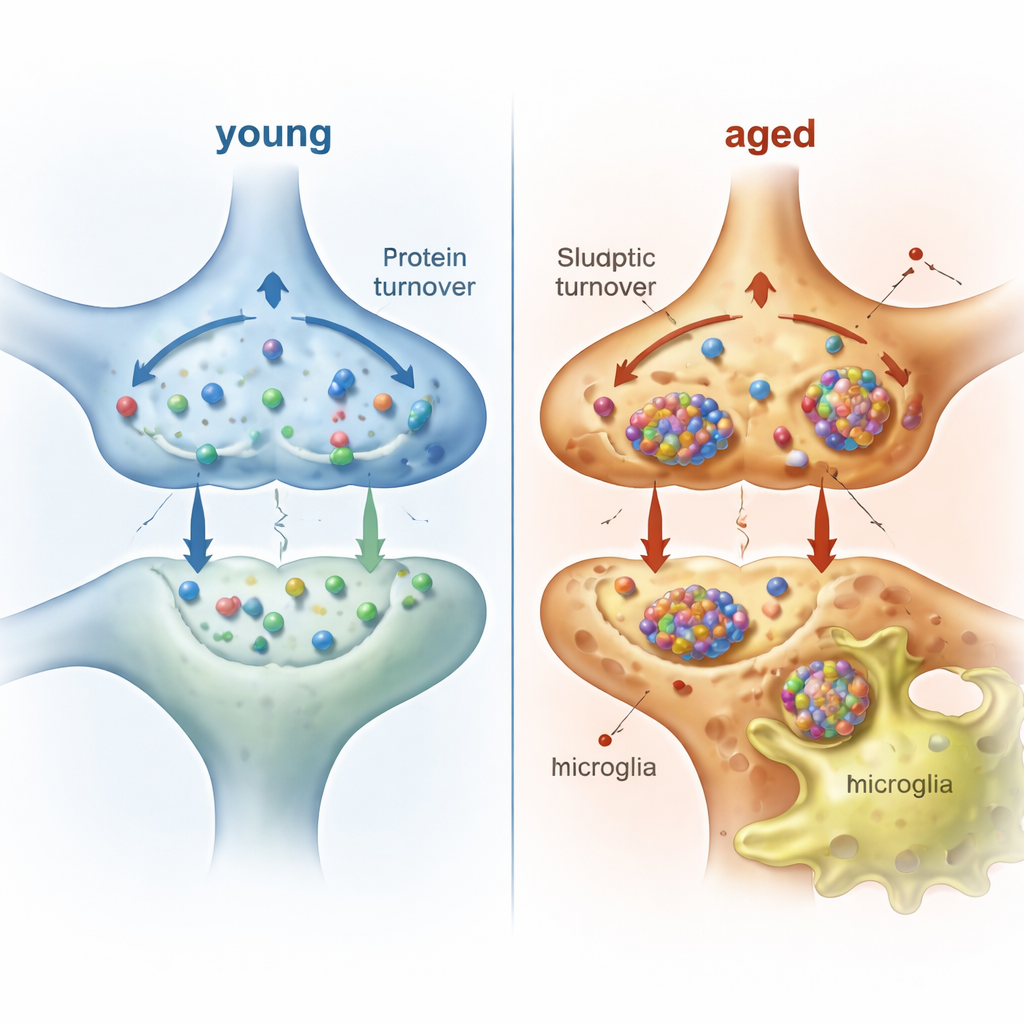
Le microglia come squadra di pulizia del cervello
I neuroni non affrontano questo carico da soli. Le microglia, le cellule immunitarie residenti del cervello, sorvegliano costantemente e potato le sinapsi. Per vedere quale materiale di origine neuronale le microglia effettivamente ingeriscono in animali vivi, gli autori hanno marcato le proteine neuronali per una settimana in topi giovani e anziani, poi hanno purificato centinaia di migliaia di microglia e isolato le proteine marcate presenti al loro interno. Hanno rilevato centinaia di proteine neuronali all’interno delle microglia, con forte rappresentanza di componenti sinaptici, di membrana e mitocondriali. Molte di queste proteine portano segnali di secrezione o sono note cargo di esosomi, suggerendo la secrezione come una via di trasferimento, mentre altre risultano coerenti con l’ingestione microgliale di elementi sinaptici. Nei topi anziani, le microglia contenevano più tipi e quantità maggiori di proteine derivate dai neuroni rispetto ai topi giovani, pur mantenendo un bilancio simile tra componenti pre- e postsinaptiche.
Quando la pulizia fallisce, il cervello paga il prezzo
Sovrapponendo tre set di dati — le proteine la cui degradazione rallenta con l’età, le proteine trovate negli aggregati neuronali e le proteine che si accumulano nelle microglia di cervelli anziani — lo studio ha identificato 166 proteine che si trovano all’intersezione di questi processi. Più della metà di tutte le proteine di origine neuronale arricchite nelle microglia anziane mostrava qualche tipo di problema di proteostasi legato all’età. Molte sono codificate da geni precedentemente segnalati come fattori di rischio per Alzheimer, Parkinson e altri disturbi cerebrali. Nel complesso, questi risultati delineano una cascata: con l’età, il turnover delle proteine neuronali rallenta, specialmente alle sinapsi; le proteine vulnerabili hanno più probabilità di malripiegarsi e aggregarsi; e le microglia rimuovono sempre più questi componenti danneggiati, probabilmente inglobando sinapsi sotto stress. Nel breve termine questo può proteggere i neuroni, ma nel corso di decenni potrebbe contribuire alla perdita di sinapsi e al deterioramento cognitivo. Comprendere e, in ultima analisi, ripristinare una proteostasi neuronale sana potrebbe quindi essere una strategia chiave per mantenere la resilienza cerebrale nella tarda età.
Citazione: Guldner, I.H., Wagner, V.P., Moran-Losada, P. et al. Ageing promotes microglial accumulation of slow-degrading synaptic proteins. Nature 650, 930–941 (2026). https://doi.org/10.1038/s41586-025-09987-9
Parole chiave: invecchiamento cerebrale, turnover proteico, sinapsi, microglia, neurodegenerazione