Clear Sky Science · it
Lo scudo metabolico dipendente dai poliamini regola lo splicing alternativo
Come piccole molecole aiutano le cellule a leggere i loro geni
All'interno di ogni cellula, lo stesso copione del DNA può essere letto in modi diversi, permettendo a un numero limitato di geni di produrre un'enorme varietà di proteine. Questa flessibilità dipende da un processo chiamato splicing alternativo, che modifica i messaggi dell'RNA prima che vengano tradotti in proteine. Questo articolo rivela che piccole molecole cariche positivamente, chiamate poliamine, guidano silenziosamente questa fase di editing, agendo come una sorta di scudo protettivo che aiuta la cellula a decidere quali versioni di RNA produrre. Poiché lo splicing alternativo è cruciale nel cancro, nelle funzioni cerebrali e nelle cellule staminali, scoprire questo livello nascosto di controllo ha implicazioni ampie per salute e malattia.
Piccoli aiutanti carichi in ogni cellula
Le poliamine sono molecole piccole e flessibili che portano più cariche positive. Le cellule le sintetizzano a partire da nutrienti di base, e da tempo sono conosciute come facilitatori della crescita e della sopravvivenza, specialmente in cellule che si dividono rapidamente come i tumori. Gli autori hanno indagato se le poliamine fungano anche da segnali, non solo da carburante. Bloccando parzialmente la produzione di poliamine in cellule di cancro alla prostata e in topi, hanno misurato come proteine e RNA cambiassero nel tempo. Hanno osservato che molto prima che i livelli totali di poliamine diminuissero drasticamente, si verificava un'ondata marcata di cambiamenti nella fosforilazione delle proteine—etichette chimiche che accendono o spengono interruttori proteici—soprattutto su componenti della macchina di editing dell'RNA, lo spliceosoma.
Riprogrammare l'editor dell'RNA della cellula
Analizzando specificamente l'RNA, il gruppo ha utilizzato sequenziamento profondo per tracciare lo splicing alternativo quando la sintesi delle poliamine era inibita. Centinaia di segmenti di RNA venivano saltati o inclusi in modo diverso, in linee cellulari tumorali, in tipi cellulari normali e in tessuti murini. Questi cambiamenti non erano semplicemente un effetto collaterale della diminuzione della divisione cellulare o di un altro noto processo dipendente dalle poliamine chiamato ipusinazione. Al contrario, quando i ricercatori reinsersero poliamine esogene nelle cellule, molti spostamenti nello splicing tornarono verso la normalità. Sia i farmaci sia gli strumenti genetici che abbassavano le poliamine produssero pattern di splicing simili, e un'ulteriore riduzione delle poliamine con una combinazione farmacologica rafforzò ulteriormente i cambiamenti, confermando che l'effetto era strettamente legato alla disponibilità di poliamine.
Un bersaglio nascosto: il modulo SF3 dello splicing
Per identificare dove nello spliceosoma agissero le poliamine, gli autori confrontarono la firma di splicing indotta dalla loro riduzione con una grande mappa di riferimento generata silenziando individualmente oltre 300 fattori noti dello splicing. La corrispondenza più stretta indicò una parte specifica dello spliceosoma chiamata sottocomplesso SF3, che aiuta a riconoscere segnali chiave nell'RNA. L'analisi computazionale di dati pubblici su legame proteina–RNA supportò questo legame: gli RNA il cui splicing era alterato dalla perdita di poliamine erano particolarmente propensi a essere legati da proteine SF3. Quando il team disabilitò parzialmente componenti di SF3, geneticamente o con un farmaco, gli effetti sullo splicing dovuti alla deplezione di poliamine vennero in gran parte annullati, dimostrando che un'attività SF3 intatta è richiesta per questo nuovo percorso regolatorio. 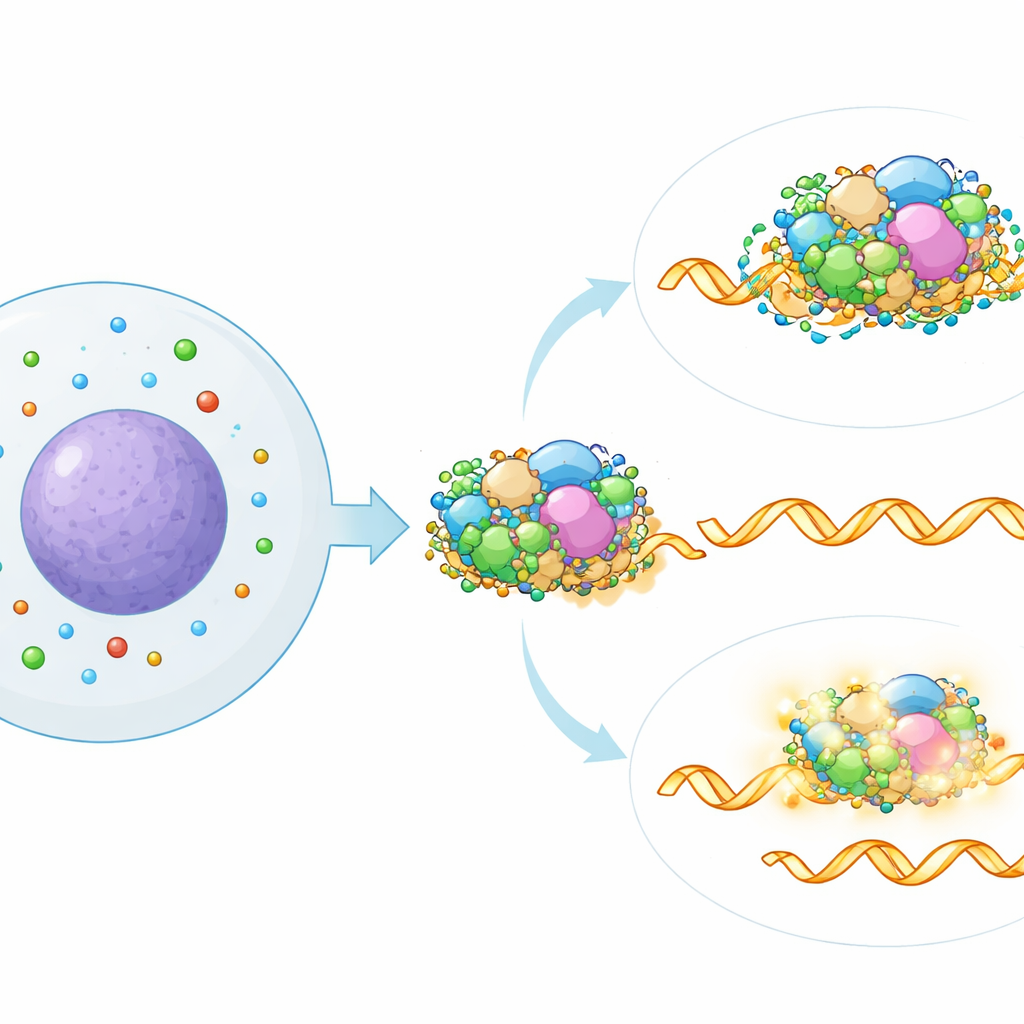
Scudo metabolico: come le poliamine bloccano l'etichettatura delle proteine
Approfondendo, i ricercatori notarono che i siti di fosforilazione più fortemente colpiti sulle proteine SF3 si raggruppavano in brevi tratti ricchi di aminoacidi con carica negativa. Modellizzazione molecolare ed esperimenti di risonanza magnetica nucleare mostrarono che le poliamine si annidano in queste zone acide, formando molteplici contatti elettrostatici e coprendo parzialmente residui di serina vicini, dove normalmente vengono aggiunti gruppi fosfato. Questo «abbraccio» fisico riduce l'accessibilità di questi punti alle chinasi proteiche—gli enzimi che attaccano i fosfati. In esperimenti in vitro, l'aggiunta di poliamine bloccò direttamente una chinasi chiamata CK1 dall fosforilare le proteine SF3. Nelle cellule, l'inibizione di CK1 e della sua stretta correlata CK2 attenuò i cambiamenti di splicing causati dalla perdita di poliamine, e topi ingegnerizzati il cui SF3A3 mancava di tre siti chiave di fosforilazione divennero in gran parte insensibili agli spostamenti di splicing dipendenti dalle poliamine. 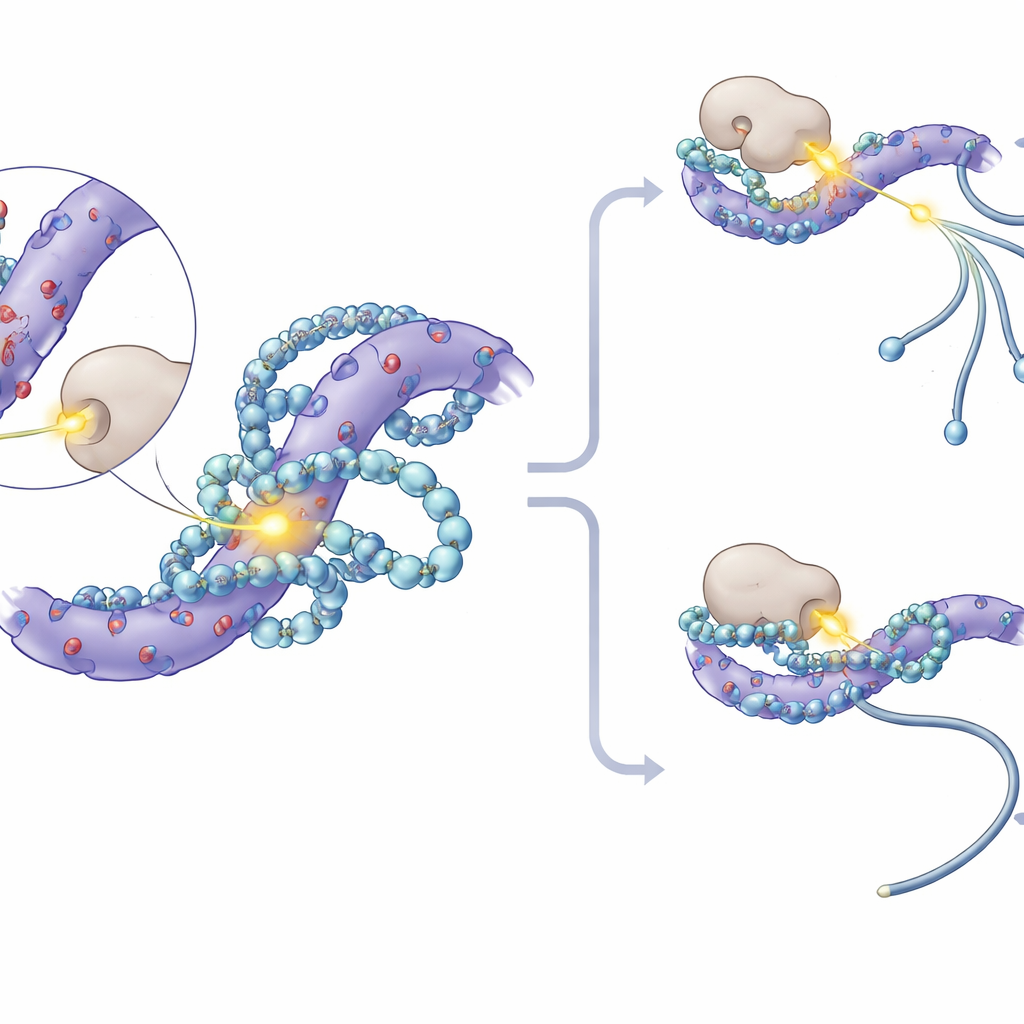
Una molecola di sintesi che separa i ruoli
Lo studio introduce anche un farmaco simile alle poliamine, BENSpm, che è più fortemente carico positivamente ma contemporaneamente sopprime la produzione cellulare di poliamine. BENSpm si legò saldamente alle patch acide di SF3 e bloccò l'azione delle chinasi, proprio come le poliamine naturali, eppure non riuscì a ripristinare la crescita cellulare quando le poliamine reali scarseggiavano. Questo permise agli autori di separare le funzioni classiche delle poliamine (sostenere crescita e metabolismo) dal ruolo di scudo recentemente definito. Nelle cellule staminali embrionali murine, la deplezione di poliamine spingeva le cellule a perdere il marcatore di «stemness» Nanog e alterava il loro panorama di splicing. BENSpm ripristinò sia il profilo di splicing sia l'espressione di Nanog nonostante la continua soppressione della sintesi normale di poliamine, indicando che lo scudo metabolico è un requisito chiave per mantenere l'identità delle cellule staminali.
Perché questa scoperta è importante
In termini pratici, questo lavoro mostra che le poliamine fungono da piccoli guanti protettivi attorno a parti sensibili di proteine chiave dello splicing. Quando i guanti sono indossati, le chinasi non possono facilmente afferrare e marcare quei siti, e l'editing dell'RNA della cellula rimane sul giusto binario. Quando le poliamine sono basse, i guanti vengono tolti, la fosforilazione aumenta e i pattern di splicing cambiano, con conseguenze per le cellule tumorali e le cellule staminali. Definendo questo meccanismo di «scudo metabolico» e fornendo una molecola strumentale che lo imita selettivamente, lo studio apre la strada a nuovi modi di modulare la lettura dei geni senza cambiare il DNA stesso, potenzialmente ispirando future terapie mirate allo splicing nel cancro e nella medicina rigenerativa.
Citazione: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Parole chiave: poliamine, splicing alternativo, processamento dell'RNA, segnalazione metabolica, regolazione delle cellule staminali