Clear Sky Science · it
Traiettorie di attivazione specifiche per ligando determinano il segnalamento dei GPCR nelle cellule
Come un solo recettore può comportarsi come molti interruttori
Molti dei farmaci odierni agiscono su una vasta famiglia di proteine di superficie cellulare chiamate recettori accoppiati a proteine G, o GPCR. Questi recettori influenzano il battito cardiaco, l’umore, la respirazione e innumerevoli altre funzioni dell’organismo. Per decenni sono stati considerati semplici interruttori on–off: un farmaco si lega, l’interruttore si attiva e un segnale passa all’interno della cellula. Questo lavoro mostra che la realtà è molto più ricca. Usando un nuovo tipo di “informatore” fluorescente integrato direttamente in un recettore, gli autori osservano, in cellule vive, come diversi farmaci guidino lo stesso recettore lungo percorsi di attivazione distinti—come scegliere rotte diverse attraverso una città—per produrre schemi di segnalazione differenti. Comprendere queste rotte nascoste potrebbe aiutare a progettare farmaci che diano il beneficio desiderato evitando gli effetti collaterali.
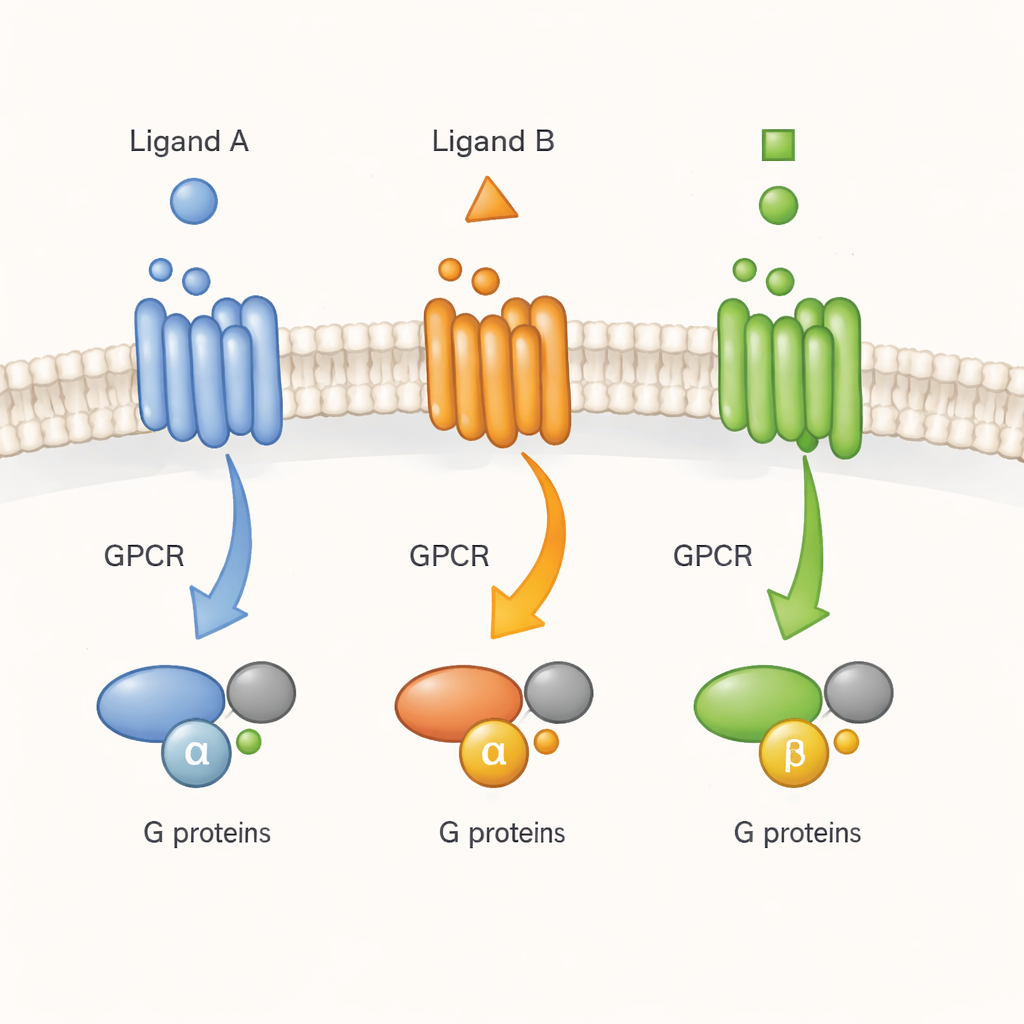
Osservare il campanello della cellula in tempo reale
I GPCR sono spesso descritti come campanelli molecolari: una molecola segnale (un ligando) suona dall’esterno e il recettore trasmette il messaggio alle proteine G dall’interno. Lavori precedenti su recettori purificati in detergenti avevano suggerito che i GPCR non si limitano a passare da una forma inattiva a una forma attiva. Piuttosto, esplorano molte conformazioni che i farmaci possono stabilizzare in gradi diversi. Ma non era chiaro se la stessa complessità esistesse nell’ambiente affollato e dinamico di una cellula viva. Qui, gli autori si concentrano su un recettore rappresentativo, il recettore muscarinico M2 per l’acetilcolina, un importante regolatore dell’attività cardiaca e nervosa, e si chiedono se diversi ligandi lo inducano in forme attive distinte che siano rilevanti per il segnalamento cellulare reale.
Costruire minuscoli rivelatori di luce sulla superficie del recettore
Per seguire i movimenti del recettore senza disturbare la sua funzione normale, il gruppo ha usato l’espansione del codice genetico, una tecnologia che consente di inserire un amminoacido progettato in posizioni selezionate sulla superficie esterna del recettore. Questo “ancoraggio” chimico può essere cliccato a una piccola molecola fluorescente nelle cellule vive. Scansionando 72 posizioni e mantenendo solo quelle che continuavano a comportarsi come recettori normali, hanno costruito un pannello di sette varianti del recettore M2, ciascuna portatrice di un singolo colorante in un diverso sito del loop esterno. Quando è stato applicato il messaggero naturale acetilcolina, la luminosità del colorante in questi siti aumentava o diminuiva in modi caratteristici, rivelando come ogni parte della superficie esterna del recettore si spostasse all’inizio della segnalazione. Fondamentalmente, questi recettori marcati potevano ancora attivare le proteine G e subire l’endocitosi normale, mostrando che i rivelatori erano fedeli rispetto al loro comportamento piuttosto che dirompenti.
I farmaci lasciano “impronte conformazionali” distinte
I ricercatori hanno quindi confrontato diversi farmaci che attivano tutti il recettore M2 ma con diverse intensità: l’acetilcolina endogena, un agonista sintetico molto potente chiamato iperoxo e due agonisti parziali più deboli, arecolina e pilocarpina. Ogni farmaco ha prodotto un modello unico di cambiamenti di fluorescenza attraverso i sette siti reporter—un’impronta conformazionale. Nella maggior parte delle posizioni, l’ampiezza del movimento seguiva quanto fortemente il farmaco attivava il recettore. In due siti, tuttavia, la relazione era invertita: i farmaci più deboli provocarono i maggiori cambiamenti, mentre il farmaco più potente ne provocò quasi nessuno. Un comportamento del genere non può essere spiegato da un singolo stato attivo. Indica invece che lo stesso recettore, nelle cellule vive, può adottare diverse forme attive distinte, alcune favorite da farmaci forti, altre da farmaci deboli.
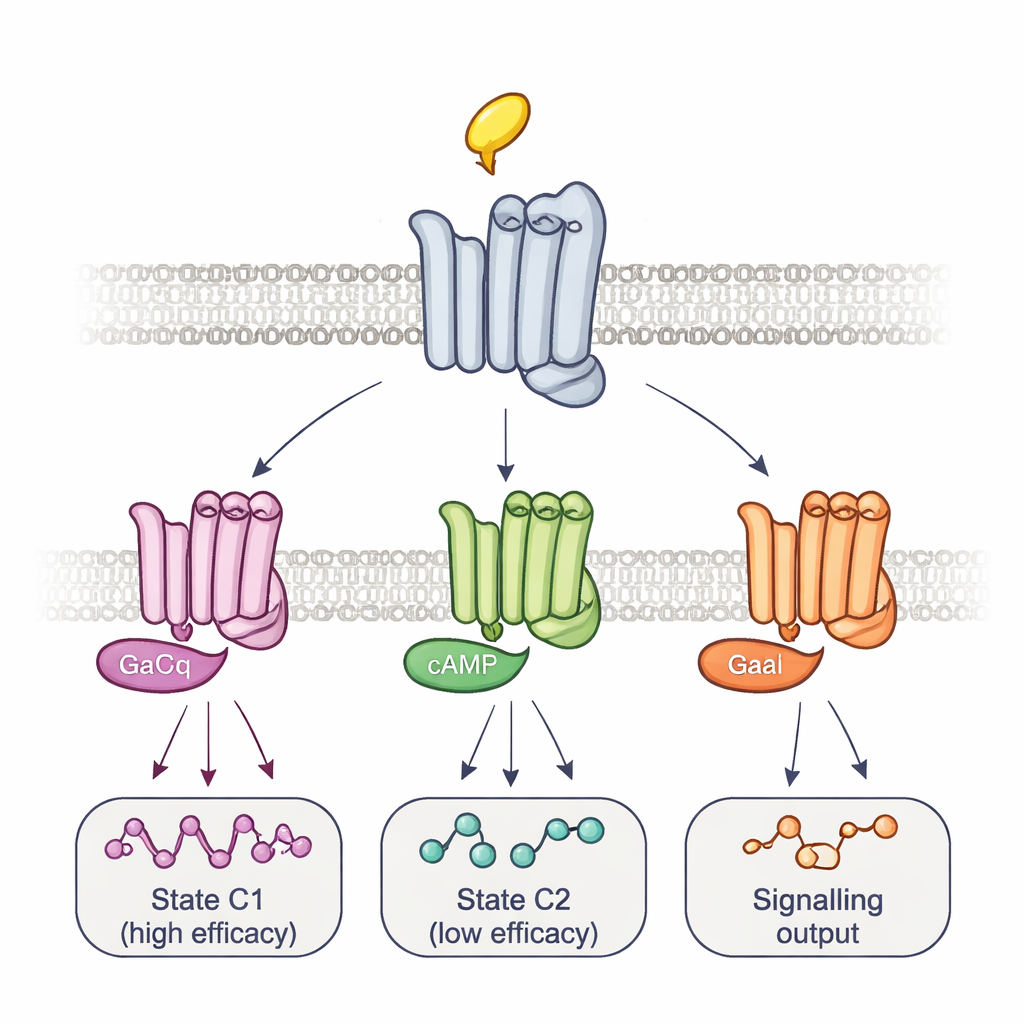
Molteplici complessi e rotte temporizzate verso la segnalazione
Per collegare queste forme al segnalamento effettivo, il gruppo ha modificato le stesse proteine G. Sovraesprimendo una proteina G mutante che forma complessi molto stretti e di lunga durata con i recettori, hanno cancellato selettivamente il segnale da alcuni siti reporter mentre ne hanno potenziato altri. Questo schema, insieme alla tempistica dei cambiamenti di fluorescenza, ha rivelato almeno due principali complessi recettore–proteina G: un complesso ad alta efficacia che si forma rapidamente e uno a bassa efficacia più lento. Diversi farmaci spostavano l’equilibrio tra questi complessi e persino utilizzavano passaggi intermedi diversi per arrivarci, tracciando traiettorie di attivazione specifiche per farmaco. Usando un saggio separato di bioluminescenza che monitora un pannello di 14 sottotipi di proteine G, gli autori hanno mostrato che questi equilibri contribuiscono a determinare non solo quanto intensamente un farmaco attivi il segnalamento complessivo, ma anche quali esatte proteine G vengono attivate. Per esempio, l’arecolina attivava preferenzialmente certi Go, mentre la pilocarpina favoriva nettamente il complesso a bassa efficacia.
Perché questo è importante per farmaci migliori
Per i non specialisti, il messaggio chiave è che un singolo recettore non è semplicemente un unico interruttore ma un insieme di interruttori correlati, ciascuno raggiungibile attraverso percorsi diversi e ciascuno connesso a effetti downstream leggermente diversi. Questo studio fornisce una vista diretta di quei percorsi e stati in cellule intatte, anziché in sistemi semplificati in provetta. Mappando come particolari farmaci indirizzano il recettore verso complessi e partner di proteine G specifici, i ricercatori ottengono un progetto per ideare medicine “più intelligenti”—composti che spingono i recettori in stati che promuovono segnali utili evitando quelli associati a effetti collaterali. La strategia del biosensore fluorescente sviluppata qui dovrebbe essere adattabile a molti altri recettori, aprendo una finestra sulla coreografia in tempo reale dell’azione dei farmaci nelle cellule vive.
Citazione: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Parole chiave: segnalamento dei GPCR, efficacia del ligando, proteine G, biosensori conformazionali, scoperta di farmaci