Clear Sky Science · it
La plasticità delle cellule T indotta dalla microbiota consente il controllo tumorale mediato dal sistema immunitario
Come i batteri intestinali amici potrebbero aiutare a combattere il cancro
L’immunoterapia oncologica ha trasformato il trattamento per molti pazienti, eppure solo una parte vede i propri tumori ridursi e restare assenti. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: possono specifici batteri intestinali “istruire” le cellule immunitarie in modi che rendano più efficaci i farmaci che bloccano i checkpoint, come la terapia anti–PD‑1? Seguendo il percorso delle cellule immunitarie dall’intestino tenue ai tumori nei topi, gli autori mettono in luce un collegamento diretto e verificabile tra un singolo microbo intestinale e il successo nel controllo tumorale.
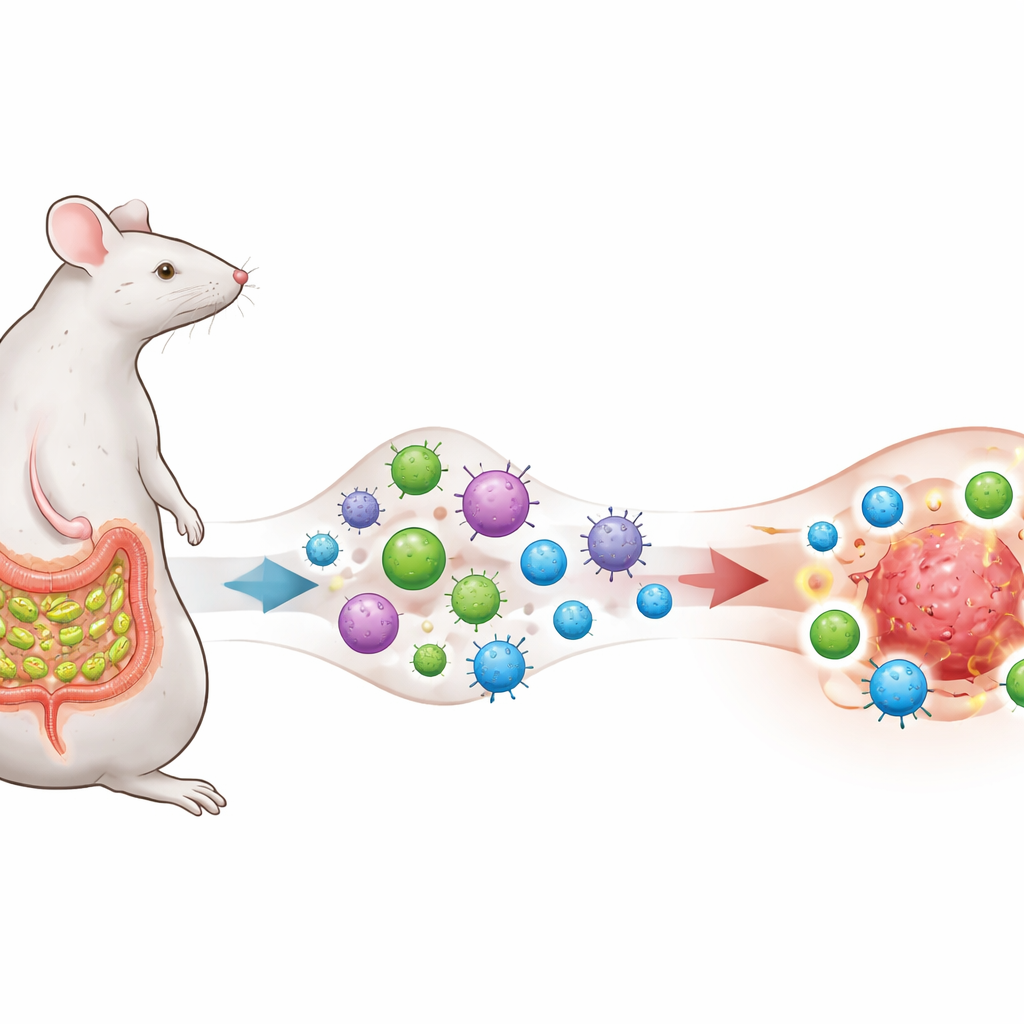
Un microbo che addestra il sistema immunitario
I ricercatori si concentrano su un batterio intestinale chiamato batteri filamentosi segmentati (SFB), noto per vivere vicino alla mucosa dell’intestino tenue nei topi e per indurre una forte, ma normalmente omeostatica, risposta delle cellule T helper 17 (TH17). Hanno ingegnerizzato cellule di melanoma, polmone e colon in modo che esprimano un frammento proteico presente anche negli SFB, creando un’intenzionale “sovrapposizione di antigeni” tra il microbo e i tumori. I topi rimangono privi di SFB o vengono colonizzati da esso, e tutti ricevono la terapia anti–PD‑1, un anticorpo ampiamente usato che mira a rimuovere i freni sulle cellule T.
Cellule addestrate dall’intestino trasformano i tumori da freddi a caldi
Il trattamento con anti–PD‑1 da solo, o la sola presenza di SFB, fa poco per rallentare la crescita tumorale. Ma quando i tumori espongono l’antigene derivato da SFB e i topi sono colonizzati da SFB, l’anti–PD‑1 diventa improvvisamente molto efficace: i tumori si riducono, la sopravvivenza migliora e gli animali sopravvissuti respingono una successiva re‑sfida tumorale senza terapia aggiuntiva, indicando una memoria immunitaria duratura. In questi topi di successo, i tumori si riempiono di aggressive cellule T CD8 “killer” che producono interferone‑γ e altre molecole tossiche, mentre le cellule T regolatorie soppressive costituiscono una quota minore della popolazione immunitaria. In breve, l’ambiente locale attorno al cancro viene rimodellato da relativamente “freddo” e non reattivo a “caldo” e infiammato.
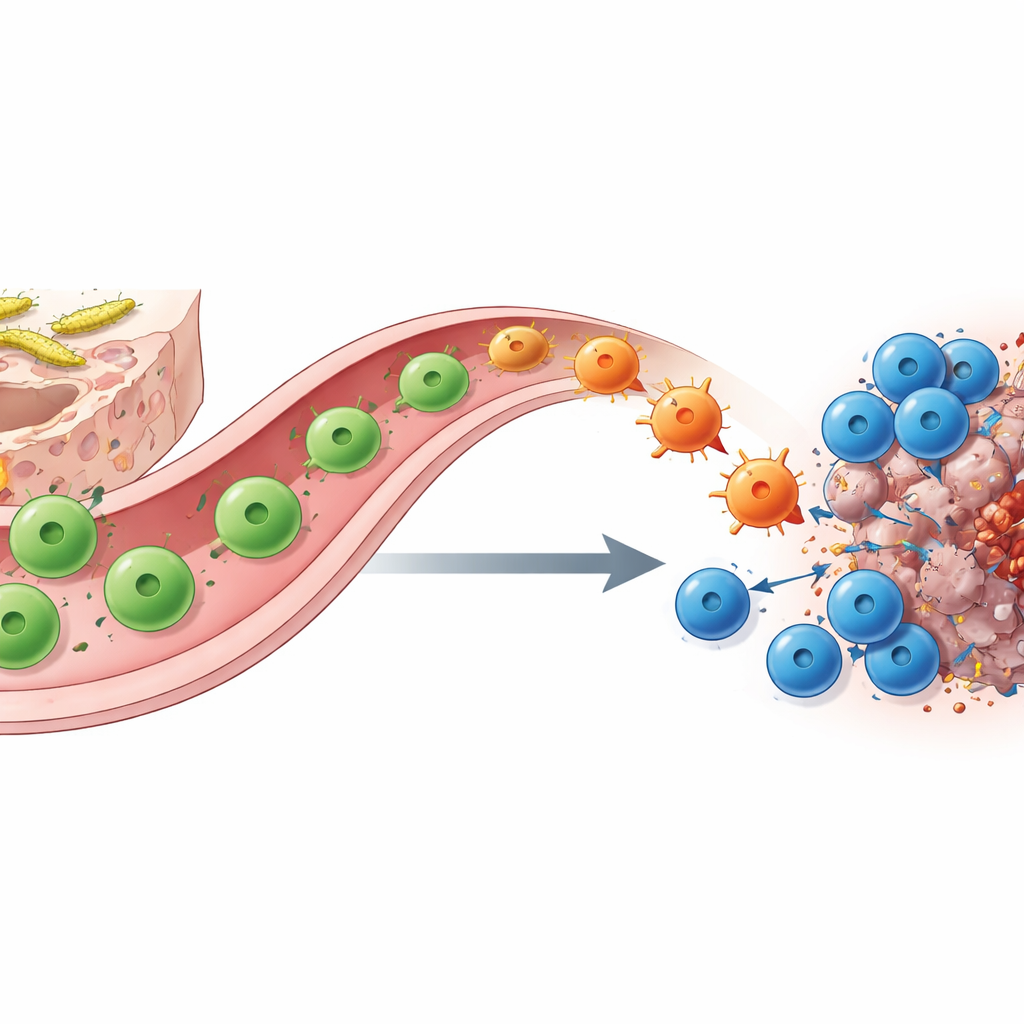
Le cellule T helper plastiche collegano intestino e tumore
Come provoca questo cambiamento la colonizzazione da SFB? Utilizzando marcatura molecolare, sequenziamento a singola cellula e tracciamento genetico intelligente, gli autori mostrano che i protagonisti chiave sono le cellule T helper CD4 specifiche per SFB. Nell’intestino tenue queste cellule iniziano come cellule TH17 che supportano la funzione di barriera e normalmente producono la molecola IL‑17A. Quando incontrano un antigene corrispondente in un tumore sotto il blocco dei checkpoint, migrano dall’intestino al sito tumorale e si “rielaborano” in cellule di tipo TH1 che invece secernono grandi quantità di interferone‑γ e TNF. Queste cellule convertite, le “ex‑TH17”, potenziano la presentazione dell’antigene e secernono chemoattrattanti, richiamando e attivando le cellule T CD8 killer. L’eliminazione sia delle cellule helper sia di quelle killer, o la cancellazione genetica delle cellule della linea IL‑17A che fungono da precursori, annulla in larga misura il beneficio dell’anti–PD‑1, sottolineando la loro collaborazione.
Non tutti i microbi forniscono istruzioni utili
Per verificare se qualsiasi batterio intestinale con antigeni sovrapponibili potesse funzionare, il gruppo ripete l’esperimento con un altro commensale, Helicobacter hepaticus. Questo organismo induce anch’esso forti risposte delle cellule T ma espande prevalentemente cellule di tipo regolatorio che attenuano l’infiammazione. Quando i tumori sono ingegnerizzati per esporre un antigene di H. hepaticus e i topi sono colonizzati da questo batterio, la terapia anti–PD‑1 non migliora i risultati. Sebbene molte cellule T helper specifiche per H. hepaticus migrino al tumore, mantengono un carattere regolatorio e producono poco interferone‑γ, non riuscendo a energizzare le cellule killer. Questo contrasto mostra che la qualità e la plasticità dei programmi delle cellule T indotti dal microbo — non solo la corrispondenza antigenica — determinano se la microbiota aiuterà o ostacolerà l’immunoterapia contro il cancro.
Cosa potrebbe significare per la cura del cancro in futuro
Complessivamente, il lavoro fornisce una prova diretta negli animali che un batterio intestinale definito può pre‑allenare le cellule T helper nell’intestino, inviarle a tumori che condividono l’antigene e, sotto il blocco dei checkpoint, indurle a cambiare ruolo diventando potenti cellule antitumorali. Chiarendo questo circuito intestino‑tumore, lo studio suggerisce che microbi scelti o ingegnerizzati con cura potrebbero un giorno essere usati insieme all’immunoterapia per convertire i tumori di più pazienti in bersagli trattabili e infiammati — a condizione che questi microbi inducano il giusto tipo di risposta delle cellule T flessibile e pro‑infiammatoria piuttosto che una risposta calmante e regolatoria.
Citazione: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
Parole chiave: microbiota intestinale, immunoterapia oncologica, plasticità delle cellule T, blocco dei checkpoint, microambiente tumorale