Clear Sky Science · it
Schermi CRISPR bidirezionali decodificano un circuito fibrotico dipendente da GLIS3
Quando la guarigione si trasforma in cicatrizzazione dannosa
I nostri intestini sono progettati per ripararsi dopo ogni graffio e irritazione. Ma in malattie croniche come il morbo di Crohn e la colite ulcerosa, questo processo di riparazione può deragliare, portando alla formazione di tessuto cicatriziale spesso e rigido che restringe l’intestino e può richiedere un intervento chirurgico. Questo studio scopre una conversazione nascosta tra cellule immunitarie e cellule strutturali dell’intestino che guida questa cicatrizzazione, e individua un interruttore maestro, un gene chiamato GLIS3, che potrebbe offrire un nuovo modo per interrompere il ciclo.
Una rete nascosta all’interno di intestini infiammati
Per capire perché alcuni pazienti sviluppano infiammazione e fibrosi ostinate, i ricercatori hanno creato un “atlante” cellulare dell’intestino umano. Hanno combinato il sequenziamento dell’RNA a singola cellula, che legge i geni attivi in singole cellule, con il profilo spaziale che mappa la posizione di quelle cellule in sezioni tissutali reali. Utilizzando campioni di persone con morbo di Crohn, colite ulcerosa e controlli, hanno mappato oltre quattro milioni di cellule attraverso la parete intestinale. Tra questa folla, un sottogruppo di fibroblasti si è distinto: i fibroblasti associati all’infiammazione, o IAF. Queste cellule si concentravano in aree di colite attiva e cronica e presentavano una firma genica legata alla resistenza alle terapie anti–TNF standard, suggerendo che svolgono un ruolo centrale nelle forme di malattia difficili da trattare. 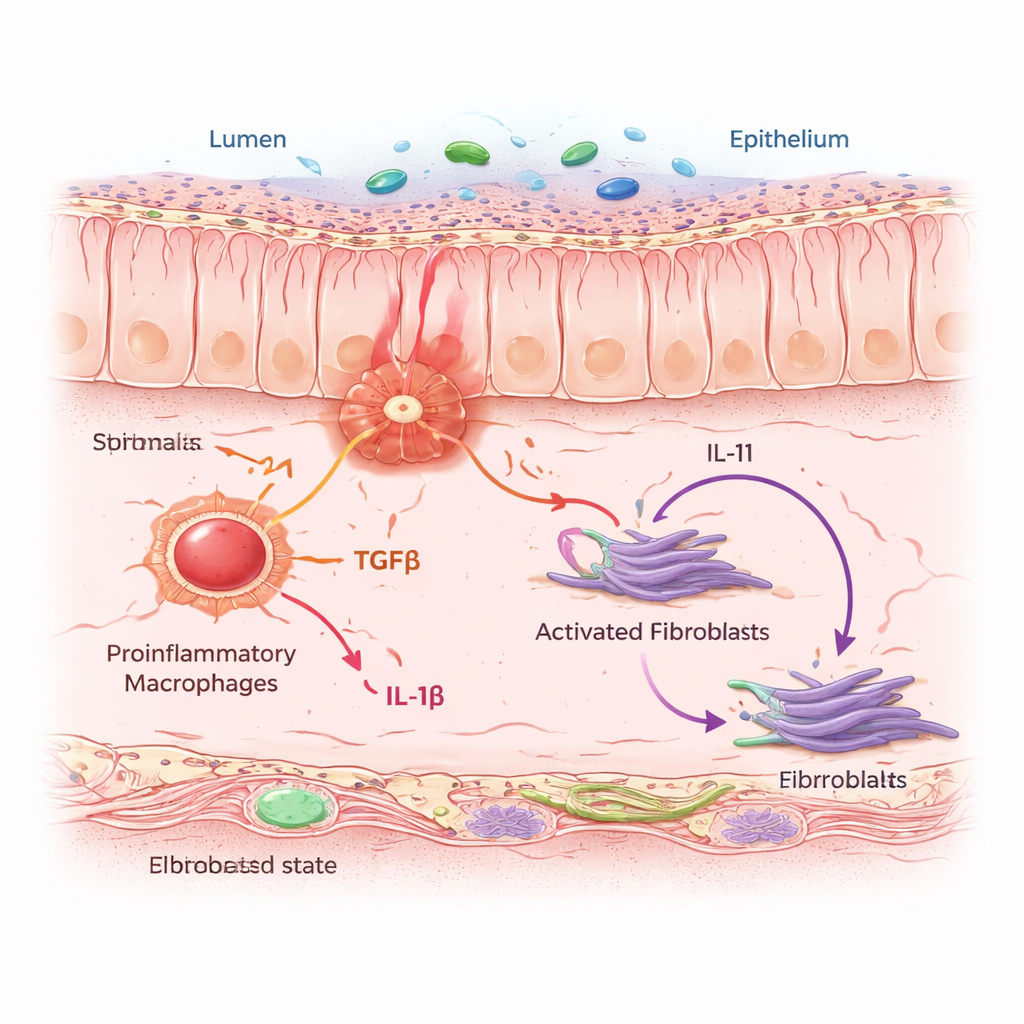
I macrofagi sussurrano, i fibroblasti cicatriziano
Gli IAF non agivano da soli. Si raggruppavano in “quartieri” densi di macrofagi proinfiammatori—cellule immunitarie che percepiscono il pericolo e rilasciano segnali d’allarme. Utilizzando modelli computazionali ed esperimenti di co-coltura cellulare, il gruppo ha mostrato che quando i macrofagi vengono spinti in uno stato infiammatorio secernono due proteine messaggere chiave: TGFβ e IL-1β. I fibroblasti vicini ascoltano questi segnali tramite recettori specifici. Quando arrivano insieme entrambi i segnali, i fibroblasti si trasformano nello stato IAF e iniziano a produrre IL-11, una citochina già sospettata di promuovere la fibrosi, insieme a collagene e altre proteine della matrice che ispessiscono e irrigidiscono la parete intestinale. In topi esposti a un protocollo di colite cronica, bloccare l’IL-11 o eliminarla selettivamente nei fibroblasti ha ridotto l’accumulo di collagene senza prevenire l’infiammazione iniziale, mostrando che l’IL-11 è un motore cruciale della fase di cicatrizzazione.
GLIS3: l’interruttore maestro nei fibroblasti fibrotici
Per passare dalle correlazioni ai meccanismi, gli autori hanno utilizzato potenti strumenti CRISPR genome-wide. Hanno ingegnerizzato fibroblasti umani in modo che la produzione di IL-11 potesse essere monitorata con un marcatore fluorescente, quindi hanno eseguito screening paralleli che o eliminavano geni o ne aumentavano l’espressione su tutto il genoma. Ordinando le cellule che producevano quantità insolitamente alte o basse di IL-11 dopo la stimolazione con TGFβ e IL-1β, hanno identificato geni che controllano questa risposta. Tra molti componenti di segnalazione, è emerso un fattore di trascrizione—GLIS3—come regolatore di primo piano. Quando GLIS3 è stato disattivato, i fibroblasti producevano molte meno IL-11; quando è stato potenziato, l’IL-11 è aumentata. Esperimenti aggiuntivi hanno mostrato che GLIS3 si sposta nel nucleo del fibroblasto in risposta ai segnali dei macrofagi, si lega direttamente al DNA vicino al gene IL11 e ad altri, e attiva un ampio programma di geni infiammatori e fibrotici, inclusi collageni e fattori che attirano altre cellule immunitarie. 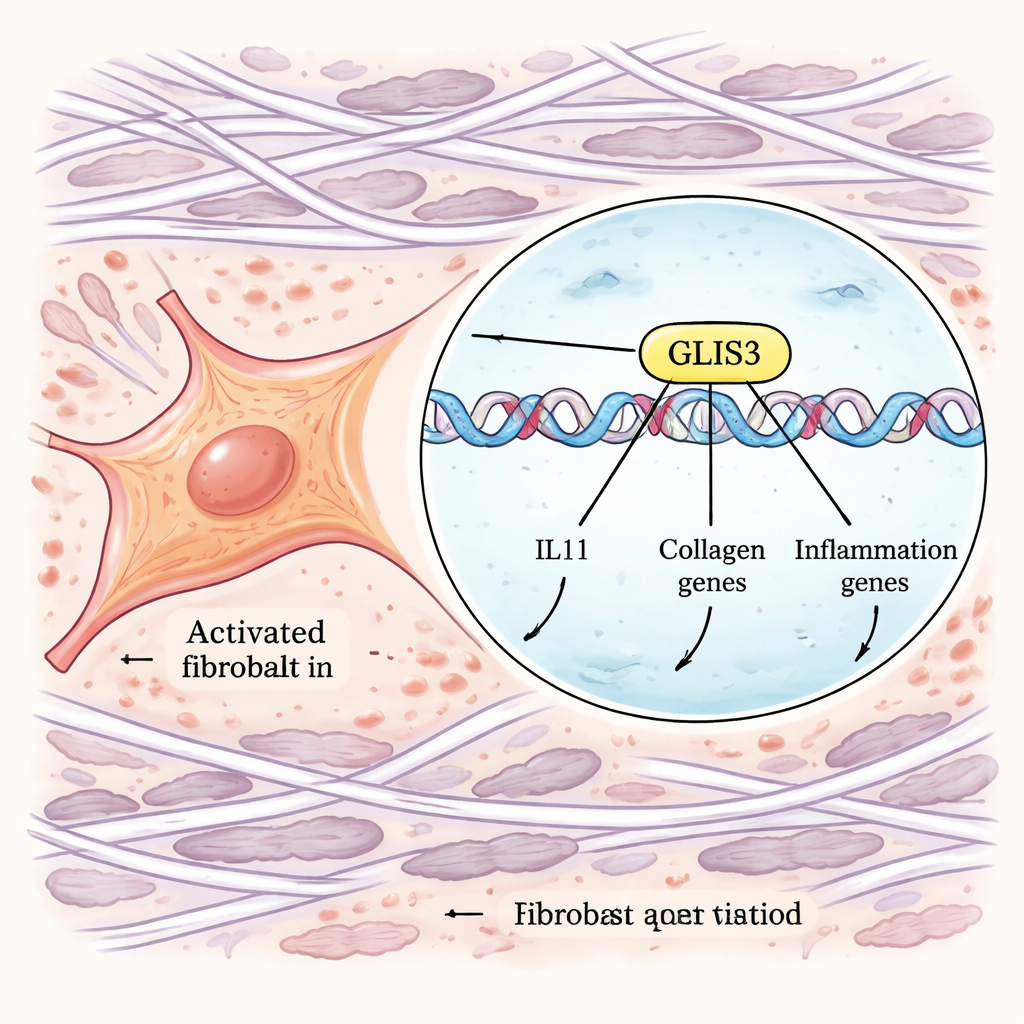
Dal modello murino alla gravità nei pazienti
Il gruppo si è poi chiesto se questo programma guidato da GLIS3 avesse rilevanza negli organismi viventi. Nei topi hanno creato una linea in cui GLIS3 poteva essere rimosso solo dai fibroblasti. Quando questi animali sono stati sottoposti a colite cronica, hanno sviluppato meno cicatrizzazione intestinale, livelli inferiori di collagene e di espressione di geni fibrotici, e hanno mostrato una riduzione dell’infiammazione rispetto ai topi normali. Il mappaggio spaziale ha confermato che nei topi privi di GLIS3 c’erano meno fibroblasti produttori di IL-11 e meno macrofagi attivati e neutrofili nelle vicinanze, indicando che interrompere GLIS3 indebolisce l’intero circuito infiammatorio-fibrotico. Rivolgendosi a una ampia coorte pediatrica di colite ulcerosa, gli autori hanno derivato una “firma” di GLIS3 di 50 geni e hanno trovato che la sua attività nelle biopsie del colon seguiva da vicino la gravità della malattia e l’abbondanza di IAF e macrofagi attivati, collegando direttamente questa via agli esiti clinici.
Interrompere il ciclo di infiammazione e cicatrizzazione
Per i non specialisti, il succo è che questo lavoro rivela un circuito auto‑rinforzante: i macrofagi infiammatori inducono i fibroblasti a diventare IAF formatori di cicatrici; questi IAF, sotto il controllo di GLIS3, secernono IL-11, collagene e altri fattori che rimodellano il tessuto e attirano altre cellule infiammatorie. I farmaci standard che sopprimono in modo ampio il sistema immunitario potrebbero non interrompere completamente questo circuito, il che aiuta a spiegare perché molti pazienti alla fine non rispondono più alle terapie esistenti. Identificando GLIS3 e lo stato dei fibroblasti produttori di IL-11 come nodi centrali nel circuito infiammazione–fibrosi, questo studio indica strategie più mirate—dirette ai fibroblasti piuttosto che solo alle cellule immunitarie—che potrebbero un giorno prevenire o invertire la cicatrizzazione nelle malattie infiammatorie intestinali e possibilmente in altre condizioni infiammatorie croniche.
Citazione: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
Parole chiave: malattia infiammatoria intestinale, fibrosi intestinale, fibroblasti, macrofagi, GLIS3