Clear Sky Science · it
Lo stress controlla l’ereditarietà dell’eterocromatina tramite l’ubiquitinazione dell’istone H3
Come le cellule ricordano lo stress
Le nostre cellule hanno bisogno di modi per “ricordare” stress passati — come calore, carenza di nutrienti o esposizione a farmaci — in modo da poter rispondere più rapidamente la volta successiva. Un potente sistema di memoria si basa sull’eterocromatina, DNA strettamente compattato che mantiene certi geni spenti per molte divisioni cellulari. Questo articolo esplora come le cellule modulino attivamente tale memoria in risposta allo stress, rivelando un punto di controllo molecolare che collega segnali ambientali a cambiamenti duraturi nell’attività genica. Comprendere questo sistema di controllo potrebbe aiutare a spiegare come i funghi evolvono la resistenza ai farmaci e come lo stress rimodella il paesaggio epigenetico delle nostre stesse cellule.
Un lucchetto sul genoma
L’eterocromatina può essere pensata come un lucchetto molecolare su tratti di DNA, che mantiene silenti i geni vicini. Quel lucchetto è costruito da segni chimici sulle proteine istoniche, in particolare una marcatura chiamata H3K9me3. Una volta stabilita, può ricopiarsi ogni volta che il DNA viene replicato, permettendo che i modelli di repressione genica siano ereditati senza alterare la sequenza del DNA sottostante. Fino ad ora, la maggior parte dei lavori suggeriva che questa ricopiatura si basasse principalmente su un circuito di retroazione “leggi‑e‑scrivi”: un complesso enzimatico riconosce i marchi H3K9me3 esistenti e aggiunge lo stesso marchio agli istoni vicini, espandendo gradualmente il dominio silente. Ma questo modello non riusciva a spiegare pienamente come le condizioni ambientali accelerino, rallentino o reindirizzino la diffusione dell’eterocromatina.
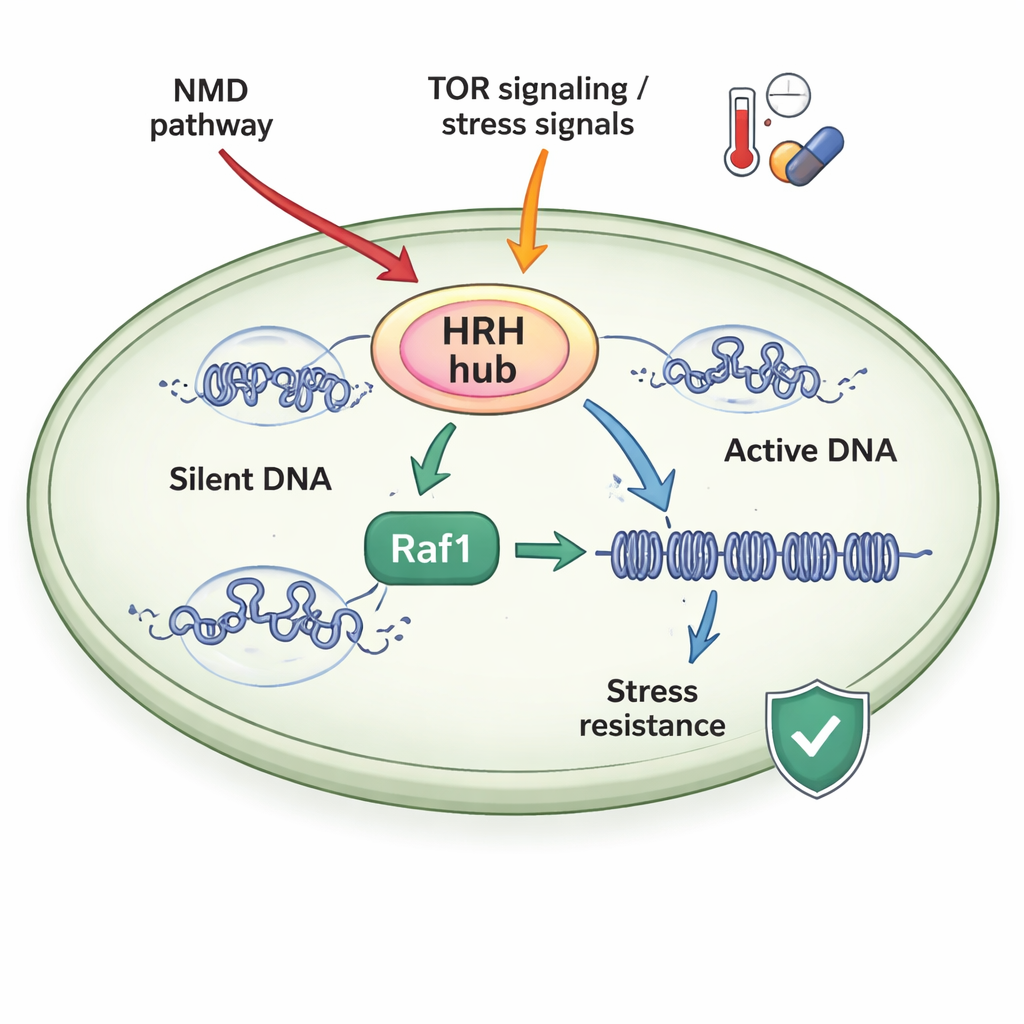
Un hub di controllo sensibile allo stress
Gli autori hanno studiato il lievito della fissione, un semplice organismo modello la cui macchina cromatinica somiglia strettamente a quella degli organismi superiori. Si sono concentrati su un complesso chiamato ClrC, che sia scrive il marchio H3K9me3 sia lega una piccola proteina, l’ubiquitina, a un’altra posizione sull’istone H3 (H3K14ub). Una subunità chiave di ClrC, Raf1, funziona come un “portinaio” limitante: quando Raf1 è scarso, gran parte dell’enzima principale (Clr4) resta libera invece di unirsi al complesso sul cromatina, e i domini silenti non riescono a propagarsi. Quando Raf1 è abbondante, si assembla più ClrC e il complesso resta legato stabilmente al DNA, permettendo ai marchi H3K14ub e H3K9me3 di estendersi lungo i cromosomi e rafforzare il silenziamento genico.
Affinare il lucchetto con l’ubiquitina
Mappando i marchi cromatinici attraverso il genoma, il gruppo ha mostrato che H3K14ub è altamente arricchito dovunque si formi eterocromatina e che questo marchio scompare praticamente se Raf1 viene rimosso. Quando le cellule portano una mutazione che blocca il passo di aggiunta dell’ubiquitina (lasciando intatto H3K9me3 nel punto di partenza), i domini silenti non riescono a propagarsi verso l’esterno. In altre parole, H3K14ub non è solo ornamentale; è necessario per spingere in avanti il fronte dell’eterocromatina. Esperimenti biochimici e di imaging rivelano il perché: H3K14ub aumenta fortemente l’attività dell’enzima Clr4 e aiuta a mantenere l’intero complesso ancorato alla cromatina, innalzando la densità locale di H3K9me3 al di sopra della soglia necessaria per un’ereditarietà stabile. È notevole che aumentare i livelli di Raf1 possa bypassare diversi altri fattori normalmente necessari a mantenere questi domini silenti, sottolineando che l’ubiquitinazione guidata da Raf1 è una leva di controllo centrale.
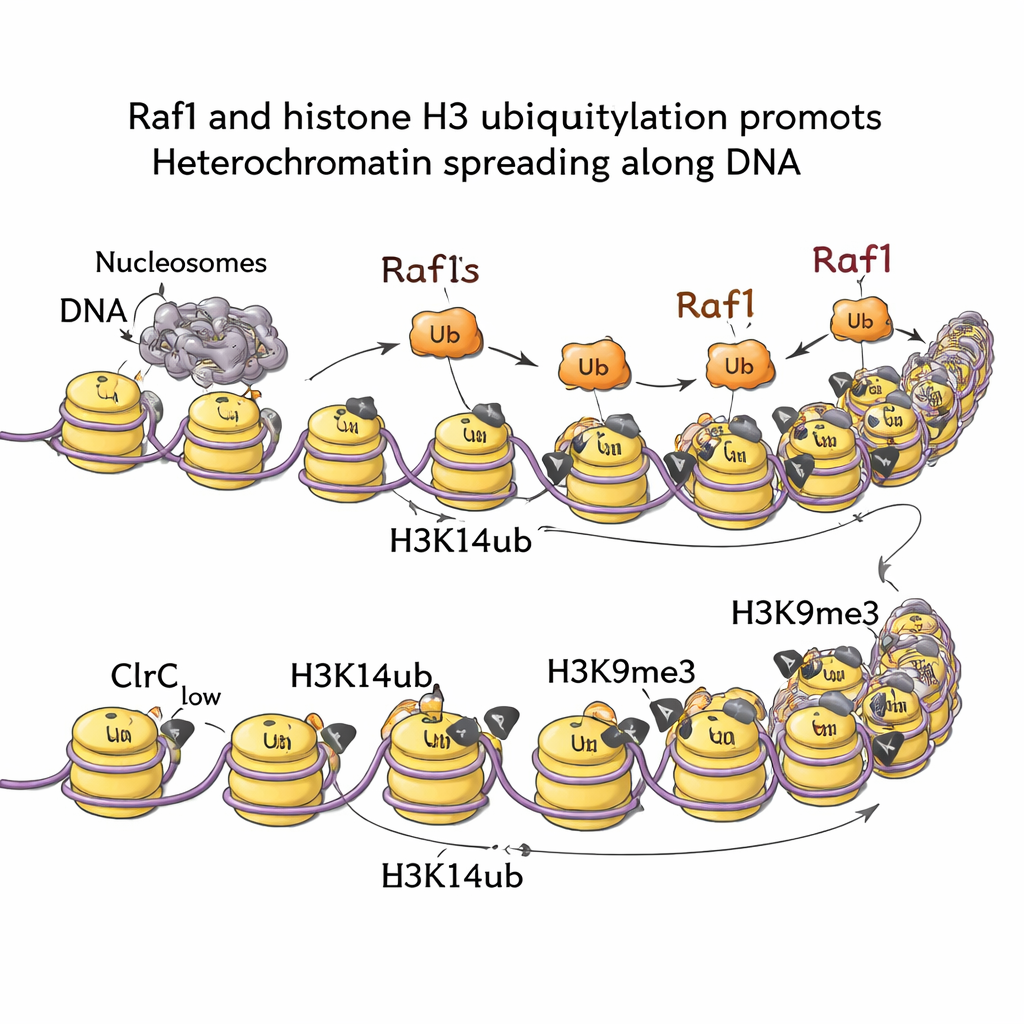
Segnali dal decadimento dell’RNA e dalle vie di crescita
Le cellule non lasciano i livelli di Raf1 al caso. Lo studio mostra che due grandi sistemi sensibili allo stress confluiscono in quello che gli autori chiamano un hub regolatore dell’ereditabilità dell’eterocromatina (HRH), centrato su Raf1. Primo, la via del decadimento mediato da nonsense (NMD) — nota soprattutto per distruggere RNA messaggeri difettosi — prende di mira l’mRNA che codifica Raf1, mantenendo bassi i livelli di Raf1 in condizioni normali. Disabilitare la NMD stabilizza l’RNA di Raf1, aumenta l’abbondanza della proteina Raf1 e ripristina la diffusione dell’eterocromatina in mutanti che altrimenti non possono mantenere i domini silenti. Secondo, un sensore di crescita e stress chiamato TORC2, che agisce tramite la chinasi Gad8, promuove l’espressione di Raf1. Alte temperature spengono questa via, abbassano i livelli di Raf1, indeboliscono l’eterocromatina e rendono più difficile per le cellule mantenere gli stati silenti a meno che Raf1 non venga aumentato sperimentalmente.
Stress, resistenza ai farmaci e implicazioni più ampie
Gli autori collegano quindi questo hub molecolare all’adattamento nel mondo reale. L’esposizione del lievito alla caffeina, uno stress noto anche per attenuare la NMD in altri sistemi, aumenta i livelli di Raf1 e favorisce la diffusione dell’eterocromatina in nuovi siti, inclusi geni la cui repressione conferisce resistenza alla caffeina e a farmaci antifungini. Allo stesso modo, le cellule con livelli artificialmente elevati di Raf1 diventano più resistenti a fluconazolo e clotrimazolo, comuni antifungini. Viceversa, quando Raf1 è ridotto — dal calore o dalla perdita del segnale TORC2–Gad8 — l’eterocromatina diventa instabile e la memoria epigenetica svanisce, a meno che Raf1 non venga ripristinato. Poiché proteine simili a Raf1, il complesso ClrC e il marchio H3K14ub hanno tutti controparti in funghi patogeni e nei mammiferi, questi risultati suggeriscono che un hub epigenetico sensibile allo stress analogo possa modellare la resistenza ai farmaci, lo sviluppo e le malattie in molte specie.
Perché è importante
Detto in termini pratici, questo lavoro mostra che il silenziamento genico mediato dalla cromatina non è un lucchetto rigido, ma un sistema intelligente e regolabile. Le cellule usano un hub centrale per leggere i segnali ambientali — variazioni di temperatura, stato dei nutrienti, stress chimici — e modulare Raf1 su o giù. Ciò a sua volta governa quanta parte del genoma è avvolta in un silenzio duraturo e quanto facilmente le cellule possono “riprogammarsi” senza mutare il loro DNA. Scoprendo il ruolo chiave dell’ubiquitinazione dell’istone H3 e del dosaggio di Raf1 in questo processo, lo studio fornisce uno schema di come lo stress possa rimodellare rapidamente il paesaggio epigenetico — e suggerisce nuove strategie per influenzare la resistenza ai farmaci nei funghi o il silenziamento genico aberrante nelle malattie umane.
Citazione: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Parole chiave: eterocromatina, ereditarietà epigenetica, ubiquitinazione degli istoni, adattamento allo stress, resistenza fungina ai farmaci