Clear Sky Science · it
Determinare l’integrità strutturale del DNA origami e la farmacocinetica in vivo
Osservare minuscole macchine di DNA all’interno del corpo
Il DNA può essere piegato come carta in piccole forme tridimensionali, una tecnica nota come DNA origami. Queste nanostrutture possono essere programmate per trasportare farmaci, vaccini o molecole segnale con estrema precisione. Ma una volta iniettate nel corpo, rimangono integre abbastanza a lungo da funzionare, o si disfano rapidamente? Questo articolo presenta un nuovo modo per osservare queste macchine di DNA in azione negli animali viventi, rivelando quanto tempo sopravvivono, come viaggiano nel flusso sanguigno e persino quali parti di ogni struttura si rompono per prime.
Perché piegare il DNA può cambiare la medicina
Il DNA origami sfrutta le stesse regole di appaiamento delle basi che conservano le nostre informazioni genetiche, ma le reinterpreta per costruire oggetti su scala nanometrica. I ricercatori possono disporre proteine, farmaci o segnali immunostimolanti su questi oggetti come perni su una piastra Lego, creando terapie altamente controllate per cancro, malattie autoimmuni e infezioni. Perché tali trattamenti di precisione siano sicuri ed efficaci, regolatori e scienziati devono sapere quanto queste strutture rimangono integre nel corpo e quanto velocemente vengono eliminate—insieme conosciute come farmacocinetica. I metodi di tracciamento esistenti di solito legano coloranti fluorescenti o semplicemente contano frammenti di DNA, il che può far sembrare detriti disassemblati come nanostrutture ancora integre. Fino a oggi non esisteva un modo pratico per distinguere, negli animali viventi, se le forme originali del DNA origami siano ancora complete.
Un “test di integrità” molecolare per il DNA origami
Il gruppo ha sviluppato un metodo che chiamano PLASTIQ, acronimo di proximity ligation assay for structural tracking and integrity quantification. L’idea chiave è lasciare che il DNA origami riporti il proprio stato. In posizioni specifiche di ogni struttura, i ricercatori inseriscono coppie di brevi staple di DNA che stanno spalla a spalla lungo un’elica quando l’origami è piegato correttamente. Uno di ciascuna coppia porta un piccolo tag chimico che permette di essere uniti enzimaticamente, o ligati, ma solo se sono ancora tenuti vicini da un filamento di scaffold integro. Se la struttura si scioglie, si rompe o viene degradatta dagli enzimi, quei due pezzi si allontanano e non possono più essere ligati. Dopo la ligazione, le coppie unite vengono amplificate usando la reazione a catena della polimerasi standard e quantify mediante qPCR sensibile o sequenziamento, trasformando la presenza di segmenti locali integri in segnali misurabili da pochi microlitri di sangue.
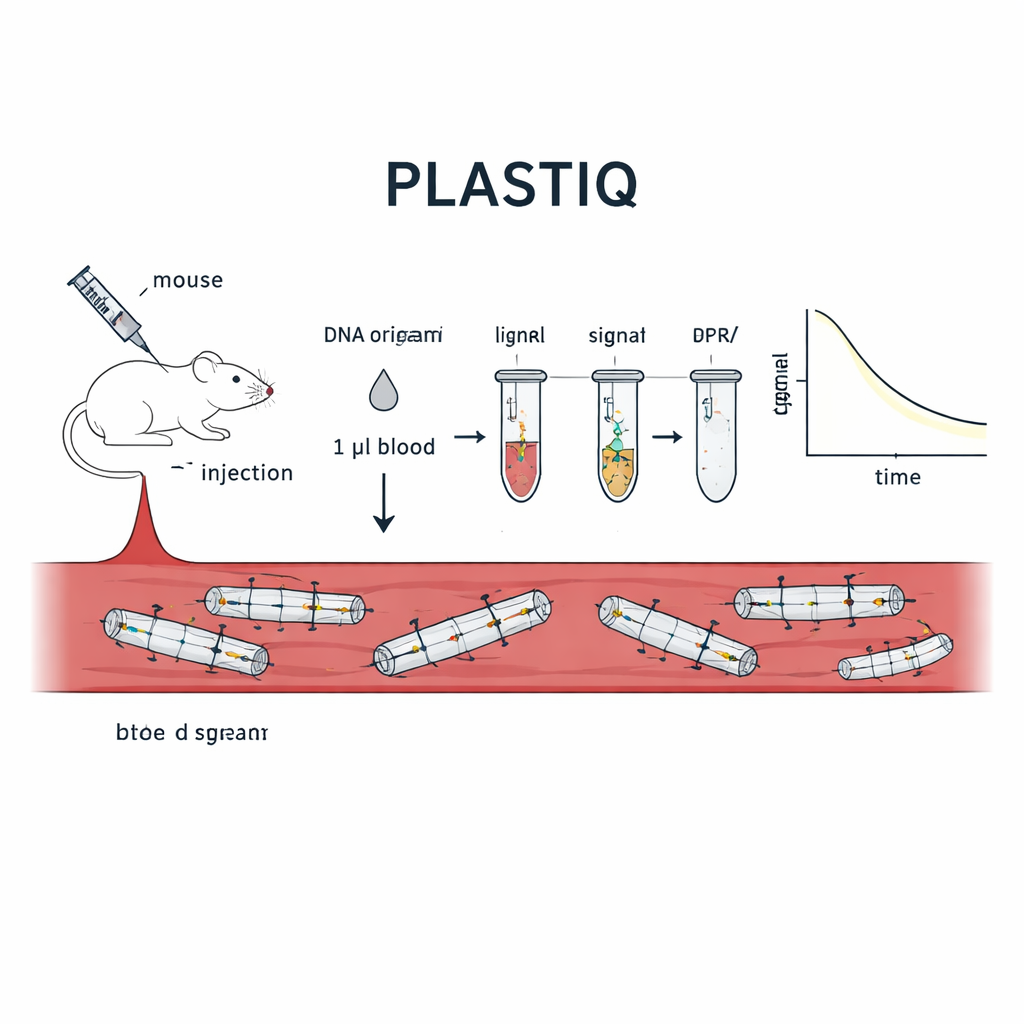
Applicare il test su topi viventi
Per dimostrare che PLASTIQ misura davvero l’integrità strutturale, gli autori lo hanno prima applicato a semplici progettazioni di DNA origami a forma di asta in provetta. I segnali apparivano solo quando le aste erano integre e sparivano dopo il disfacimento indotto dal calore, mentre saggi più tradizionali basati sul DNA registravano ancora presenza di DNA indipendentemente dalla forma. Successivamente hanno iniettato queste aste nei topi attraverso diverse vie—direttamente nel flusso sanguigno, nella cavità addominale, nel muscolo e sotto la pelle—e prelevato solamente un microlitro di sangue a intervalli temporali. PLASTIQ ha rivelato come la concentrazione di strutture integre aumentasse e poi calasse, a seconda della via di iniezione, corrispondendo alle aspettative generali della farmacologia dei farmaci ma con dettagli strutturali molto più fini. Il metodo era sensibile fino a 0,01 femtomolare, richiedendo però un sangue minimo, permettendo campionamenti ripetuti dallo stesso animale per ore.
Testare rivestimenti protettivi e punti deboli nascosti
Molti gruppi cercano di proteggere il DNA origami rivestendolo con polimeri come il PEG, reticolando gli strand con luce ultravioletta o aggiungendo leganti chimici, ma è stato difficile valutare quanto questi stratagemmi aiutino effettivamente in vivo. Usando PLASTIQ, gli autori hanno mostrato che le aste rivestite con PEG nel flusso sanguigno rimangono intatte leggermente più a lungo rispetto a quelle nude ma vengono anche eliminate più rapidamente una volta raggiunta la circolazione, e che il rivestimento non impedisce agli enzimi PLASTIQ di svolgere il proprio lavoro. Combinando PLASTIQ con modelli matematici semplici, hanno estratto i tassi di assorbimento ed eliminazione per diverse vie di iniezione e rivestimenti, e sono stati in grado persino di simulare schemi di somministrazione ripetuta. Hanno poi spinto il metodo oltre con un origami a forma di barile a doppio strato, confezionato più densamente all’interno che all’esterno. Le misure PLASTIQ hanno mostrato che gli staple sulla superficie esterna esposta perdevano integrità più rapidamente di quelli rivolti verso la cavità interna, confermando direttamente che le eliche sepolte sono schermate dagli enzimi degradanti nel sangue.
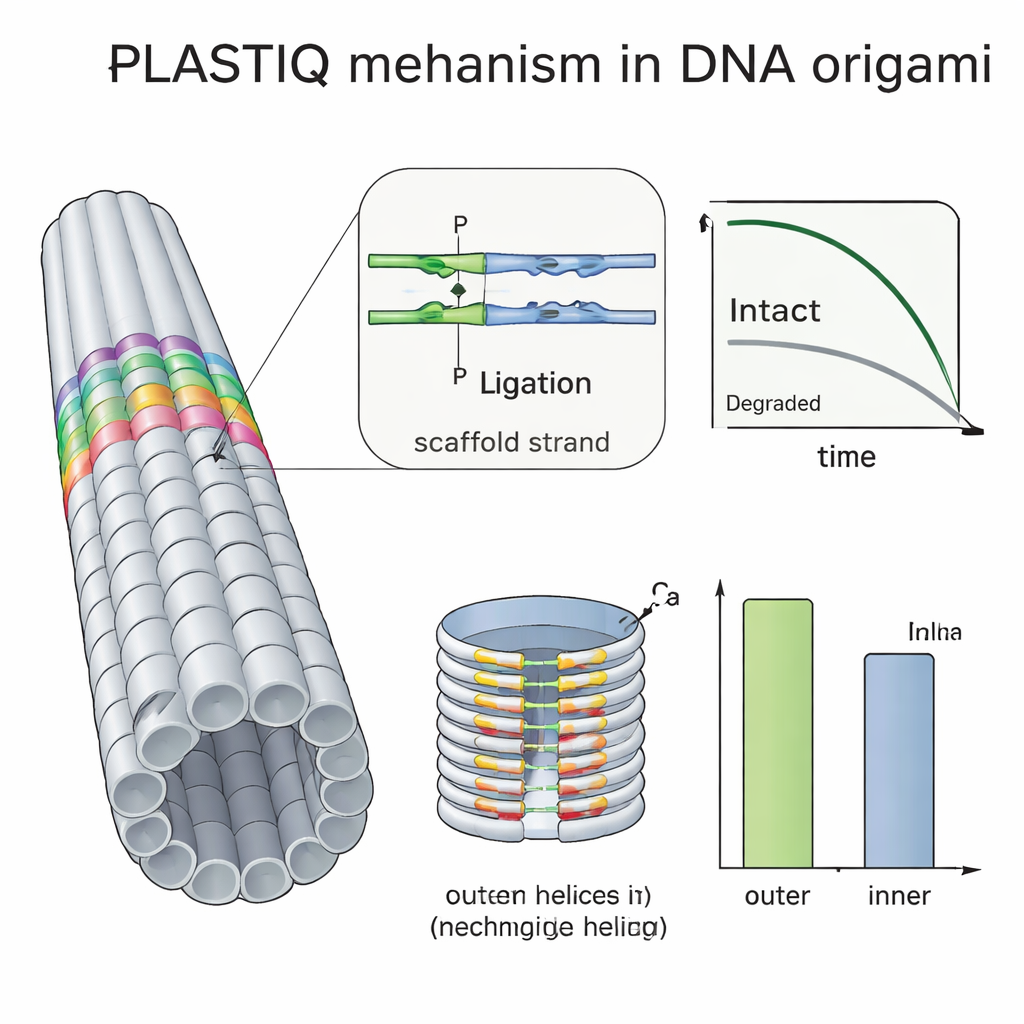
Cosa significa questo per le future terapie a base di DNA
Per un non specialista, PLASTIQ può essere visto come un controllo strutturale per dispositivi di DNA su scala nanometrica che viaggiano nel corpo. Invece di chiedere semplicemente “c’è DNA qui?”, pone la domanda “questo DNA è ancora piegato nell’oggetto preciso che abbiamo progettato?”. Rispondendo a questa domanda con alta sensibilità a partire da piccole quantità di sangue, PLASTIQ offre agli sviluppatori di farmaci un modo per ottimizzare il design, il rivestimento e il dosaggio dei medicinali e dei vaccini basati su DNA origami. Col tempo, tale conoscenza dettagliata e quantitativa su come queste nanostrutture si comportano in ambienti biologici reali potrebbe aiutare a trasformare il DNA origami da un elegante concetto di laboratorio in terapie affidabili e pronte per i regolatori.
Citazione: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Parole chiave: DNA origami, nanomedicina, consegna di farmaci, farmacocinetica, nanotecnologia