Clear Sky Science · it
La disattivazione della triptofanasi favorisce il mutualismo insetto–batterio
Come i piccoli partner intestinali possono fare la differenza per un insetto
Molti animali, compresi gli esseri umani, dipendono da trilioni di microbi che vivono nell’intestino. Questi partner nascosti possono aiutare a digerire il cibo, produrre vitamine o, in alcuni casi, causarci malattie. Questo studio esamina una modifica genetica semplice ma sorprendente nei batteri che trasforma un microbo ordinario in un partner che salva la vita di una cimice fitofaga. Focalizzandosi su un singolo gene batterico, il lavoro mostra come un cambiamento microscopico possa innescare un’amicizia stabile tra forme di vita molto diverse.
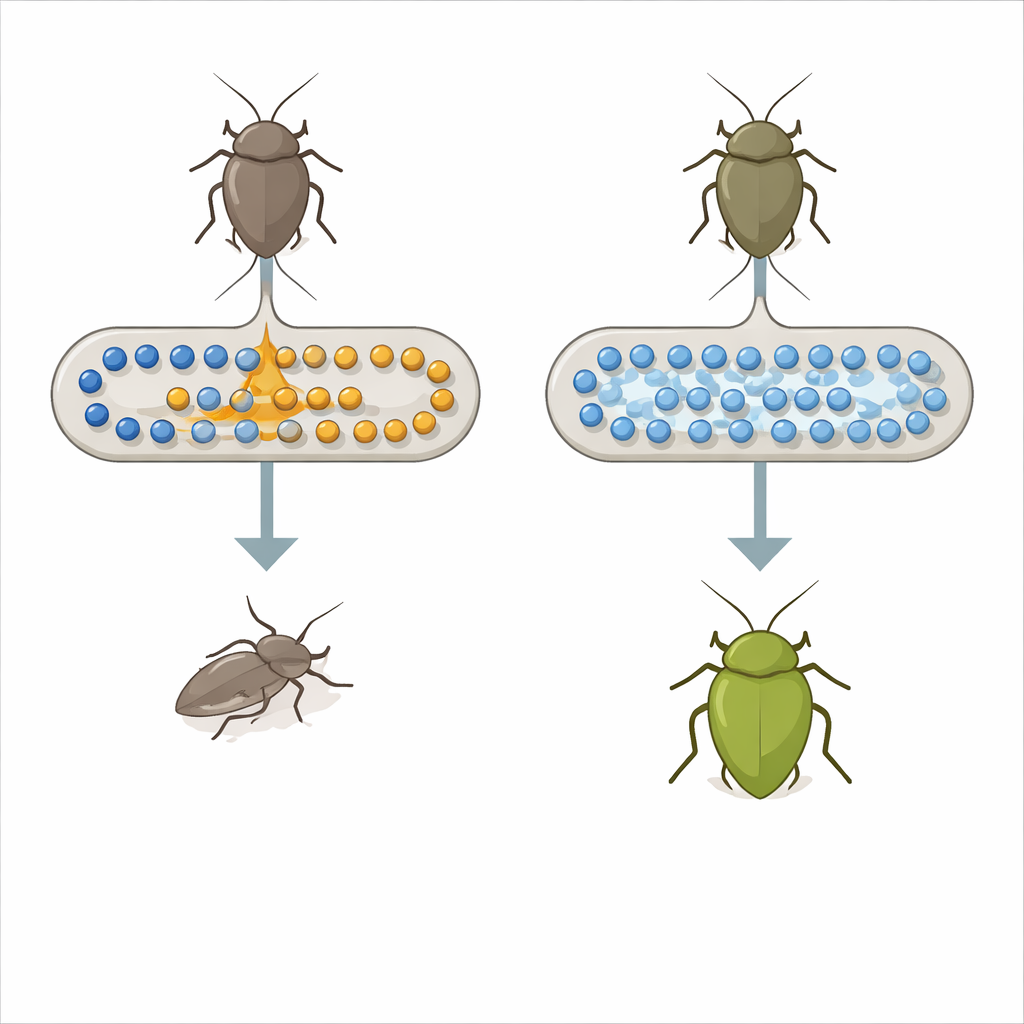
Una cimice, un batterio e un’alleanza inattesa
La cimice Plautia stali dipende da batteri speciali che vivono in una sacca del suo intestino medio per crescere e sopravvivere. In natura, questi partner sono di solito membri del genere Pantoea, che forniscono nutrienti che l’insetto non può ottenere dalla sola linfa delle piante. Lavori di laboratorio avevano già dimostrato che un ceppo di laboratorio comune di Escherichia coli, tipico batterio intestinale dei mammiferi, può evolvere rapidamente in un partner utile per questa cimice dopo una sola mutazione in un sistema di controllo globale chiamato repressione catabolica del carbonio. Quel risultato precedente sollevava una grande domanda: un cambiamento regolatorio così drastico è davvero il modo in cui sorgono i simbiosi utili in natura, o esiste un interruttore genetico più mirato?
Seguire la pista di un singolo mattoncino
Per rispondere, i ricercatori hanno confrontato cimici portatrici di E. coli ordinario con quelle portatrici di mutanti di E. coli evoluti e più utili. Hanno misurato molte piccole molecole nel sangue e nell’intestino degli insetti. Un amminoacido essenziale, il triptofano, è emerso in modo evidente: i suoi livelli erano più di dieci volte superiori negli insetti che ospitavano i mutanti utili rispetto a quelli con E. coli normale. Tra le dozzine di geni batterici influenzati dalla precedente mutazione regolatoria, due erano collegati all’elaborazione del triptofano. Uno, chiamato tnaA, codifica per un enzima che degrada il triptofano in un composto chiamato indolo insieme ad altri prodotti; l’altro aiuta a trasportare il triptofano nella cellula. Quando il team ha cancellato il gene tnaA da E. coli, le cimici hanno improvvisamente mostrato un netto miglioramento, con maggiore sopravvivenza e un ricco colore verde del corpo, caratteristico di insetti sani e ben nutriti.
Quando meno distruzione significa più aiuto
La modifica chiave non si è rivelata essere che i batteri producessero più triptofano, ma che cessassero di distruggerlo e di generare indolo in eccesso. Gli insetti che ospitavano E. coli privi di tnaA avevano alti livelli di triptofano e quasi nessun indolo circolante nei loro corpi. Al contrario, gli insetti con E. coli normale avevano poco triptofano e molto più indolo. Esperimenti di somministrazione hanno confermato questo quadro: fornire indolo nell’acqua da bere danneggiava gli insetti, specialmente quelli con batteri produttori di indolo, mentre un eccesso di triptofano era dannoso solo quando i batteri potevano convertirlo in ulteriore indolo. Un diverso ceppo di E. coli ingegnerizzato per sovraprodurre triptofano ha dato agli insetti un modesto beneficio, rafforzando l’idea che più di questo mattoncino e meno prodotto di degradazione tossico migliorino la salute dell’insetto.
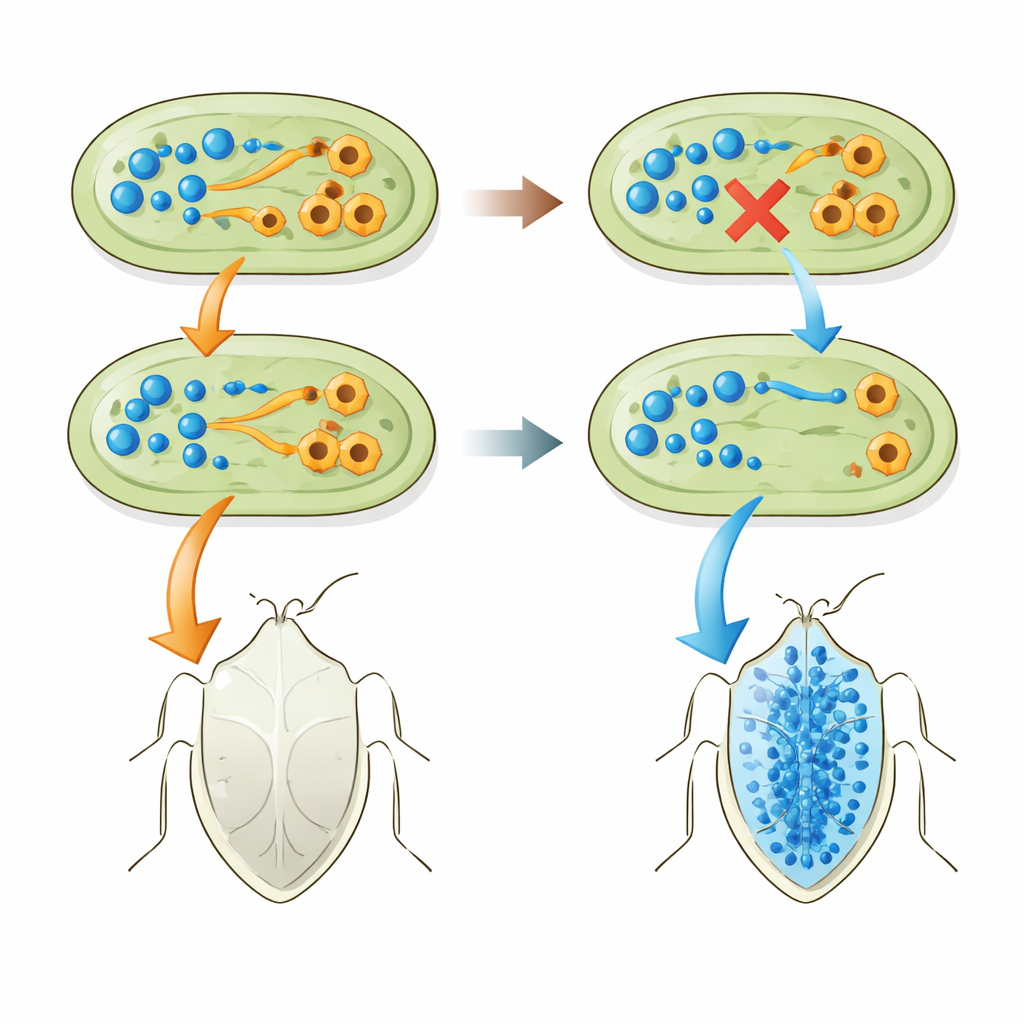
I partner naturali condividono la stessa perdita genetica
Il team si è poi chiesto se questa stessa perdita genica si presenti nelle simbiosi del mondo reale. Hanno sequenziato i genomi di molti batteri Pantoea che vivono dentro P. stali e cimici affini nelle isole Ryukyu del Giappone, così come ceppi di Pantoea isolati dal suolo che potevano essere indotti a aiutare le cimici. Colpisce che ogni simbiote di successo o potenzialmente di successo fosse privo del gene tnaA e non mostrasse attività dell’enzima che scinde il triptofano. Per contro, diversi ceppi di Pantoea ananatis liberi in natura che ancora possedevano tnaA non erano in grado di sostenere lo sviluppo delle cimici. Quando i ricercatori hanno eliminato tnaA in uno di questi ceppi di P. ananatis, la sua capacità di aiutare gli insetti è migliorata, sebbene non raggiungesse il livello dei partner naturali. E quando hanno costretto un simbiote naturale a portare un operone tnaA attivo, le cimici sono andate peggio e presentavano minori livelli di triptofano e maggiori di indolo nel loro sangue.
Cosa significa per le alleanze nascoste della vita
Nel complesso, i risultati indicano una regola semplice ma potente: i batteri che smettono di degradare il triptofano, evitando così di inondare l’ospite di indolo, hanno maggiori probabilità di diventare partner affidabili per le cimici che si nutrono di piante. In laboratorio, ciò può essere innescato da una mutazione in un sistema regolatorio globale; in natura, si manifesta come una perdita diretta del gene che scinde il triptofano. In entrambi i casi, disattivare quell’unico enzima aiuta ad allineare gli interessi dell’insetto e del microbo. Lo studio suggerisce che il percorso da un’associazione superficiale a un mutualismo stretto può talvolta dipendere da passi genetici sorprendentemente piccoli e che perdite di funzione simili nel metabolismo batterico potrebbero essere alla base di molte altre alleanze nascoste sull’albero della vita.
Citazione: Wang, Y., Moriyama, M., Koga, R. et al. Tryptophanase disruption promotes insect–bacterium mutualism. Nat Microbiol 11, 759–769 (2026). https://doi.org/10.1038/s41564-026-02264-z
Parole chiave: microbioma degli insetti, mutualismo batterico, metabolismo del triptofano, evoluzione della simbiosi, simbioti Pantoea