Clear Sky Science · it
La vaccinazione con mRNA supera l’impedimento mediato dall’emozoin ai vaccini antimalarici a parassita intero nei topi
Perché la malaria pregressa rende i vaccini meno efficaci
La malaria uccide centinaia di migliaia di persone ogni anno, e uno dei vaccini più promettenti usa parassiti interi attenuati per addestrare il sistema immunitario. Eppure, curiosamente, questo approccio «gold standard» funziona molto meglio nelle persone che non hanno mai avuto la malaria rispetto a chi è cresciuto in zone dove la malattia è comune. Questo studio, condotto nei topi, pone una domanda semplice ma cruciale: che cosa delle infezioni malariche precedenti fa sì che un vaccino altamente efficace improvvisamente perda potenza — e un nuovo tipo di vaccino a mRNA può risolvere il problema?
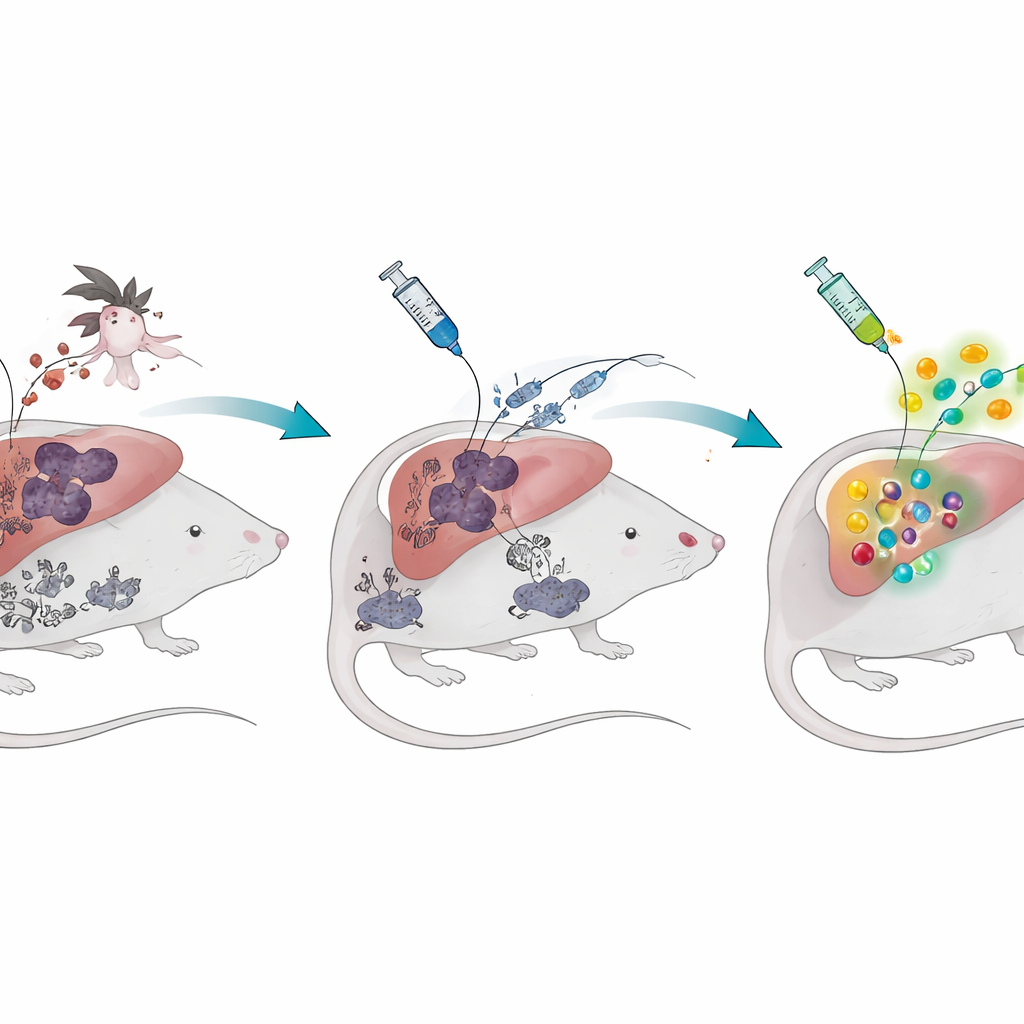
Il racconto di due stadi della malaria
Il parassita della malaria ha due stadi principali nell’organismo umano. Prima, dopo la puntura di una zanzara, infetta silenziosamente il fegato. Più tardi invade i globuli rossi, causando febbre e malattia. I vaccini a parassita intero, detti sporozoiti attenuati tramite radiazioni, mirano allo stadio epatico silenzioso: i parassiti entrano nelle cellule del fegato ma non possono completare il loro ciclo vitale, offrendo al sistema immunitario un’anteprima sicura. Nei topi privi di esposizione alla malaria, questa strategia genera un gran numero di cellule T citotossiche specializzate che si insediano nel fegato e possono eliminare i parassiti prima che causino malattia. Ma quando i ricercatori hanno prima infettato i topi con la forma ematica della malaria e ne hanno lasciato risolversi l’infezione, lo stesso vaccino ha prodotto molte meno cellule T protettive e gli animali sono risultati molto meno protetti quando esposti a parassiti vivi.
Un pigmento persistente che non se ne va
Il gruppo ha quindi indagato cosa fosse diverso in questi topi «con esperienza di malaria». Un sospetto evidente è stato l’emozoin, un pigmento scuro, simile a cristalli, che il parassita produce all’interno dei globuli rossi per detossificare i prodotti di scarto ricchi di ferro derivati dalla digestione dell’emoglobina. Questo pigmento non scompare quando l’infezione si risolve; può rimanere nel fegato, nella milza e nel midollo osseo per molti mesi. Gli scienziati hanno rilevato che anche più di un anno dopo la risoluzione di un’infezione ematica, i topi mostravano sia emozoin immagazzinato sia una risposta delle cellule T indebolita al vaccino contro lo stadio epatico. Somministrare a topi sani emozoin sintetico purificato — senza alcun parassita vivo — è stato sufficiente per riprodurre questa debolezza vaccinale di lunga durata e ridurre la protezione contro una successiva sfida con la malaria.
Come l’emozoin ostacola le sentinelle immunitarie
Approfondendo, i ricercatori si sono concentrati sulle cellule dendritiche, le sentinelle del sistema immunitario che raccolgono frammenti di patogeni e li presentano alle cellule T. Perché il vaccino epatico a parassita intero funzioni, le cellule dendritiche devono catturare il materiale parassitario proveniente dalle cellule epatiche infette e mostrarlo alle cellule T citotossiche. In esperimenti in coltura cellulare, il gruppo ha dimostrato che l’emozoin interferisce direttamente con questa fase di raccolta: più emozoin le cellule dendritiche avevano incontrato, meno efficacemente ingerivano antigeni proteici. Questo difetto è apparso sia nelle cellule murine sia in cellule immunitarie umane ottenute da donatori di sangue, e non dipendeva da un noto sensore infiammatorio, suggerendo che l’emozoin agisca di per sé come un ostacolo fisico o biochimico alla normale gestione degli antigeni.
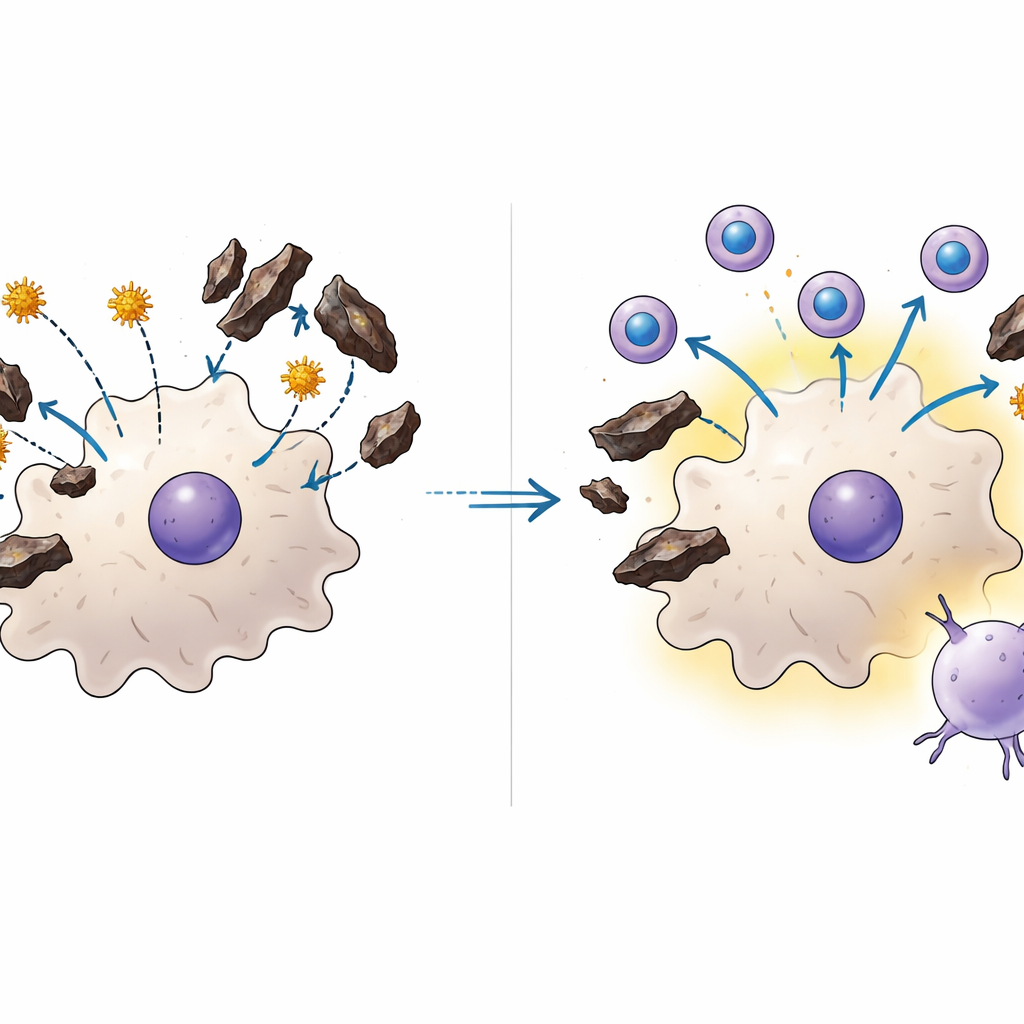
I vaccini a mRNA aggirano l’ostacolo
Per verificare se un formato vaccinale diverso potesse eludere questo problema, gli scienziati hanno progettato un vaccino a mRNA confezionato in nanoparticelle lipidiche. Invece di fornire proteine parassitarie dall’esterno, questo approccio dà alle cellule dell’ospite istruzioni genetiche per produrre al loro interno brevi frammenti di diverse proteine parassitarie. Nei topi con o senza malaria pregressa, il vaccino a mRNA ha generato risposte forti e simili di cellule T citotossiche e ha migliorato il controllo dell’infezione epatica. Colpisce che, quando il vaccino a mRNA è stato combinato con una singola dose del vaccino epatico a parassita intero, i topi hanno sviluppato pool particolarmente ampi di cellule T che hanno preso residenza a lungo termine nel fegato — una popolazione cellulare nota per essere cruciale per una protezione rapida. In colture, l’emozoin non ha bloccato l’ingresso né la funzione delle nanoparticelle cariche di mRNA, spiegando come questa strategia possa avere successo dove il vaccino più vecchio, da solo, fallisce.
Cosa significa per i futuri vaccini antimalarici
In termini pratici, lo studio mostra che le infezioni malariche pregresse lasciano detriti microscopici simili a minerali che intasano il modo in cui certe cellule immunitarie apprendono normalmente dai vaccini, indebolendo un importante vaccino antimalarico a parassita intero. Ma passando a, o combinando con, un vaccino a base di mRNA che fa entrare direttamente nelle cellule le istruzioni per frammenti di parassita, gli scienziati possono bypassare questi detriti e ripristinare una protezione forte negli ospiti con esperienza di malaria — almeno nei topi. Il lavoro indica l’emozoin come un ostacolo rilevante per i vaccini nelle persone che vivono in regioni endemiche e suggerisce che regimi vaccinali a mRNA o misti, progettati con attenzione, potrebbero essere una strada promettente verso un’immunizzazione antimalarica più efficace e ampiamente utile.
Citazione: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Parole chiave: vaccini contro la malaria, emozoin, vaccino a mRNA, immunità mediata da cellule T, infezione da Plasmodium