Clear Sky Science · it
Analisi comparativa dei dataset di deep mutational scanning negli enterovirus A e B individua divergenze funzionali e bersagli terapeutici
Perché i minuscoli virus a RNA ci interessano
Gli enterovirus sono un vasto gruppo di minuscoli virus a RNA che circolano silenziosamente in tutto il mondo, causando di solito raffreddori lievi o gastroenteriti ma talvolta paralisi, danni al cuore o altre malattie gravi. Abbiamo pochi vaccini e ancora meno farmaci efficaci in modo ampio contro di essi, in parte perché questi virus evolvono molto rapidamente. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni pratiche: quando questi virus mutano, quali parti della loro “macchina” possono cambiare liberamente e quali sono così vitali che l’evoluzione le mantiene quasi immutate? Le risposte indicano nuove strategie per progettare terapie difficili da eludere per il virus.
Leggere il manuale del virus, una mutazione alla volta
I ricercatori si sono concentrati su due enterovirus umani che causano malattie molto diverse: Enterovirus A71, collegato a gravi malattie neurologiche nei bambini, e coxsackievirus B3, associato a infiammazione cardiaca e persino a cancro del pancreas. Utilizzando una tecnica chiamata deep mutational scanning, hanno creato librerie virali in cui quasi ogni posizione delle proteine di ciascun virus è stata modificata sistematicamente. Questi virus mutanti sono stati lasciati infettare cellule in coltura e il sequenziamento ad alta produttività è stato usato per misurare come ogni cambiamento influenzasse la crescita virale. Confrontando ogni mutante col virus originale, il gruppo ha costruito una mappa dettagliata di quali siti nel proteoma virale tollerano il cambiamento e quali sono fortemente vincolati. 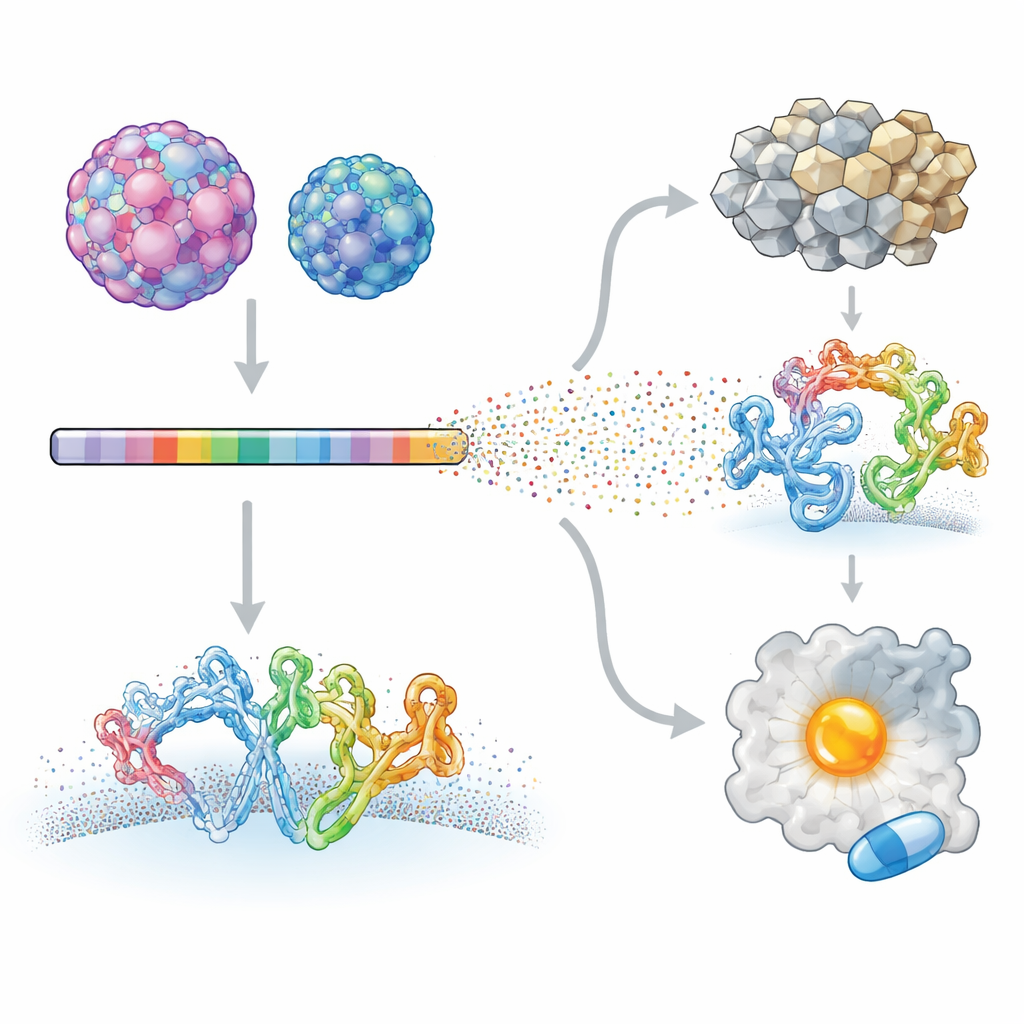
Limiti condivisi e flessibilità specifica del virus
Nonostante condividano solo circa la metà delle sequenze di amminoacidi, i due virus hanno mostrato schemi complessivi di vincolo sorprendentemente simili. I “cavalli da lavoro” enzimatici interni che copiano il genoma, tagliano le proteine virali e svolgono l’RNA erano altamente sensibili alle mutazioni in entrambi i virus. Allo stesso modo, le superfici nascoste che tengono insieme l’involucro proteico, o capsid, si sono rivelate difficili da modificare senza compromettere il virus. Al contrario, molte regioni rivolte verso l’esterno e che interagiscono con l’ospite erano più libere di cambiare e spesso differivano nettamente tra le due specie. L’analisi strutturale ha mostrato che le regioni conservate e intolleranti alle mutazioni si raggruppano attorno ai siti attivi e alle interfacce di assemblaggio, mentre le regioni che toccano recettori cellulari, membrane o molecole immunitarie sono punti caldi di flessibilità specifica della specie.
Come i virus incontrano le cellule e sfuggono alle difese
Il gruppo ha quindi esaminato più da vicino la stretta molecolare tra virus e ospite. Enterovirus A71 e coxsackievirus B3 utilizzano recettori cellulari diversi per entrare, e lo studio ha rilevato che le impronte di contatto esatte sulla superficie del capsid sono tra le regioni maggiormente divergenti in termini di tolleranza alle mutazioni. Residui che afferrano il recettore in un virus sono fortemente vincolati in quel virus ma relativamente permissivi nell’altro, riflettendo come ciascuno abbia perfezionato la propria piattaforma di aggancio. Una divergenza simile è emersa in una piccola proteina associata alla membrana chiamata 3A, che aiuta a rimodellare le membrane cellulari e reclutare fattori ospite per la replicazione del genoma. La modellizzazione suggerisce che i due virus usino parzialmente patch di contatto diverse su 3A per ingaggiare lo stesso fattore ospite, GBF1, e che possano inserire questa proteina nelle membrane a profondità diverse. Queste differenze aiutano a spiegare perché virus strettamente correlati possono infettare tessuti differenti e provocare schemi di malattia distinti.
Cosa l’evoluzione in laboratorio non coglie—and cosa invece riproduce
Per collocare i loro esperimenti in coltura cellulare nel contesto reale, gli autori hanno confrontato le loro mappe di mutazione con migliaia di sequenze virali naturali provenienti da campioni di pazienti. Nel complesso, i siti flessibili in laboratorio tendevano anche ad essere variabili in natura, specialmente nei confronti di confronti su larga scala a livello di specie. Tuttavia, quando hanno esaminato quali specifici amminoacidi fossero preferiti in ogni sito, l’evoluzione naturale e la selezione di laboratorio concordavano più strettamente all’interno di un singolo tipo virale. È significativo che i maggiori disallineamenti si accumulassero sulla superficie esterna del capsid e nelle regioni che interagiscono con l’ospite delle proteine non strutturali 2A e 3A—esattamente dove le risposte immunitarie e gli ambienti ospite complessi dovrebbero avere maggiore peso. Questo suggerisce che il deep mutational scanning cattura i vincoli meccanici di base delle proteine virali, mentre le infezioni reali sovrappongono pressioni aggiuntive provenienti dall’immunità e dalla tropismo tissutale, difficili da riprodurre in vitro.
Trovare un punto debole condiviso per futuri farmaci
Infine, i ricercatori hanno chiesto se queste mappe potessero evidenziare un punto debole comune per lo sviluppo di farmaci. Usando strumenti computazionali, hanno cercato in entrambi i virus tasche sulla superficie delle proteine che, in linea di principio, potrebbero legare piccole molecole. Hanno poi sovrapposto i dati di mutazione per vedere quali tasche erano composte da residui che il virus non può facilmente cambiare senza danneggiarsi. Una tasca, situata sull’elicasi 2C—un motore ad anello che aiuta a svolgere l’RNA virale—è emersa in modo particolare. La sua forma e i residui costituenti sono altamente conservati attraverso quattro principali specie di enterovirus umano, si trovano lontano dai siti attivi già noti, e le mutazioni in quella regione sono sia rare in natura sia fortemente dannose nei test di laboratorio. 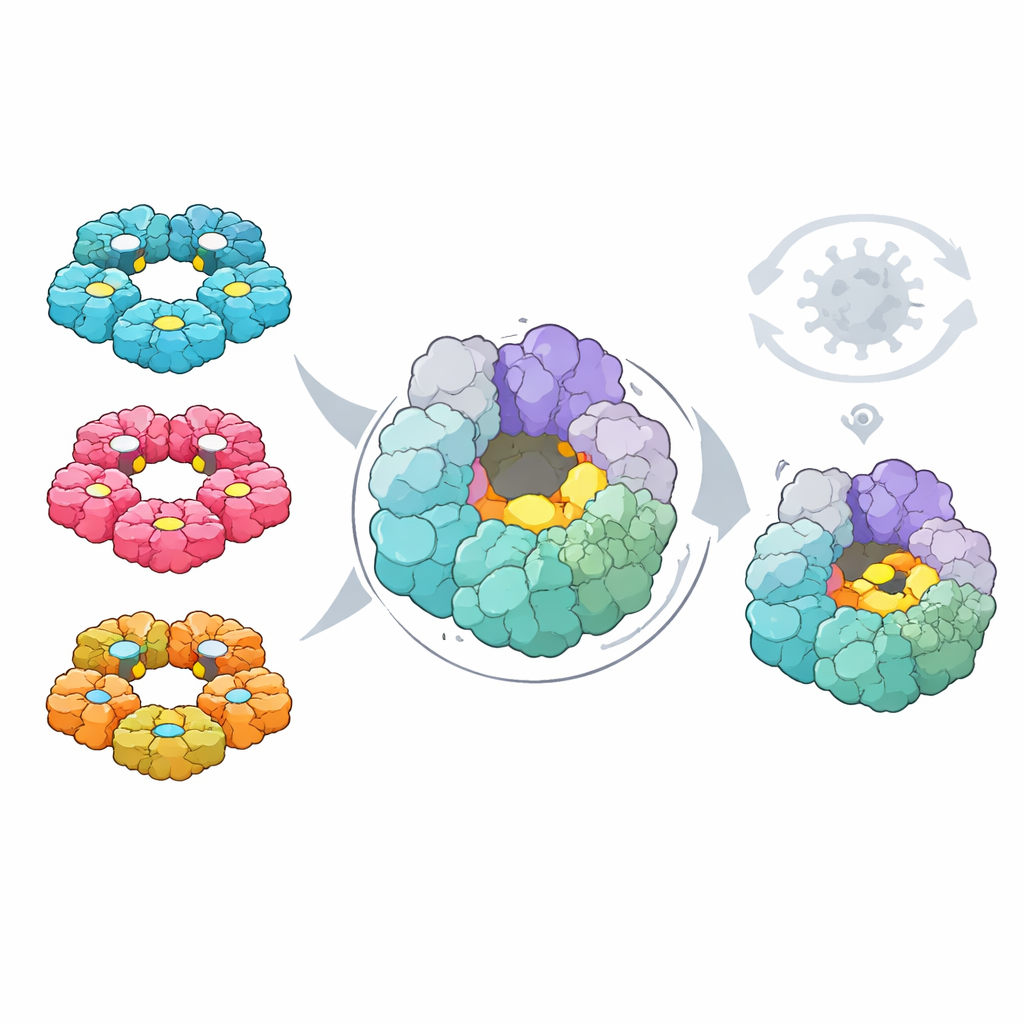
Cosa significa per i trattamenti futuri
Indagando sistematicamente come ogni possibile cambiamento di una singola lettera influisce su due importanti enterovirus, questo studio rivela una chiara divisione tra un nucleo rigido e condiviso della macchina virale e interfacce più flessibili e specifiche per virus che interagiscono con l’ospite. Il nucleo conservato include una tasca recentemente evidenziata sull’elicasi 2C che sembra difficile da mutare per il virus senza sacrificare la fitness, rendendola un bersaglio attraente per antivirali ad ampio spettro con alta barriera alla resistenza. Allo stesso tempo, le superfici esterne più adattabili e i siti di contatto con l’ospite spiegano perché virus correlati si comportano in modo così diverso nell’organismo e indicano dove vaccini e terapie basate sull’immunità devono fare i conti con un’evoluzione rapida. Nel complesso, questi risultati forniscono una road map per progettare trattamenti che sfruttino i limiti evolutivi del virus stesso.
Citazione: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Parole chiave: enterovirus, evoluzione virale, deep mutational scanning, bersagli antivirali, elicasi 2C