Clear Sky Science · it
Ipercorsi H2 nativi consentono l’idrogenazione biocompatibile di alcheni metabolici nei batteri
Trasformare i microbi in piccole fabbriche verdi
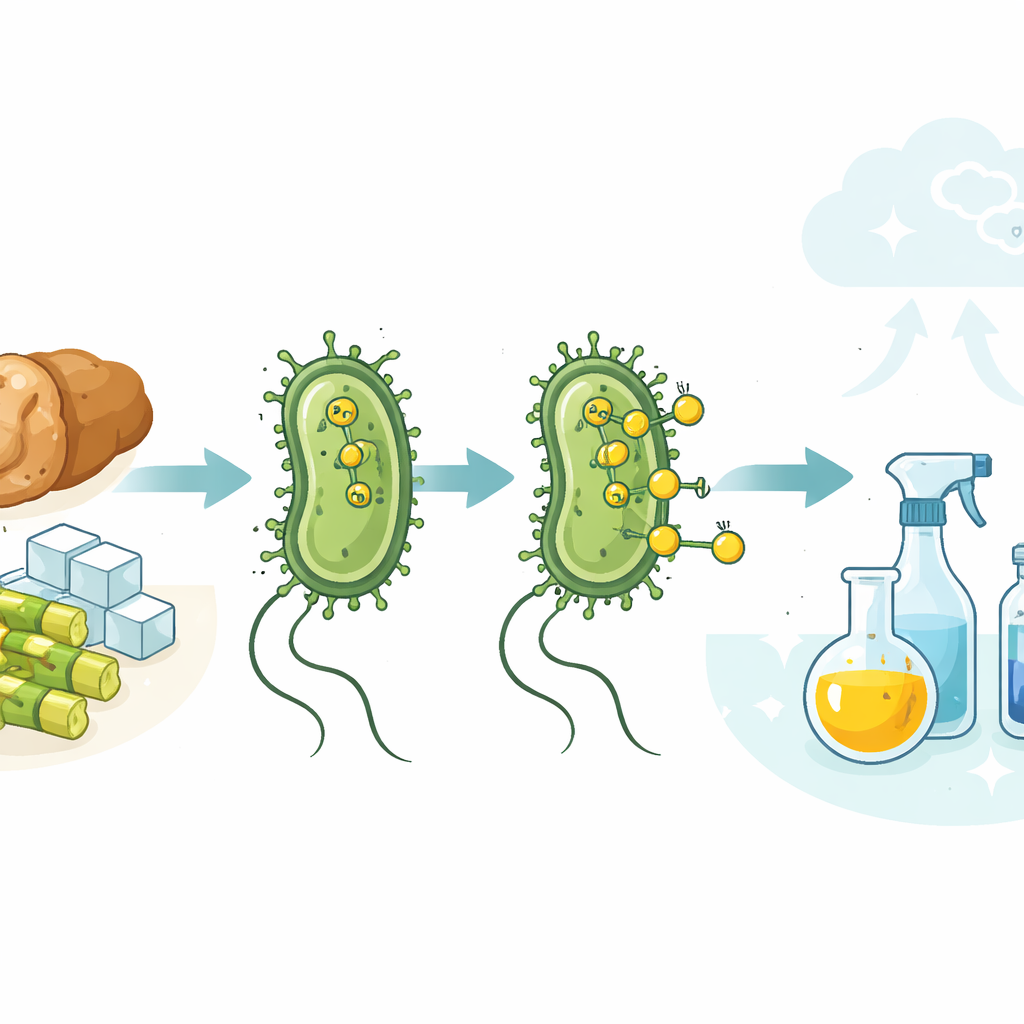
Immaginate se comuni batteri intestinali potessero contribuire a sostituire i combustibili fossili nella produzione di prodotti chimici di uso quotidiano — dai conservanti alimentari alle materie plastiche — pulendo al contempo i rifiuti alimentari. Questo studio dimostra che semplici ceppi di laboratorio di Escherichia coli possono fare proprio questo: producono naturalmente gas idrogeno all’interno delle loro cellule, e quell’idrogeno può essere sfruttato in superficie cellulare per alimentare reazioni chimiche in stile industriale in condizioni delicate e acquose. Accoppiando microbi vivi con un catalizzatore metallico solido, i ricercatori delineano un percorso verso una manifattura più pulita e con minori emissioni di carbonio.
Perché l’idrogeno è importante per i prodotti di uso quotidiano
Il gas idrogeno è al centro della chimica moderna. Viene impiegato per trasformare oli liquidi in spalmabili, migliorare combustibili grezzi e costruire molti ingredienti per medicinali e materie plastiche. Oggi quasi tutto quell’idrogeno proviene da fonti fossili, principalmente gas naturale e carbone, rilasciando grandi quantità di anidride carbonica. Allo stesso tempo, molti microbi rilasciano naturalmente idrogeno mentre degradano zuccheri in condizioni di scarsità di ossigeno. Il problema affrontato dagli autori è come sfruttare questo tenue flusso di idrogeno biologico per guidare gli stessi tipi di reazioni che l’industria esegue oggi con alte pressioni, solventi organici e gas di origine fossile.
Lasciare che i batteri alimentino un catalizzatore metallico
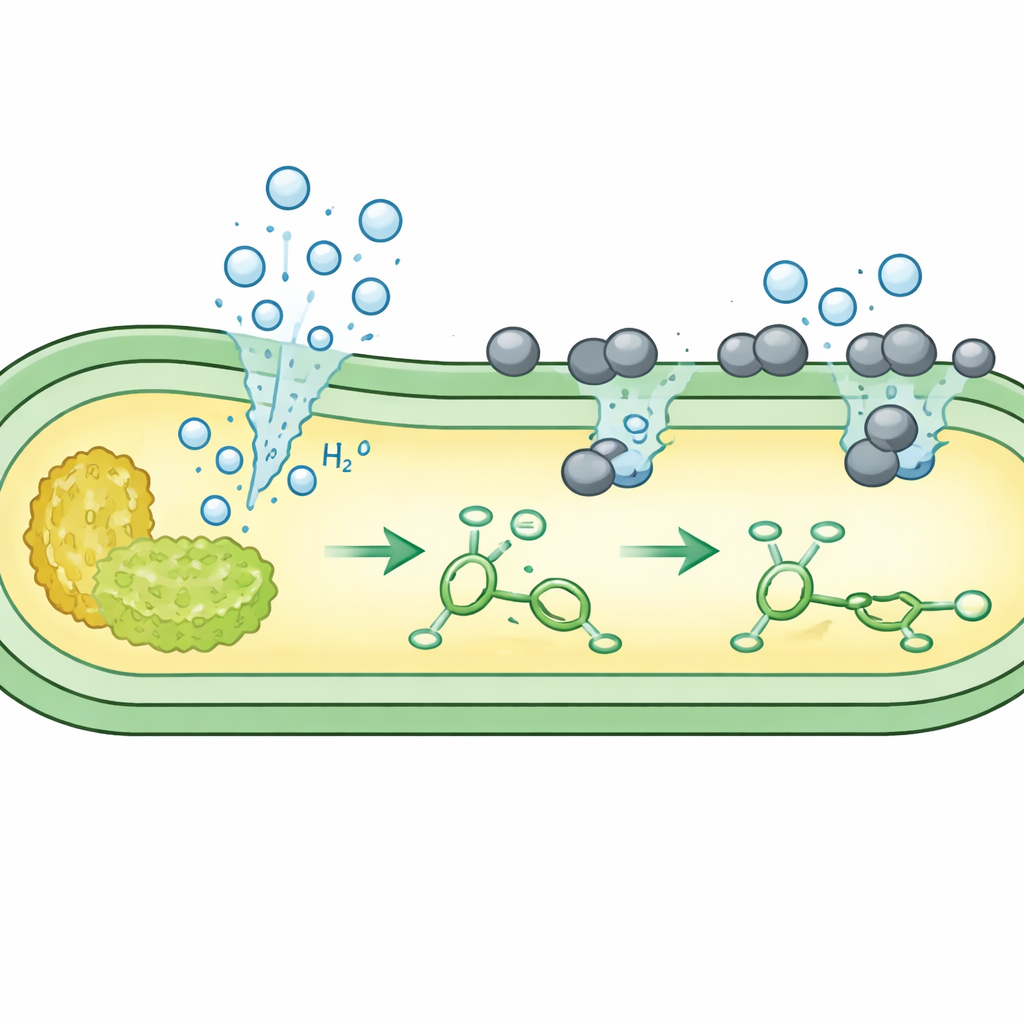
Il gruppo si è concentrato su reazioni semplici di addizione di idrogeno, in cui un doppio legame in una molecola viene “saturato” con idrogeno. Hanno coltivato diversi ceppi non modificati di E. coli in un mezzo a base di zuccheri, quindi hanno aggiunto un catalizzatore a base di palladio finemente disperso compatibile con cellule viventi. In condizioni anaerobiche, il metabolismo nativo dei batteri ha convertito lo zucchero in formiato e poi in idrogeno al lato interno della membrana cellulare. La microscopia ha mostrato che le particelle di catalizzatore cariche positivamente si adagiano sulla superficie cellulare caricata negativamente, dove incontrano l’idrogeno in uscita. Lì, il metallo usa l’idrogeno microbico per ridurre una molecola di prova, l’acido caffeico, al suo prodotto saturato con rese molto elevate — spesso migliori di quelle ottenute con un ceppo precedentemente fortemente ingegnerizzato.
Espandere il menu di prodotti e materie prime
Una volta che la reazione di base ha funzionato, i ricercatori hanno testato un’ampia gamma di molecole contenenti doppi legami carbonio–carbonio, incluse acidi di origine vegetale e composti grassi a catena lunga. Molte sono state convertite agevolmente nelle loro forme sature, alcune in rese quasi quantitative. Hanno inoltre costruito ceppi di E. coli che producono più idrogeno deviando maggior flusso metabolico verso il percorso nativo di formazione di idrogeno. Questi ceppi potenziati hanno permesso conversioni simili con meno catalizzatore metallico. In una svolta notevole, il team ha sostituito lo zucchero puro con pane di scarto liquefatto come fonte di cibo. Enzimi hanno scomposto il pane raffermo in glucosio, che i batteri hanno fermentato altrettanto efficacemente, trasformando un comune rifiuto alimentare sia in idrogeno biologico sia in prodotti chimici a valore aggiunto.
Produrre contemporaneamente ingrediente e combustibile all’interno di una singola cellula
Successivamente, gli autori si sono chiesti se un singolo batterio potesse produrre non solo il “reagente” idrogeno ma anche il “substrato” insaturo che deve modificare. Hanno ingegnerizzato E. coli in modo che lo zucchero fluisse prima in percorsi che producono precursori aromatici come gli acidi cinnamico e coumarico, e in un altro percorso che produce idrogeno. Quando la coltura aveva accumulato questi metaboliti interni, hanno aggiunto il catalizzatore al palladio. Sulla superficie cellulare, il catalizzatore ha usato l’idrogeno prodotto in situ per convertire i metaboliti di nuova formazione a doppio legame in prodotti completamente saturi come l’acido idrocinnamico, la desaminotirosina e l’acido adipico, un precursore chiave per il nylon. In alcuni allestimenti, questa cometabolizzazione ha raggiunto una conversione quasi completa, il tutto all’interno della stessa coltura vivente.
Misurare il guadagno climatico
Per valutare se questa ingegnosa biochimica aiuti davvero il pianeta, il team ha condotto una valutazione del ciclo di vita confrontando il loro approccio ibrido “chemo-microbico” con le tipiche rotte di idrogenazione basate su idrogeno fossile o elettrolitico. Quando l’idrogeno biologico e la produzione intracellulare dei substrati sono stati combinati in un unico processo efficiente dal punto di vista termico, le emissioni totali di gas serra sono calate sensibilmente. L’uso del pane di scarto come materia prima ha migliorato ulteriormente il bilancio: evitando discarica o incenerimento e trasformando alimenti scartati in prodotti chimici, alcuni scenari sono diventati complessivamente negativi in termini di carbonio, cioè rimuovono più gas serra di quanti ne emettono.
Cosa significa per la manifattura futura
In termini semplici, lo studio mostra che batteri di uso comune possono essere persuasi ad agire sia come sorgente di energia sia come fabbrica di ingredienti per reazioni chimiche importanti, mentre un solido metallico sulla loro superficie completa silenziosamente il lavoro. Poiché tutto avviene in acqua, a temperature prossime a quelle corporee e utilizzando zuccheri rinnovabili o di scarto, questo approccio potrebbe un giorno offrire alternative più pulite agli impianti petrolchimici tradizionali. Con ulteriore ingegneria dei percorsi microbici e dei catalizzatori, questa piattaforma a cellule viventi potrebbe abilitare una nuova generazione di processi sostenibili che trasformano carbonio rinnovabile e cibo scartato in prodotti utili con un’impronta climatica molto più bassa.
Citazione: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Parole chiave: idrogeno microbico, chimica verde, biocatalisi, rifiuti in prodotti chimici, produzione sostenibile