Clear Sky Science · it
Prodotti pseudo-naturali monovalenti sovralimentano la degradazione di IDO1 da parte della sua E3 nativa KLHDC3
Spegnere un enzima amico del tumore
Il nostro sistema immunitario pattuglia costantemente alla ricerca di cellule tumorali, ma i tumori spesso reagiscono di rimando sfruttando la chimica del corpo. Un attore chiave in questo braccio di ferro è un enzima chiamato IDO1, che aiuta i tumori a disarmare le cellule immunitarie. Questo studio descrive una nuova classe di piccole molecole che fa più che bloccare l’attività di IDO1: induce le cellule a eliminare l’enzima del tutto. Sfruttando i meccanismi naturali di smaltimento cellulare, questi composti potrebbero rianimare gli attacchi immunitari contro i tumori in modi che i farmaci più vecchi non riuscivano a ottenere.
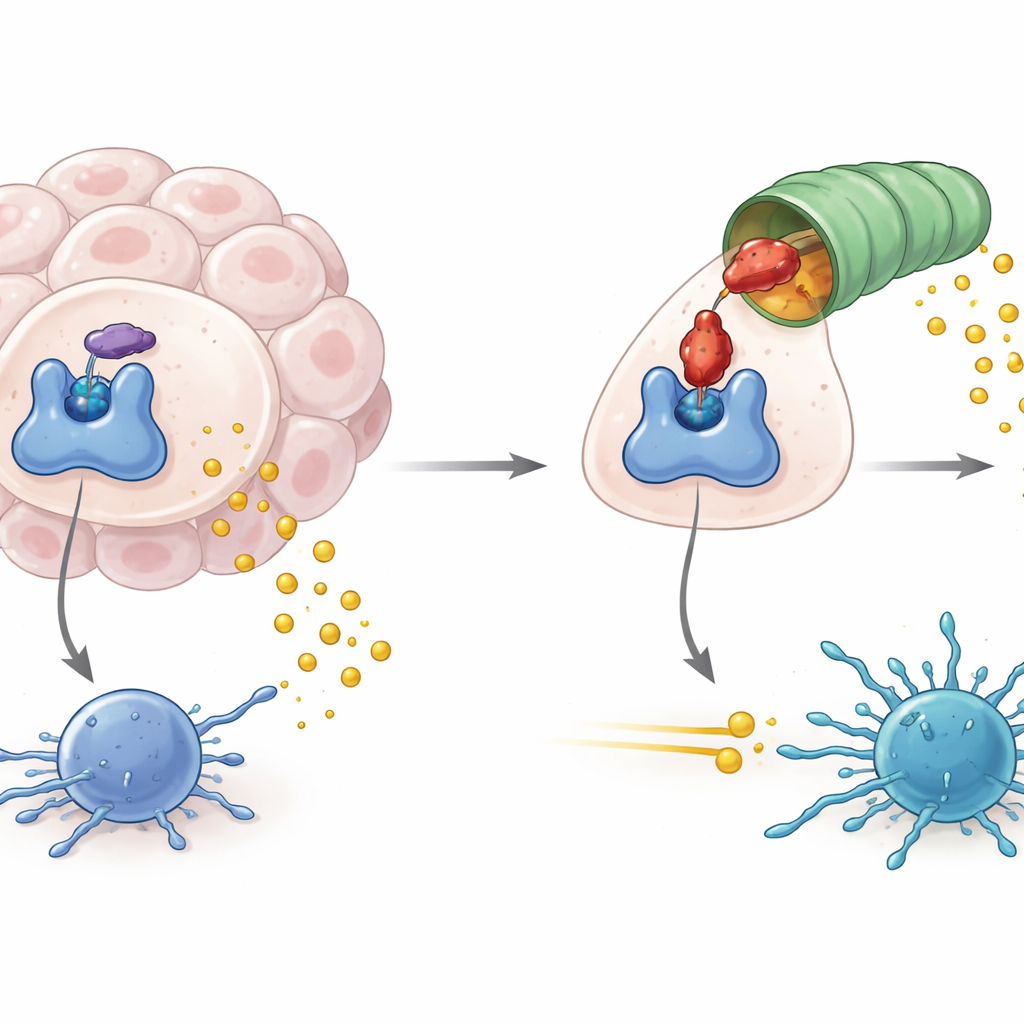
Come i tumori sfruttano un guardiano metabolico
IDO1 siede al punto d’ingresso di una via metabolica che degrada l’amminoacido triptofano in un prodotto chiamato chinurenina. Quando IDO1 è abbondante e attivo, i livelli di triptofano calano e la chinurenina aumenta, creando un ambiente chimico che attenua l’attività delle cellule immunitarie, comprese le cellule T antitumorali. Un’elevata attività di IDO1 è stata collegata non solo a una ridotta immunità antitumorale, ma anche a linfomi associati a virus e ad alcune forme di neurodegenerazione. Gli sviluppatori di farmaci si sono quindi concentrati sul bloccare l’attività enzimatica di IDO1, nella speranza di interrompere questo segnale immunosoppressivo e migliorare l’efficacia delle immunoterapie oncologiche esistenti.
Perché i semplici inibitori enzima sono risultati insufficienti
Nonostante risultati promettenti negli studi su animali, le sperimentazioni cliniche degli inibitori tradizionali di IDO1 sono state deludenti. Una spiegazione emergente è che IDO1 è più di un semplice catalizzatore. Anche quando la sua attività chimica è bloccata, la proteina stessa può agire come un centro di segnalazione che continua a favorire la crescita e la diffusione tumorale. Alcuni inibitori addirittura stabilizzano IDO1, aumentando la quantità della proteina presente nelle cellule. In altre parole, spegnere soltanto la funzione catalitica può non intaccare i ruoli pro-tumorali non enzimatici — o, peggio, può addirittura rafforzarli.
Progettare composti che innescano l’autodistruzione
Gli autori hanno setacciato una grande libreria di molecole “pseudo-naturali” — composti sintetici costruiti da frammenti ispirati a prodotti naturali ma ricombinati in modi nuovi. Hanno individuato una famiglia di molecole, chiamate iDeg, derivate da un blocco costitutivo di tipo vegetale chiamato (−)-myrtanol. Questi composti si legano nella tasca abituale di IDO1 destinata al suo cofattore contenente ferro, l’emina. Sostituendo l’emina, gli iDeg indeboliscono sia la capacità di IDO1 di produrre chinurenina sia, cosa cruciale, rimodellano parte della regione terminale della proteina. Strutture cristalline ad alta risoluzione rivelano che quando gli iDeg occupano il sito dell’emina, allentano e in parte disordinano un’elica C-terminale che normalmente è mantenuta in una conformazione compatta e protetta.
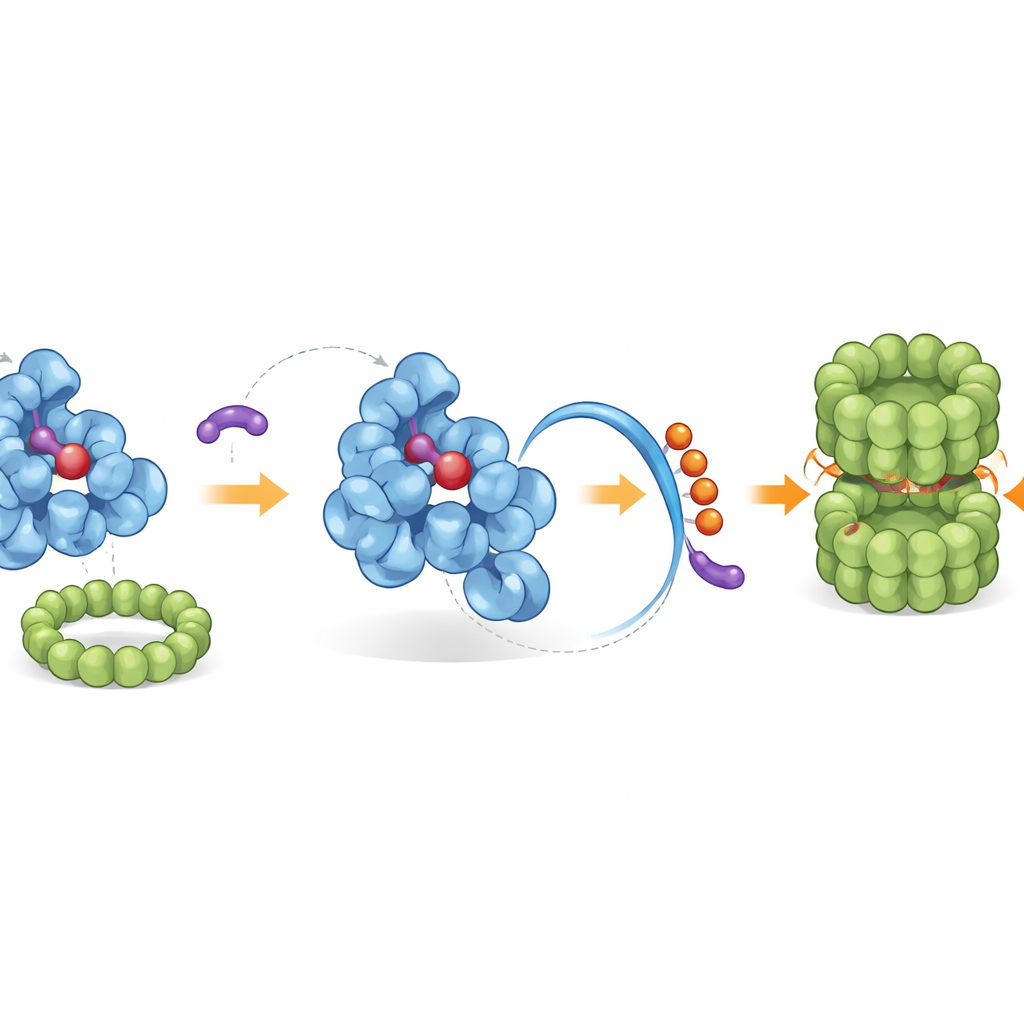
Reclutare la squadra di pulizia nativa della cellula
La coda riorganizzata espone un “tag finale” incorporato che la macchina di smaltimento cellulare riconosce. Attraverso screening genetici e ricostituzioni biochimiche, i ricercatori hanno identificato un complesso ligasico specifico, chiamato CRL2–KLHDC3, che normalmente attacca piccoli “flag” di ubiquitina alla coda esposta di IDO1, segnalandola per la distruzione da parte del proteasoma — il trituratore molecolare della cellula. In condizioni normali, solo la forma di IDO1 priva di emina viene etichettata con efficienza in questo modo, mentre l’IDO1 legata all’emina è protetta. Gli iDeg spostano questo equilibrio legandosi solo alla forma priva di emina, amplificando la via di degradazione naturale. I membri potenti della serie non solo bloccano la produzione di chinurenina, ma aumentano anche l’etichettatura con ubiquitina su IDO1 e riducono drasticamente i livelli proteici in diversi tipi di cellule tumorali.
Cambiare il destino di IDO1 — e le risposte immunitarie
Questo comportamento a doppia azione ha conseguenze funzionali importanti. In saggi di migrazione con cellule di carcinoma ovarico, un inibitore di IDO1 esplorato clinicamente che stabilizza l’enzima ha in realtà accelerato il movimento cellulare, coerentemente con il ruolo non enzimatico e pro-tumorale di IDO1. Al contrario, un composto iDeg ha rallentato la migrazione, compatibile sia con l’inibizione enzimatica sia con la perdita della proteina stessa. Lo studio scopre quindi un nuovo modo di manipolare IDO1: non trascinandolo forzatamente verso una ligasi estranea con una molecola ingombrante progettata ad arte, ma “sovralimentando” una via di degradazione nativa che esiste già nelle cellule.
Cosa potrebbe significare per le terapie oncologiche future
Per i non specialisti, il messaggio chiave è che la qualità — non solo la quantità — dell’inibizione enzimatica conta. Queste nuove piccole molecole agiscono come interruttori di precisione: bloccano IDO1 in una conformazione vulnerabile che la cellula è pronta a distruggere, tagliando sia il contributo metabolico sia quello di segnalazione alla sopravvivenza tumorale. Poiché gli iDeg sono compatti, simili a farmaci e si affidano alla ligasi della cellula per rimuovere IDO1, possono offrire un approccio più sottile e ampiamente applicabile rispetto ai precedenti farmaci “degradatori di proteine”. Se strategie analoghe possono essere applicate ad altre proteine problematiche, questo lavoro suggerisce una nuova generazione di terapie che spingono le cellule malate a smantellare le proprie armi molecolari.
Citazione: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Parole chiave: IDO1, immunoterapia oncologica, degradazione mirata delle proteine, ligasi ubiquitina, degradatori a piccole molecole