Clear Sky Science · it
Bilanciamento biocompatibile dei ligandi nella coordinazione dei metalli di transizione consente arilazione proteica innocua all'interno delle cellule
Trasformare i metalli in strumenti delicati per le cellule
Molte reazioni chimiche potenti si basano sui metalli, ma avvicinarli a sistemi viventi spesso causa problemi: danno, stress e morte cellulare. Questo studio dimostra che, con la «maniglia» molecolare giusta attorno a un atomo di nichel, è possibile eseguire una reazione sofisticata all'interno di cellule vive senza danneggiarle. Questa svolta permette agli scienziati di marcare migliaia di siti specifici sulle proteine e persino di monitorare la comparsa di patogeni difficili da seguire, aprendo nuove strade per mappare ciò che avviene nelle cellule in salute e in malattia.
Perché i metalli sono amici e nemici
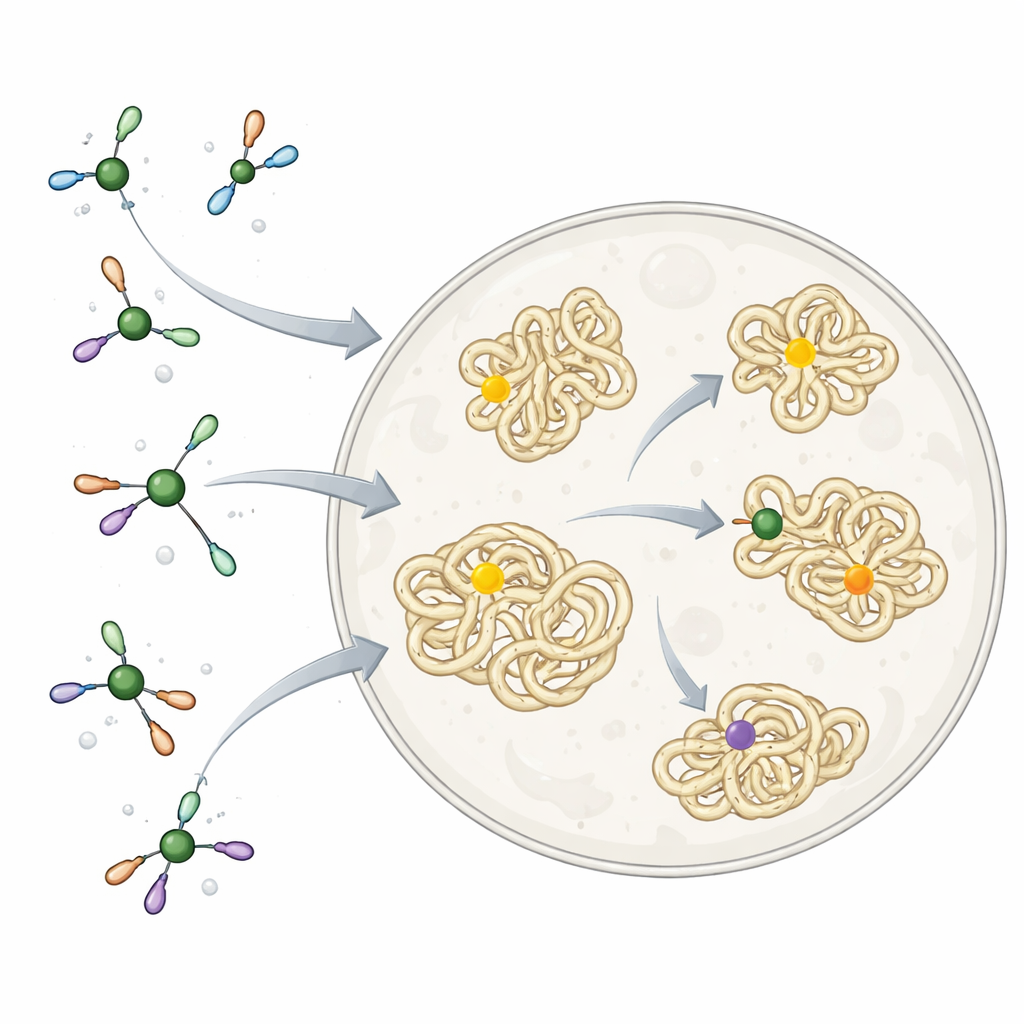
Il nichel e altri metalli agiscono già silenziosamente nel nostro organismo come componenti di enzimi naturali, ma possono anche risultare tossici se si legano nel posto sbagliato. La natura risolve questo avvolgendo i metalli con piccole molecole e proteine scelte con cura, che li indirizzano verso i bersagli giusti e bloccano reazioni indesiderate. I chimici, al contrario, spesso impiegano reagenti metallici estremamente reattivi e non ottimizzati per la vita. Questi sono stati eccellenti strumenti per costruire molecole complesse in provetta, ma troppo aggressivi per essere usati liberamente all'interno delle cellule, soprattutto quando l'obiettivo è unire un piccolo «tag» a un amminoacido specifico di una proteina senza perturbare il resto della cellula.
Progettare un reagente al nichel più gentile
I ricercatori si sono ispirati a come le cellule gestiscono il nichel. Hanno costruito una serie di complessi di nichel avvolti in un ligando semplice e biocompatibile chiamato TMEDA. Questa piccola molecola agisce come una pinza morbida: abbastanza stretta da impedire al nichel di attaccarsi ai componenti cellulari sbagliati, ma sufficientemente lassa da permettergli di compiere la reazione chiave. La reazione unisce un frammento arilico — un gruppo piatto ad anello comune nei farmaci — all'atomo di zolfo dell'amminoacido cisteina nelle proteine. Su proteine purificate in soluzione, questi complessi di nichel hanno rapidamente e selettivamente attaccato gruppi arilici a singoli siti di cisteina, funzionando su molteplici conformazioni e posizioni proteiche, a dimostrazione della compatibilità della chimica con molecole biologiche reali.
Modificare le proteine all'interno di cellule vive
Successivamente, il team ha verificato se gli stessi reagenti potessero agire all'interno di cellule vive senza essere velenosi. Hanno confrontato semplici sali di nichel, noti per la loro tossicità, con i complessi di nichel legati al TMEDA. Nelle cellule di mammifero, le fonti di nichel non protette hanno causato una morte cellulare sostanziale a dosi relativamente basse, mentre i complessi con il ligando sono risultati ben tollerati anche a concentrazioni millimolari. Questa finestra di sicurezza ha permesso ai ricercatori di esporre cellule batteriche e mammifere ai reagenti al nichel abbastanza a lungo perché penetrassero e modificassero le proteine. Inserendo un «manico» azido in una versione del gruppo arilico, hanno poi potuto legare coloranti fluorescenti o tag di biotina dopo la reazione, rivelando una marcatura chiara e dipendente dalla dose di proteine in tutto il citoplasma e il nucleo delle cellule vive.
Mappare siti proteici reattivi nell'intero proteoma
Con una reazione in cellula rapida e sicura a disposizione, gli autori l'hanno trasformata in uno strumento di scoperta. Hanno trattato cellule umane vive con il reagente al nichel contenente l'azido, poi hanno usato un tag di biotina fotocleavabile e spettrometria di massa avanzata per identificare esattamente quali cisteine erano state modificate. In un singolo esperimento hanno rilevato quasi 11.000 siti di cisteina su quasi 5.000 proteine — circa il doppio delle proteine censite da tutti gli studi precedenti di profilazione della cisteina in cellule vive messi insieme. La marcatura è stata altamente selettiva per la cisteina e ha mostrato scarso bias verso tipi proteici, localizzazioni o siti attivi noti. Notevolmente, molte delle proteine bersaglio erano considerate «non legabili» secondo gli standard attuali della scoperta di farmaci, incluse proteine di segnalazione a bassa abbondanza e sensori redox difficili da studiare solo con la genetica.
Seguire patogeni nascosti in tempo reale
La stessa chimica si è dimostrata sufficientemente sensibile anche per catturare proteine estranee espresse durante l'infezione. In cellule umane portatrici di sequenze virali latenti, il metodo ha rilevato fattori di trascrizione virali presenti a livelli estremamente bassi, incluse forme alternative dovute a splicing. Il team ha quindi infettato cellule con due patogeni molto diversi: il batterio intracellulare Chlamydia trachomatis e il virus Sindbis, un virus a RNA correlato al chikungunya. Pulsando le cellule infette con il reagente al nichel in momenti diversi, sono riusciti a intrappolare siti di cisteina su proteine ribosomiali e regolatorie batteriche chiave mentre il batterio cambiava stadio del ciclo vitale, e su proteine non strutturali virali critiche che guidano la replicazione dell'RNA. Questi siti marcati emergono ora come possibili punti deboli per future strategie antivirali o antibatteriche.
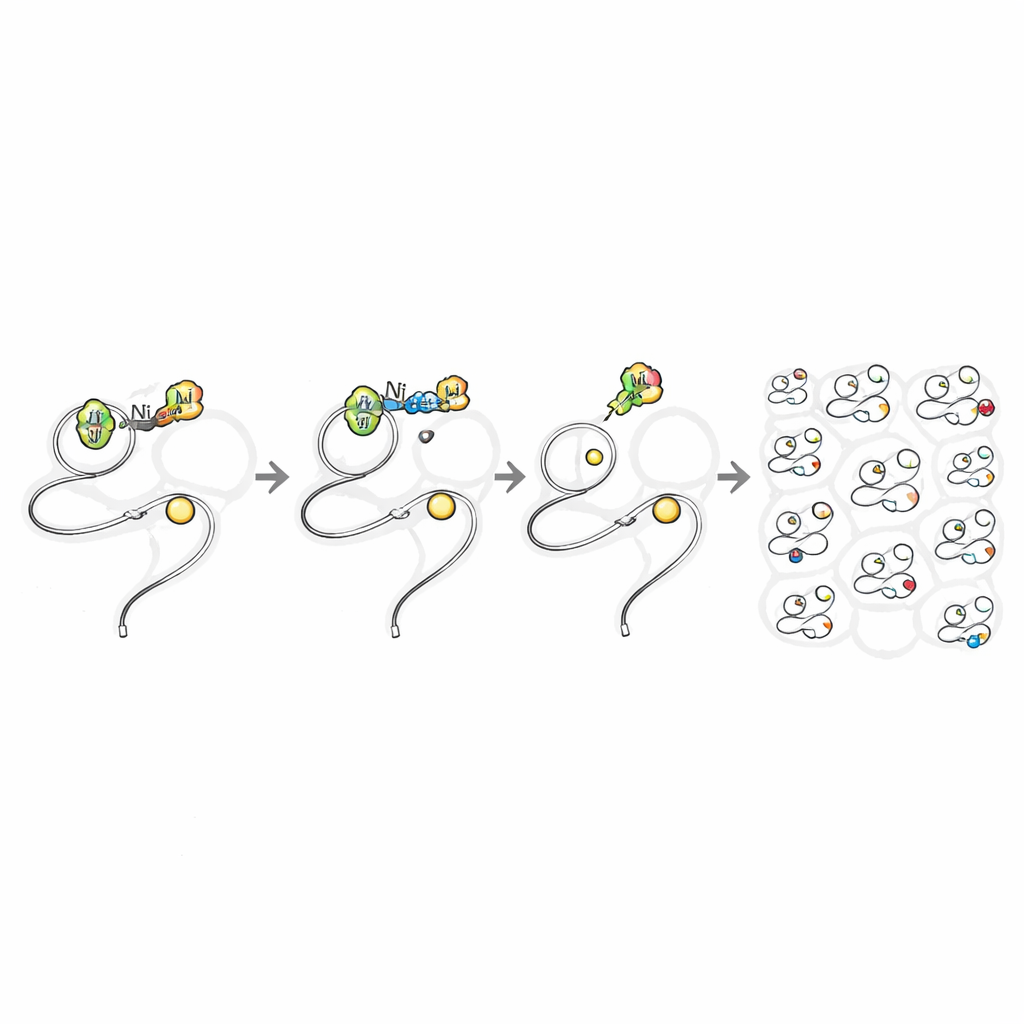
Cosa significa per la chimica cellulare futura
Bilanciando con cura il guscio di ligandi intorno al nichel, questo lavoro dimostra che un metallo tradizionalmente rischioso può eseguire una reazione covalente precisa di editing proteico nel profondo delle cellule vive con danni minimi. Ciò rende possibile tracciare una mappa funzionale dettagliata dei siti reattivi di cisteina nell'intero proteoma, incluse proteine scarse, transitorie o difficili da druggare. Offre inoltre un modo per monitorare e sondare i patogeni all'interno delle cellule ospiti a livello di singoli amminoacidi. Più in generale, lo studio suggerisce che molte altre chimiche metalliche «vietate» potrebbero essere addomesticate in modo analogo, aprendo una nuova era in cui gli strumenti potenti della chimica sintetica operano in sicurezza all'interno di sistemi viventi.
Citazione: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Parole chiave: profilazione della cisteina, bioconiugazione con nichel, marcatura proteica in cellule vive, chemioproteomica, mappatura del proteoma dei patogeni