Clear Sky Science · it
La traduzione locale specifica per RNA è modellata dai condensati per la crescita delle cellule multinucleate
Come le grandi cellule sincronizzano compiti distanti
Le cellule nei nostri tessuti sono di solito unità piccole e autosufficienti con un singolo nucleo. Ma alcuni organismi, inclusi certi funghi e le cellule muscolari, sono compartimenti enormi pieni di molti nuclei che condividono lo stesso citoplasma. In questi giganti, segnali e molecole possono impiegare molto tempo a diffusione da un punto all’altro, sollevando un interrogativo: come coordinano crescita e divisione su distanze così vaste senza perdere il controllo? Questo studio affronta la questione in un fungo multinucleato rivelando come minuscole goccioline all’interno della cellula modulino localmente la produzione proteica proprio dove serve.
Piccole goccioline che organizzano una cellula gigante
Nel fungo filiforme Ashbya gossypii, lunghe cellule tubolari chiamate ife contengono molti nuclei che si dividono fuori fase mentre la crescita avviene principalmente alle punte. Lavori precedenti avevano mostrato che una proteina chiamata Whi3 forma goccioline microscopiche, o condensati, con specifici RNA messaggeri (mRNA) che codificano regolatori chiave del ciclo cellulare e della crescita apicale. Qui, gli autori hanno voluto capire cosa fanno realmente questi condensati. Utilizzando imaging tridimensionale veloce, hanno scoperto che i condensati di Whi3 cambiano dimensione e numero a seconda della posizione nella cellula e dello stato locale di crescita e divisione nucleare. Grandi condensati si raggruppano vicino a punte ifali a crescita lenta, mentre condensati più piccoli e variabili circondano nuclei in particolari fasi del ciclo cellulare. I funghi mutanti incapaci di formare condensati normali crescono più rapidamente alle punte e mostrano divisioni nucleari più sincronizzate, suggerendo che le proprietà dei condensati aiutano a coordinare questi processi.
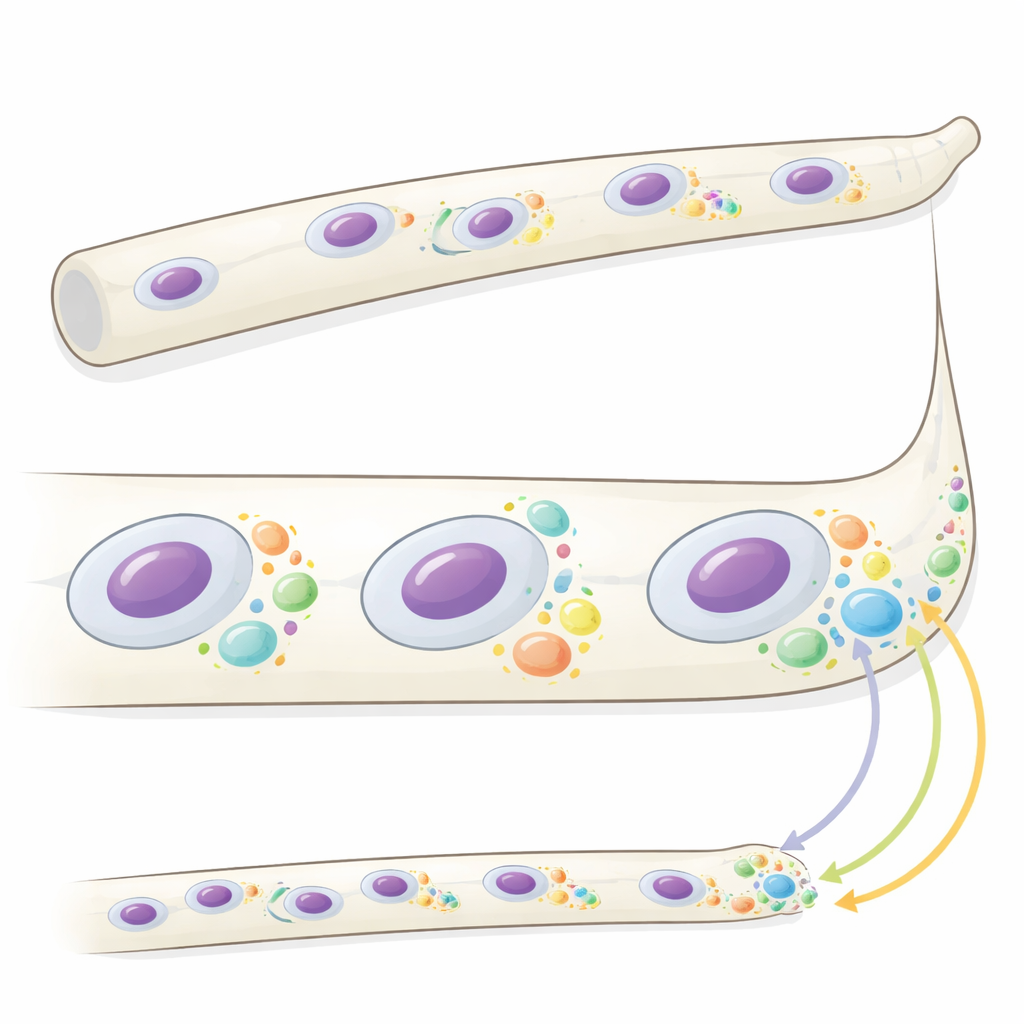
Produzione proteica locale scritta nello spazio e nel tempo
Per verificare se i condensati di Whi3 controllano dove vengono prodotte le proteine, il gruppo ha misurato la traduzione — il processo che trasforma l’mRNA in proteina — per due importanti messaggi legati a Whi3. Uno, CLN3, codifica una ciclina che aiuta a spingere le cellule attraverso il ciclo di divisione; l’altro, BNI1, codifica un fattore che modella la crescita alla punta ifale. Utilizzando un metodo fluorescente sensibile che rileva ribosomi attivi su singole molecole di mRNA endogene, i ricercatori hanno mostrato che CLN3 viene tradotto principalmente vicino a certi nuclei e solo durante fasi specifiche del loro ciclo, in particolare attorno a nuclei mitotici. L’mRNA di BNI1 si concentra alle punte ifali, ma la sua traduzione lì è solitamente scarsa e variabile. Quando il comportamento di Whi3 viene alterato da una mutazione fosfo-mimetica, la traduzione di BNI1 diventa fortemente arricchita alle punte e la crescita apicale accelera, rivelando che Whi3 può reprimere o permettere la traduzione a seconda del suo stato e della sua posizione.
Componenti minimi, molteplici output
Per verificare se questa modulazione è una proprietà intrinseca dei componenti del condensato, gli autori hanno ricreato il sistema in estratti cellulari privi di cellule. Hanno collegato un reporter luciferasi alle regioni regolatorie degli mRNA di CLN3 o BNI1 e hanno miscelato questi RNA con Whi3 purificato a diverse concentrazioni. A livelli bassi, dove non si formano goccioline, la traduzione cambiava poco. A livelli più alti che favoriscono la formazione di condensati, la traduzione legata a CLN3 era fortemente repressa all’aumentare della concentrazione di Whi3 e della dimensione dei condensati. BNI1 si comportava diversamente: livelli moderati di condensati ne aumentavano la traduzione, mentre condensati più abbondanti o più grandi invertivano il sistema in repressione. Versioni mutanti di Whi3 che formavano goccioline più piccole o meno numerose, o RNA con meno siti di legame per Whi3, spostavano queste risposte, spesso alleviando la repressione e potenziando la traduzione. Questi esperimenti mostrano che gli stessi ingredienti di base — Whi3, i suoi RNA bersaglio e i loro condensati — possono generare un continuum di stati di traduzione semplicemente variando concentrazione, forza d’interazione o dimensione delle goccioline.
Dove avviene la traduzione: al bordo della gocciolina
Le prove di massa fanno la media su molte molecole e non possono rivelare dove avviene la traduzione all’interno o attorno ai condensati. Per visualizzare direttamente questo aspetto, il team ha usato un reporter “MoonTag” che si illumina quando nuove catene proteiche emergono dai ribosomi. In vitro, hanno osservato segnali MoonTag accumularsi sulla superficie e all’interno delle goccioline Whi3–RNA, dimostrando che questi condensati possono essere effettivamente siti attivi di traduzione piuttosto che semplici depositi di stoccaggio. Colpisce il fatto che sia i ribosomi sia i segnali di proteine nascenti fossero più intensi all’interfaccia della gocciolina, formando un anello luminoso attorno a ciascun condensato. I condensati più piccoli, con più area di superficie rispetto al volume, supportavano più traduzione per RNA rispetto alle goccioline più grandi, che erano complessivamente più represse. Modificare la valenza dell’RNA o lo stato di carica di Whi3 spostava la zona permissiva alla traduzione dalla superficie a regioni più interne, indicando che sottili caratteristiche molecolari del condensato regolano quanto facilmente la macchina di traduzione può accedere agli RNA residenti.
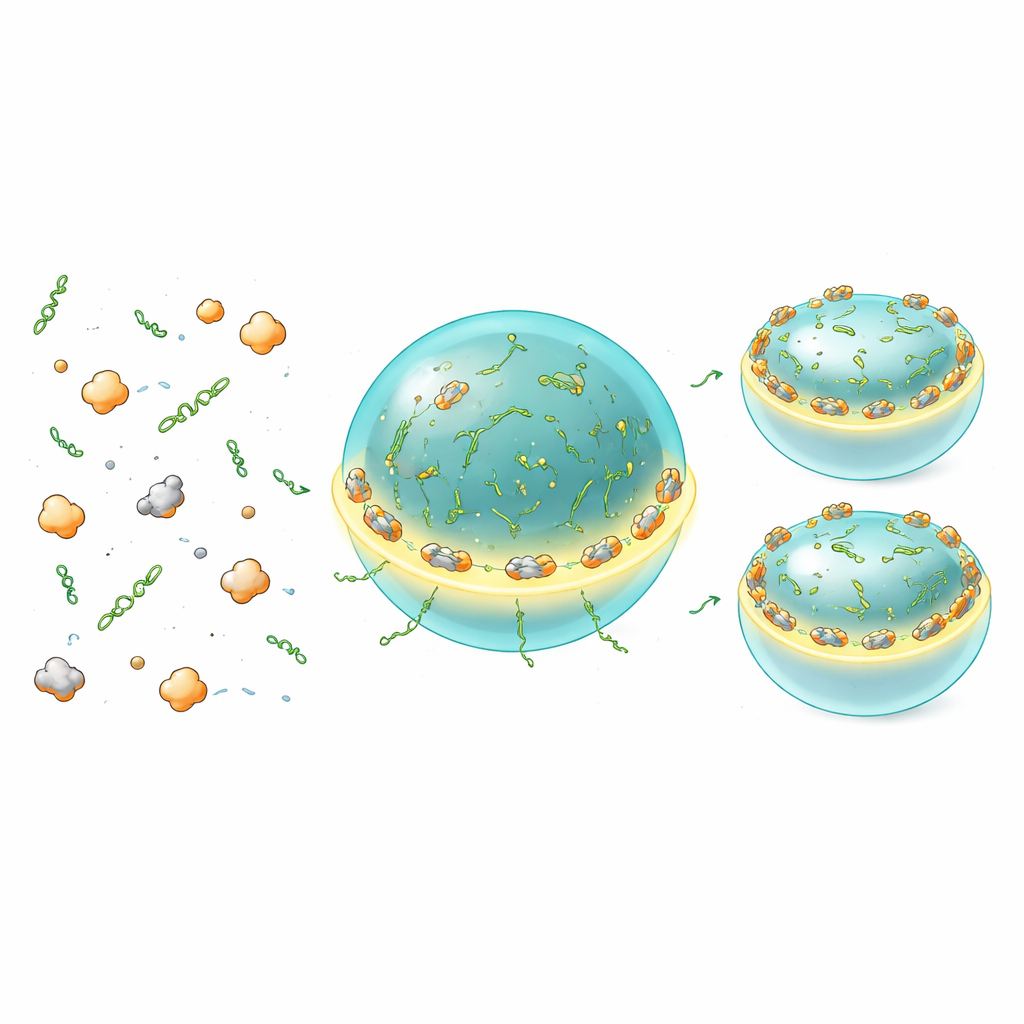
Dosi finemente regolate per una crescita bilanciata
Complessivamente, il lavoro ritrae i condensati Whi3–RNA come valvole regolabili che dosano la produzione proteica locale invece di semplici interruttori acceso–spento. Nel fungo, questo significa che la ciclina CLN3 può essere prodotta a impulsi attorno a nuclei selezionati per mantenere i loro cicli di divisione fuori fase, mentre BNI1 può essere sintetizzata in raffiche intermittenti alle punte ifali per sostenere la crescita evitando un’espansione incontrollata in un unico sito. Quando la formazione o le proprietà dei condensati vengono disturbate, questo controllo sottile si perde: la produzione proteica diventa più uniforme nello spazio e nel tempo, i nuclei si dividono in modo sincrono, cambiano gli schemi di ramificazione e la morfologia complessiva si altera. Per un pubblico generale, il messaggio chiave è che le cellule possono utilizzare piccole goccioline separate per fase come reattori spazialmente e temporalmente modulabili, permettendo a grandi cellule multinucleate di coordinare crescita e divisione su lunghe distanze scolpendo localmente quando e dove le proteine vengono prodotte.
Citazione: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Parole chiave: condensati biomolecolari, traduzione locale, controllo del ciclo cellulare, ife fungine, separazione di fase