Clear Sky Science · it
Ubiquitinazione su lisina-11 guida l’induzione degli interferoni di tipo I/III da parte di cGAS–STING e dei Toll-like receptor 3 e 4
Come le nostre cellule danno l’allarme
Quando virus o molecole pericolose invadono l’organismo, le nostre cellule devono decidere nel giro di pochi minuti se attivare potenti segnali antivirali chiamati interferoni. Questi segnali possono salvarci da infezioni gravi, ma se scattano in modo inappropriato possono anche promuovere malattie autoimmuni dannose. Questo studio rivela un “centralino” molecolare finora nascosto nelle cellule che aiuta a decidere quando accendere le risposte a interferone e quando invece frenarle. Comprendere questo centralino offre indizi per vaccini migliori, terapie antivirali e trattamenti per disturbi guidati dagli interferoni.
Guardiani che percepiscono il pericolo
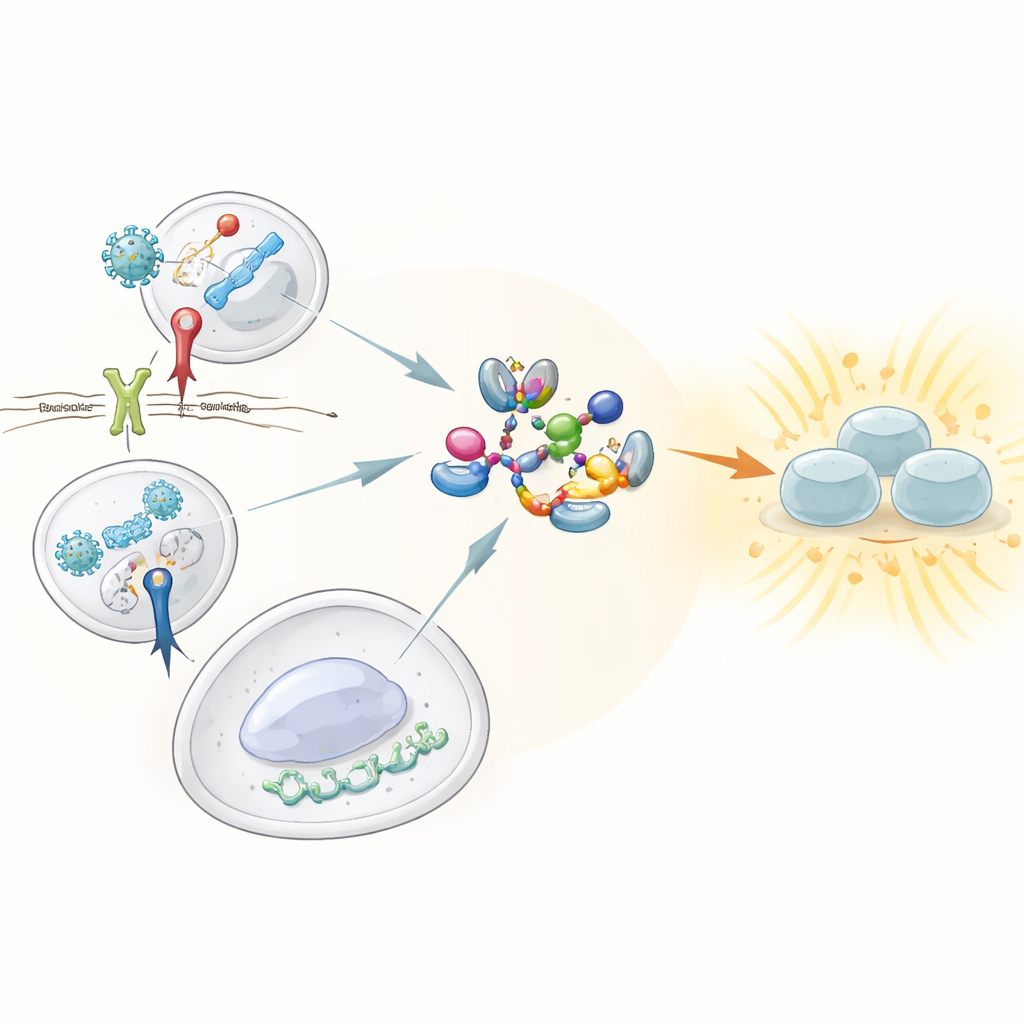
Il nostro sistema immunitario innato si basa su sentinelle note come recettori di riconoscimento del pattern, che pattugliano alla ricerca di caratteristiche riconoscibili di virus e batteri. Tra questi, tre emergono per la loro capacità di scatenare forti risposte a interferone: il Toll-like receptor 3 (TLR3), che rileva l’RNA virale a doppio filamento; il Toll-like receptor 4 (TLR4), che riconosce un componente delle pareti batteriche; e la via cGAS–STING, che individua DNA estraneo nel posto sbagliato all’interno delle cellule. Tutti e tre devono attivare un enzima centrale chiamato TBK1, che a sua volta attiva il fattore di trascrizione IRF3 per promuovere la produzione di interferoni di tipo I e III. Finora non era chiaro come questi sensori convergessero su TBK1 per attivarlo.
Un collegamento molecolare nascosto
I ricercatori hanno scoperto che una proteina chiamata ANKIB1 funge da connettore cruciale tra questi sensori e TBK1. ANKIB1 è un enzima che attacca piccoli marcatori molecolari, noti come catene di ubiquitina, ad altre proteine. Importante è che costruisce un tipo specifico di catena, basata su un legame chiamato “K11”, precedentemente noto più per ruoli nella divisione cellulare che per l’immunità. Nelle cellule umane prive di ANKIB1, la stimolazione di TLR3 o l’attivazione di STING non provocava più la corretta attivazione di TBK1 e IRF3, e i geni degli interferoni venivano scarsamente espressi. Ripristinare ANKIB1 ha riportato la risposta, dimostrando che questo singolo enzima è sia necessario sia sufficiente per guidare questo ramo dell’allarme antivirale.
Costruire una piattaforma di aggancio per le proteine di rilancio
Un’analisi più approfondita ha rivelato come ANKIB1 eserciti la sua influenza. Quando TLR3 o STING rilevano il pericolo, assemblano piattaforme multiproteiche chiamate signalosomi. ANKIB1 viene reclutato su queste piattaforme tramite una regione che riconosce l’ubiquitina. Una volta lì, decora diversi componenti chiave — inclusi gli adattatori TRIF e lo stesso STING, oltre ad altre molecole di segnalazione — con catene di ubiquitina legate in K11. Queste catene non marchiano semplicemente le proteine per la degradazione; agiscono piuttosto come un Velcro molecolare. Un’altra proteina, Optineurina (OPTN), viene attratta specificamente da questi siti modificati. Funzionando come adattatore di collegamento, OPTN porta quindi TBK1 nel complesso in modo che possa essere attivato e trasmettere il segnale a IRF3 e ai geni degli interferoni. Quando OPTN veniva rimossa, l’attivazione di TBK1 crollava, sottolineando che la marcatura K11 operata da ANKIB1 e il legame con OPTN costituiscono un unico asse essenziale.
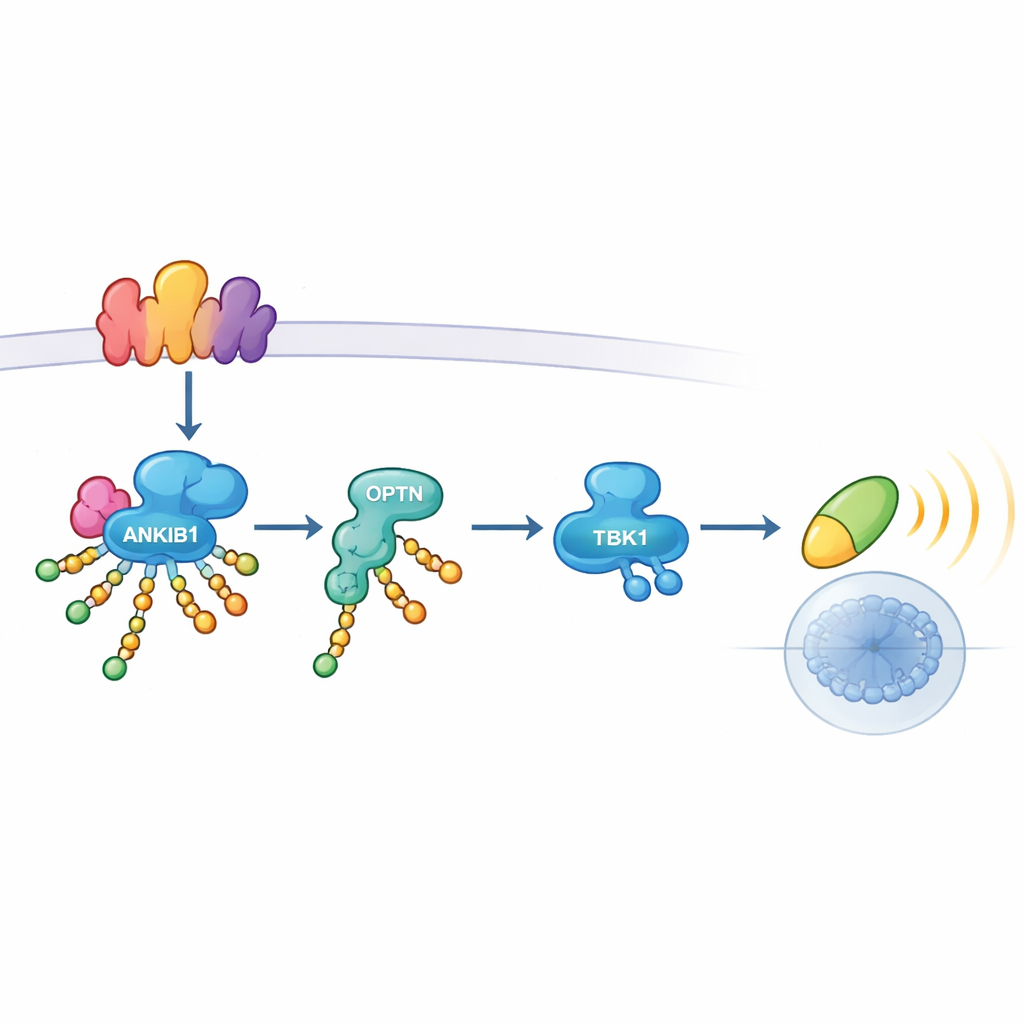
Quando questa via è importante — e quando non lo è
Il gruppo ha quindi indagato se questo meccanismo fosse universale per tutti i sensori antivirali. Hanno scoperto che ANKIB1 è vitale per l’induzione di interferone tramite TLR3, per il braccio dipendente da TRIF di TLR4 e per la via cGAS–STING, tutte vie che utilizzano OPTN come principale adattatore per TBK1. Al contrario, un altro sensore, RIG-I, che rileva RNA virale, si basa su un diverso insieme di proteine adattatrici e non necessita di ANKIB1 o OPTN per attivare TBK1. Esperimenti nel topo hanno rispecchiato questi risultati cellulari. Gli animali privi di Ankib1 producevano molta meno quantità di interferone dopo l’attivazione di TLR3 o STING, erano protetti da una sindrome infiammatoria letale guidata dagli interferoni, ma diventavano molto più vulnerabili all’infezione da herpes simplex virus 1, un virus a DNA che dipende fortemente dalla risposta interferon-mediata da cGAS–STING per essere controllato. Le risposte all’influenza, rilevata principalmente da RIG-I, rimanevano in gran parte intatte.
Bilanciare protezione e danno
Nel loro insieme, questi risultati rivelano le catene di ubiquitina legate in K11 generate da ANKIB1 come una valuta centrale in un ramo importante della segnalazione antivirale innata. Creando siti di aggancio per OPTN, ANKIB1 contribuisce ad assemblare il preciso circuito molecolare che converte il pericolo percepito da TLR3, TLR4 (attraverso TRIF) e cGAS–STING in una robusta produzione di interferoni. Questo asse è a doppio taglio: è essenziale per la difesa contro alcuni virus, ma alimenta anche malattie infiammatorie guidate dagli interferoni quando è iperattivato. Poiché l’attività catalitica e i domini specifici di ANKIB1 sono necessari per questa funzione, essi rappresentano bersagli interessanti per futuri farmaci mirati sia ad attenuare risposte interferoniche dannose nelle condizioni autoimmuni, sia a potenziare l’immunità antivirale dove è troppo debole.
Citazione: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Parole chiave: immunità innata, segnalazione degli interferoni, ubiquitinazione, via cGAS–STING, infezione virale